はじめに——「骨折が寿命を縮める」という不都合な真実
「骨折したくらいで死ぬわけではない」と思っていませんか。
現実は少し残酷です。大腿骨近位部骨折(いわゆる「股関節の骨折」)を起こした高齢者の約20〜30%が、骨折後1年以内に亡くなります。原因は骨折そのものではなく、長期臥床による肺炎・深部静脈血栓・筋力低下の連鎖です。ゾレドロン酸(ビスホスホネート系静注薬)の基盤的RCT(大規模無作為化比較試験)では、大腿骨近位部骨折後の患者に薬を投与したところ、全死因死亡が28%低下しました [20]。骨粗鬆症治療は「骨を守る」と同時に「命を守る」治療なのです。
骨粗鬆症(こつそしょうしょう:英語 Osteoporosis)は「骨の強度が低下して骨折しやすくなる骨格疾患」です。世界の高齢者における有病率を40研究・約79,000名でまとめたメタ分析(統合解析)では、60歳以上の女性で特に有病率が高く、地域によっては50%を超えます [1]。日本でも推定1,590万人が骨粗鬆症または骨粗鬆症のリスク状態にあるとされています。
この記事では、2025年に10年ぶり改訂された日本骨粗鬆症学会ガイドラインを軸に、「骨を壊す薬」から「骨を作る薬」への治療パラダイムシフト、そして40代から今日始められる実践的な骨の「貯金」戦略をお伝えします。
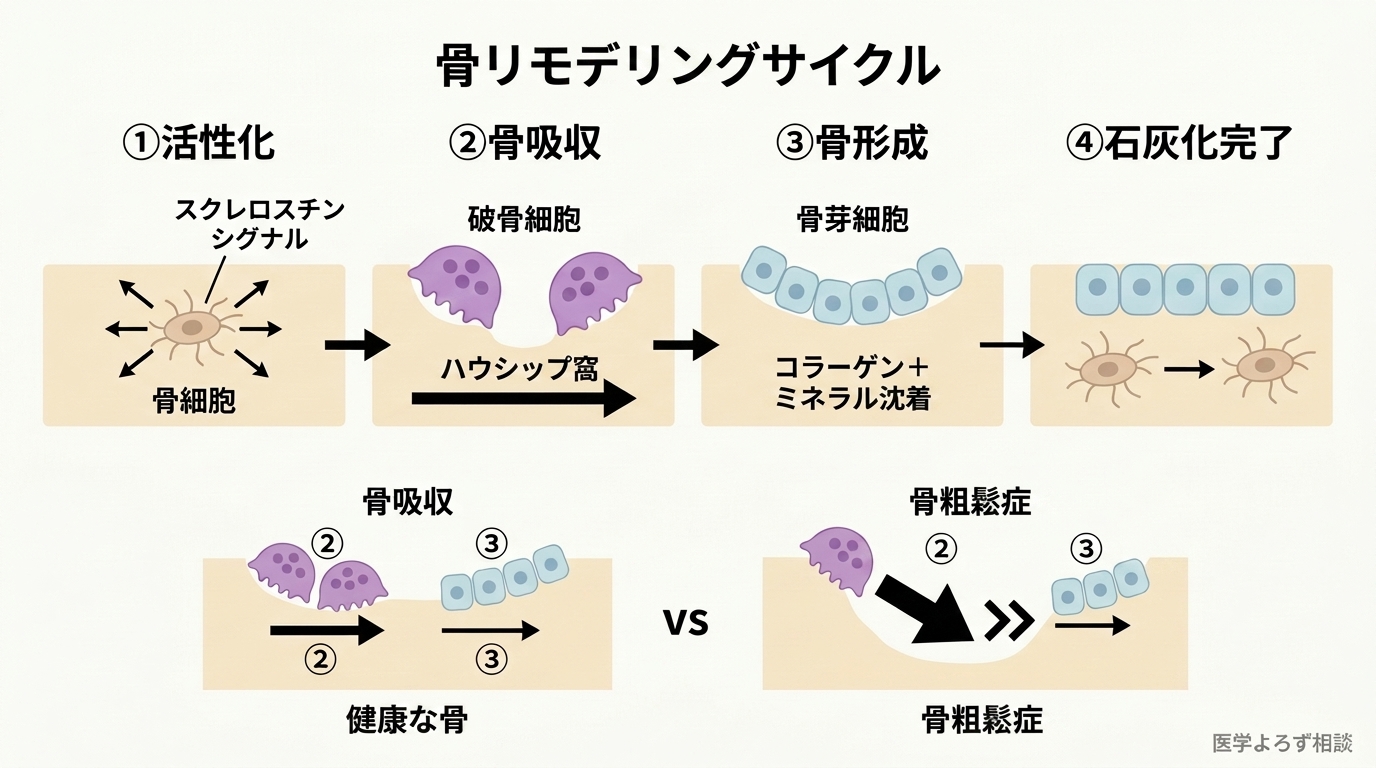
骨は生きている——リモデリングの精密なバランス
「骨は一度できたら変わらない」と思われがちですが、それは誤解です。成人の骨格は約10年で全て入れ替わる動的な組織です。この再構築プロセスを「骨リモデリング(bone remodeling)」と呼びます。
リモデリングには3種類の細胞が関わります。
- 破骨細胞(はこつさいぼう:英語 Osteoclast):古い骨を酸と酵素で溶かして除去する「解体屋」
- 骨芽細胞(こつがさいぼう:英語 Osteoblast):コラーゲンを分泌して新しい骨を形成する「建設業者」
- 骨細胞(こつさいぼう:英語 Osteocyte):骨の中に埋め込まれてリモデリング全体を調節する「管理棟」
健康な状態では解体と建設が釣り合っています。骨粗鬆症とは、このバランスが崩れ、解体が建設を上回り続ける状態です。エストロゲン(女性ホルモン)が閉経で急減すると、破骨細胞の抑制が外れて骨吸収が加速します。加齢によって骨芽細胞の活性も低下します。二重の打撃で、骨量は急速に失われていきます。
ピークボーンマスから下り坂へ——年齢と骨密度の関係
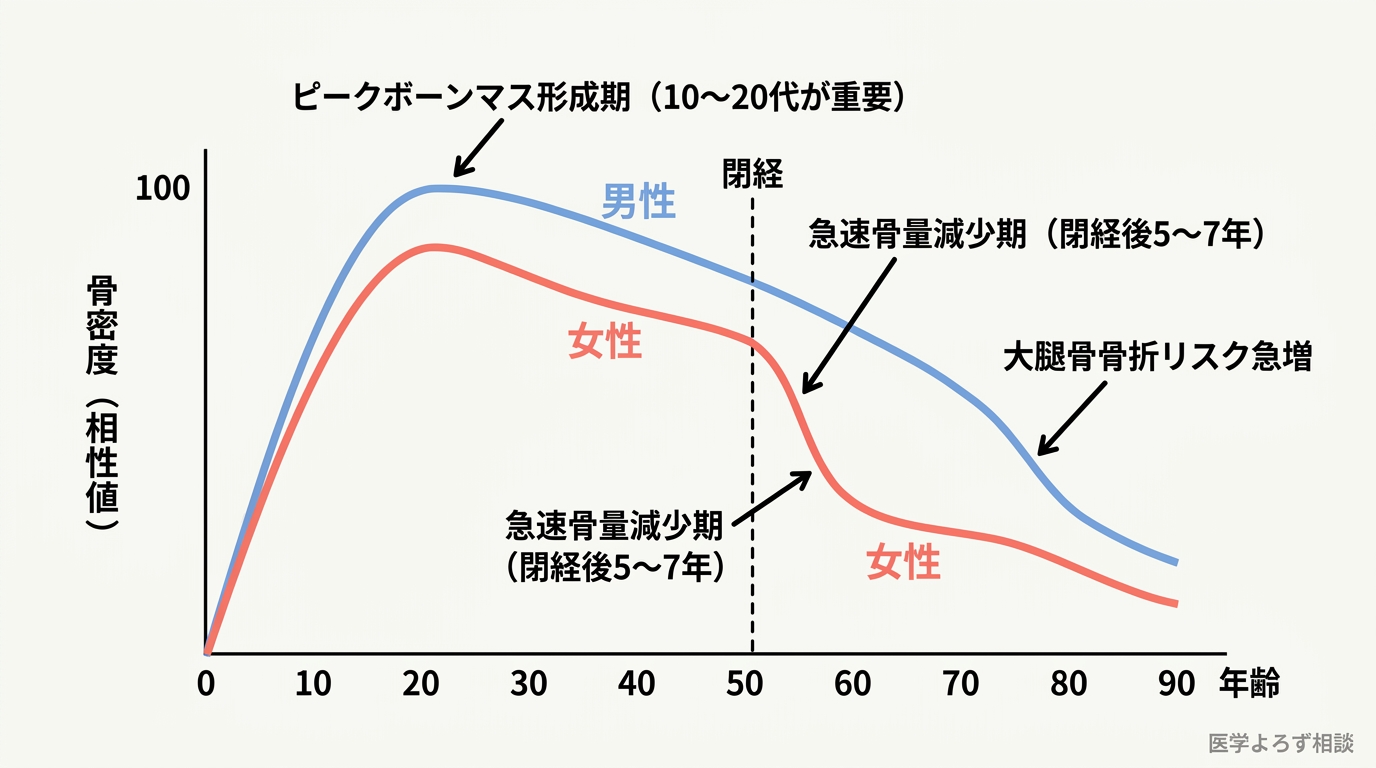
骨密度は生涯を通じて均一に変化するわけではありません。いくつかの「転換点」があります。
思春期〜20代前半が骨量の形成ピークです。この時期に達する最大骨量を「ピークボーンマス(Peak Bone Mass: PBM、最大骨量)」と呼びます。遺伝的要因が60〜80%を占めますが、カルシウム摂取・運動・日照の影響も大きい。10代に十分な骨を蓄えることが、60代の骨折リスクを左右します。
30代後半〜40代からは、男女ともにゆるやかな骨量減少が始まります。ただし、この時期は年間0.3〜0.5%程度の緩やかな傾斜です。
閉経前後(平均51歳)から女性の骨量減少は劇的に加速します。閉経後5〜7年間で骨量の15〜20%が失われるとされており、これが女性の骨粗鬆症リスクが男性の2〜3倍に達する主要因です。
70〜80代では男性も皮質骨(緻密骨)の薄化が顕著になり、大腿骨近位部骨折リスクが急増します。
日本の現状——1,590万人が「骨折予備軍」
骨粗鬆症は「サイレントディジーズ(沈黙の病気)」と呼ばれます。痛みもなく、ゆっくりと骨量が失われていき、骨折が起きて初めて発覚することが多いのです。
日本の現状を数字で整理すると:
- 推定患者数:1,590万人(骨粗鬆症:約1,280万人、骨量減少:約310万人)
- 治療率の低さ:骨折後でさえ適切な骨粗鬆症治療を受けているのは約30%以下
- 骨折連鎖:1回骨折した人は次の骨折リスクが1.5〜3倍に増加
- 経済的コスト:大腿骨近位部骨折1件あたりの医療費は急性期だけで150〜200万円
特に問題なのは「骨折の連鎖」です。椎体骨折(背骨の圧迫骨折)は無症状のことも多く、気づかないまま放置されると、次の骨折が起きやすくなります。1回の椎体骨折が確認されれば、次の1年以内に別の椎体骨折が起きるリスクは5倍以上に跳ね上がります。
骨粗鬆症の世界有病率を高齢者で最大規模に調査したメタ分析(86研究)では、特に高齢女性での罹患率が非常に高く、地域差・人種差が大きいことも示されており、日本を含むアジア系では骨折リスクの上昇に注意が必要です [1]。
診断の進化——DXAからTBS、FRAXへ
DXA——骨の「量」を測る標準検査
骨粗鬆症の標準的な診断には DXA(二重エネルギーX線吸収測定法: Dual-energy X-ray Absorptiometry、骨密度測定) が使われます。腰椎と大腿骨近位部のBMD(骨密度: Bone Mineral Density)を測定し、若い成人の平均値と比較した「Tスコア」で評価します。
- Tスコア ≧ −1.0:正常
- Tスコア −1.0〜−2.5:骨量減少(osteopenia)
- Tスコア ≦ −2.5:骨粗鬆症
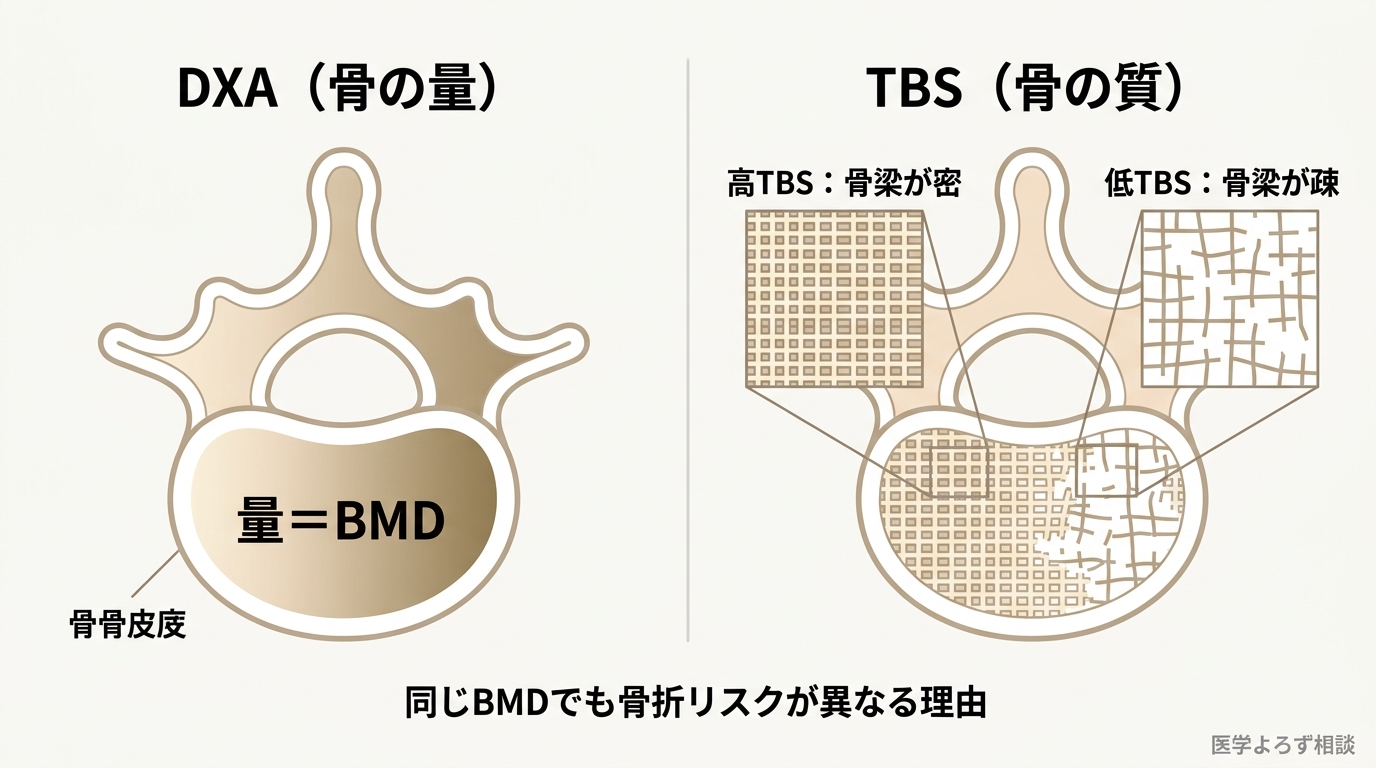
ただし、BMDだけでは骨折リスクを十分に予測できないことが分かってきました。同じBMDでも骨折する人としない人がいるのは、「骨の量」以外に「骨の質」が関係するからです。
TBS——骨の「質」を映す新指標
TBS(骨梁スコア: Trabecular Bone Score、骨の微細構造を評価するスコア) は、DXA画像から骨梁(こつりょう:骨の内部の格子状構造)の質を数値化する指標です。同じBMD画像を使いながら、BMDとは独立して骨折リスクを予測できます [16]。
TBSは特に、BMDが「正常〜骨量減少」の範囲でも骨折を繰り返す患者の評価に有用です。糖尿病・ステロイド投与・クッシング症候群などでは、BMDが正常でも骨の質が低下しているケースがあり、TBSがこれを捉えます。最新のガイドラインでは、TBSをFRAXに統合する方法も推奨されています [16]。
FRAX——10年骨折リスクを計算する
FRAX(骨折リスク評価ツール: Fracture Risk Assessment Tool) は、BMDや骨折歴・喫煙・飲酒・ステロイド使用などの臨床的リスク因子を組み合わせて、向こう10年間の主要骨粗鬆症性骨折(MOF)と大腿骨近位部骨折のリスク(%)を計算するツールです。
FRAXは無料のオンラインツールとして公開されており、日本語版もあります(https://www.sheffield.ac.uk/FRAX/)。「BMDは正常だが複数のリスク因子がある」といったケースの治療判断に特に役立ちます。
薬物治療の最前線——「壊す速度を抑える」から「つくる力を呼び覚ます」へ
骨粗鬆症の薬物治療は、作用機序によって大きく3種類に分けられます。
| 分類 | 代表薬 | 作用 |
|---|---|---|
| 骨吸収抑制薬 | ビスホスホネート、デノスマブ | 破骨細胞の働きを抑えて骨量減少を止める |
| 骨形成促進薬 | テリパラチド、アバロパラチド | 骨芽細胞を刺激して新しい骨を作る |
| 二重作用薬 | ロモソズマブ | 骨吸収を抑えつつ骨形成を同時に促進 |
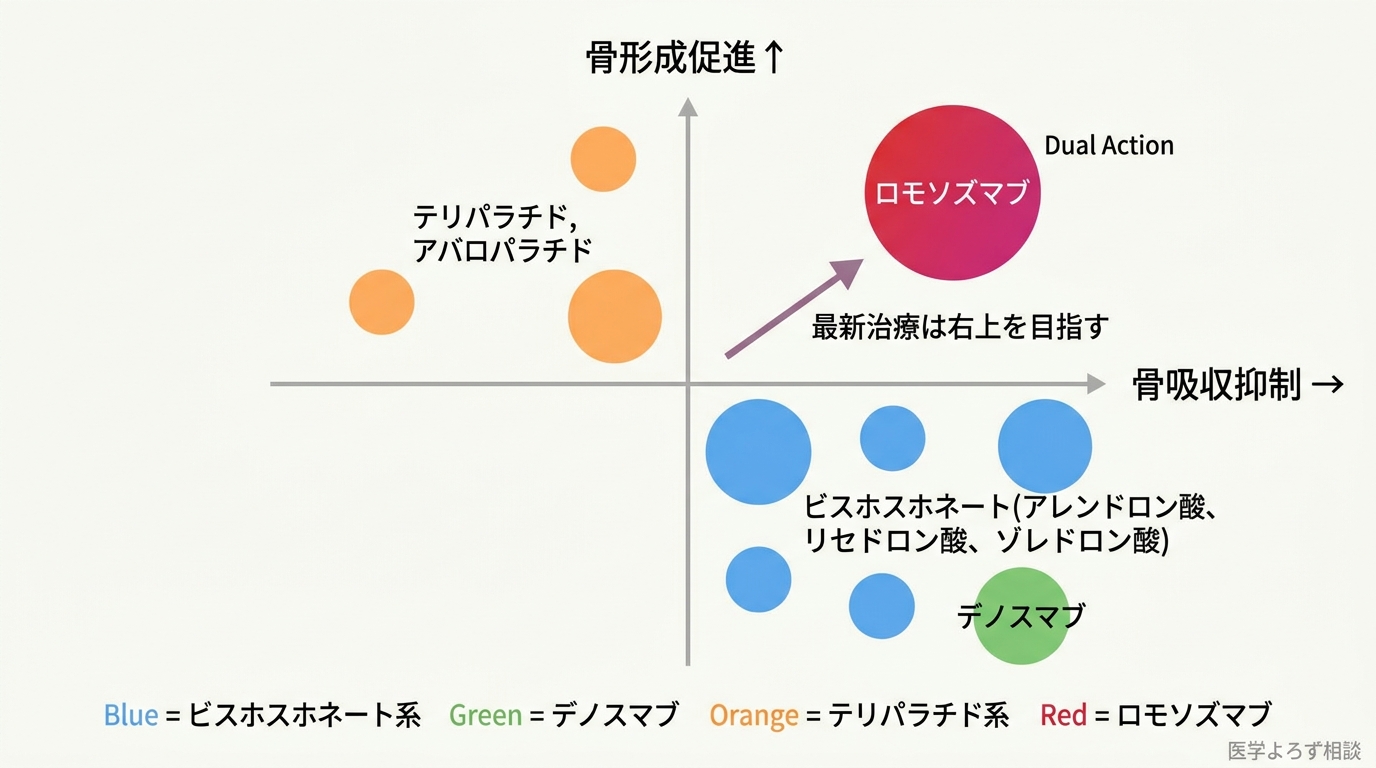
ビスホスホネート——最も使われてきた土台の薬
ビスホスホネート(BP)は、骨吸収抑制薬の代表格です。破骨細胞が骨表面に付着するのを妨げ、骨量減少を止めます。アレンドロン酸(経口週1回)・リセドロン酸(経口週1回または月1回)・ゾレドロン酸(年1回静注)など複数の剤型があります。
ACP(米国内科学会)が推奨する骨粗鬆症治療のリビングネットワークメタ分析(生きた統合解析:継続的にエビデンスを更新)は、ビスホスホネート・デノスマブ・ロモソズマブをはじめ全ての主要薬が骨折リスクを有意に低下させることを示しています [3]。一方で、長期使用(5〜10年以上)では非定型大腿骨骨折(AFF)と顎骨壊死(ONJ)のリスクが微増することも確認されており、定期的なリスク評価が重要です [3]。
ゾレドロン酸——唯一「死亡率を下げた」薬
大腿骨近位部骨折後の患者2,127名を対象とした HORIZON-RFT(高リスク患者へのゾレドロン酸試験)では、ゾレドロン酸の年1回静注が臨床骨折を35%低下させるとともに、全死因死亡を28%低下させる唯一の骨粗鬆症薬であることが示されました [20]。骨折後の入院機会に投与できる利便性とともに、死亡率改善効果は特筆に値します。
デノスマブ——長期使用で骨量増加が止まらない
デノスマブ(Denosumab) はRANKL(ランクル:破骨細胞を活性化するシグナル分子)を阻害するモノクローナル抗体(生物学的製剤)です。皮下注射を6カ月ごとに行います。
FREEDOM試験(7,868名、3年間)では椎体骨折68%低下、大腿骨近位部骨折40%低下という強力なエビデンスが示されました [18]。さらに10年間の長期延長試験では、骨量増加がプラトー(頭打ち)にならず増加し続け、重篤な有害事象も低率を維持していました [6]。
最新のメタ分析でも、デノスマブはビスホスホネートと比較して椎体骨折をより低く抑えることが示されています [7]。ただし、投与を突然中止すると急速な骨量減少と多発骨折のリスクがあるため、中止後は必ずビスホスホネートなど別の骨吸収抑制薬に切り替える必要があります。
ロモソズマブ——2020年代の治療革命
ロモソズマブ(Romosozumab) は骨粗鬆症治療の概念を変えた薬です。スクレロスチン(Sclerostin:骨形成を抑制する蛋白質)を阻害することで、骨形成を促進しながら骨吸収も抑制する「二重作用」を持ちます。月1回の皮下注射で使用します。
FRAME試験(7,180名)では、12カ月間のロモソズマブ投与で椎体骨折リスクが73%低下(0.5% vs 1.8%)しました [4]。
さらに重要なのがARCH試験(4,093名)です。ロモソズマブとアレンドロン酸(ビスホスホネート)を直接比較したところ、ロモソズマブ群で椎体骨折が48%減少、臨床骨折(非椎体+症候性椎体骨折)が27%減少、大腿骨近位部骨折が38%減少しました [5]。ただし心血管系有害事象(心筋梗塞・脳卒中)がロモソズマブ群でわずかに多く(2.5% vs 1.9%)、心血管疾患の既往がある患者には使用禁忌となっています [5]。
閉経後女性を対象とした骨粗鬆症治療のネットワークメタ分析(BMJ、2023年)では、骨形成促進薬(ロモソズマブ・テリパラチド等)がビスホスホネートよりも骨折予防効果で上回ることが示されています [2]。
テリパラチドとアバロパラチド——骨を「作る」注射薬
テリパラチド(Teriparatide) は副甲状腺ホルモン(PTH: Parathyroid Hormone)の活性断片(1-34フラグメント)を合成したものです。毎日の自己注射で骨芽細胞を刺激し、骨形成を促します。
基盤となるNeer試験(1,637名)では椎体骨折リスクが65%低下(RR 0.35)という劇的な効果が示されました [19]。
PTH1受容体作動薬を比較したネットワークメタ分析では、アバロパラチド(Abaloparatide)がテリパラチドより非椎体骨折・大腿骨近位部骨折において有利であることが示されています [8]。
逐次療法——「作ってから守る」戦略
骨粗鬆症治療で重要な概念が逐次療法(Sequential Therapy:骨形成促進薬から骨吸収抑制薬への引き継ぎ)です。
テリパラチド→デノスマブと切り替えた DATA-Switch 試験の結果は明確です [9]:
- テリパラチド→デノスマブ切替:BMD(骨密度)が増加し続ける
- デノスマブ→テリパラチド切替:急速な骨量減少が起きる
つまり、「骨を作る薬で土台を高め、骨吸収抑制薬で守り固める」のが正しい戦略です。逆の順番は骨量を失うリスクがあります。
2025年に10年ぶりに改訂された日本骨粗鬆症学会ガイドライン(GL 2025) では、ロモソズマブが「骨形成促進薬」として正式追加(エビデンスA、合意率93.8%)されました [17]。骨形成促進薬→骨吸収抑制薬の逐次療法が明確に推奨されており、日本の治療戦略も国際水準に到達しています [17]。
ビタミンDとカルシウム——「飲めば安心」の落とし穴
ビタミンDとカルシウムのサプリメントは「骨に良い」というイメージが定着しています。しかし、最新のエビデンスはより細かい状況を示しています。
大規模なメタ分析(33研究、51,145名)によると、地域在住の高齢者に対するカルシウム単独・ビタミンD単独・カルシウム+ビタミンD併用のいずれも、骨折リスクの低下と有意な関連がないことが示されました [10]。「飲めば骨折が防げる」という単純な話ではないのです。
一方、別の大規模ネットワークメタ分析では異なる結果も出ています [11]:
- ビタミンD単独:効果なし
- ビタミンD+カルシウムを毎日投与した場合:全骨折が6%減少、大腿骨近位部骨折が16%減少
つまり、カルシウムとビタミンDを連日一緒に摂取した場合に限って効果があるという限定的なエビデンスです。間欠的な大量投与や単独サプリメントでは効果が期待しにくいことも示されています [11]。
実際に何を心がけるべきか
サプリメントへの過度な期待より、食事からの摂取を優先する考え方が基本です:
| 栄養素 | 推奨摂取量(成人) | 主な食品源 |
|---|---|---|
| カルシウム | 700〜800mg/日 | 牛乳、ヨーグルト、小魚、豆腐、小松菜 |
| ビタミンD | 20〜25μg/日 | 鮭、きのこ類、卵黄 + 日光(1日15〜30分程度) |
ビタミンDは食事からの摂取量が少なく、日照不足が続く冬季・室内生活者では血中濃度が低下しやすいため、その場合にのみサプリメントが有用です。
「飲めば骨折が防げる」という過信を捨てつつ、食事・日光・運動という骨の土台を作る生活習慣を優先することが重要です。
運動という処方箋——高強度レジスタンストレーニングの科学
運動は骨に対して直接的な「機械刺激」を与えます。骨は圧力・衝撃・牽引力を感知すると、骨細胞が骨芽細胞にシグナルを送り、骨形成を促進します。「使われない骨は弱くなる」という原則の逆で、「負荷をかけた骨は強くなる」のです。
37件のRCT(無作為化比較試験)を統合したメタ分析では、レジスタンス運動(筋力トレーニング)が骨密度の変化に対して低〜中程度の有意な効果を示すことが確認されました [12]。
さらに最新のメタ分析(2025年)では、より具体的な「最適処方」が明らかになっています [13]:
- 強度:最大挙上重量(1RM)の70%以上
- 頻度:週3回
- 期間:長期継続(短期では効果が限定的)
この条件を満たしたレジスタンストレーニングが、骨密度改善に最も効果的であることが示されています [13]。
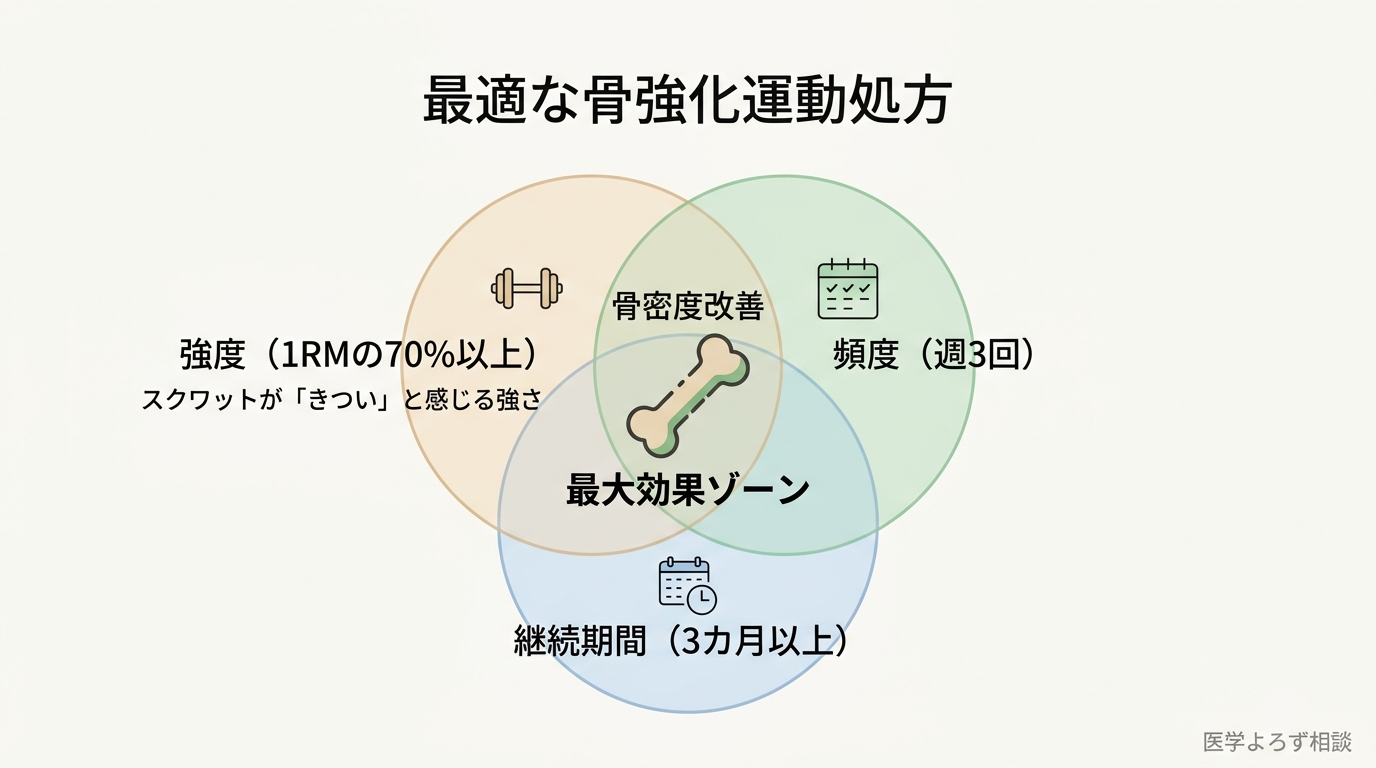
自宅でできる最低限の「骨強化メニュー」
| 種目 | 目安 | ポイント |
|---|---|---|
| スクワット | 8〜12回×3セット | 「きつい」と感じる深さまで下げる |
| 踏み台昇降 | 15分程度 | 10〜15cm台でOK。衝撃が骨に刺激を与える |
| ランジ(片足前踏み込み) | 左右8回×2セット | バランスと荷重刺激を同時に与える |
| かかと落とし | 30回 | つま先立ちからかかとを落とす衝撃が骨刺激 |
特に「かかと落とし(ヒールドロップ)」は、コスト・時間・難易度すべてが低く、腰椎と大腿骨への衝撃刺激を与える手軽な方法として研究でも評価されています。歩行や踏み台昇降も「荷重運動」として骨への機械刺激を与えます。
水泳や自転車は有酸素運動として優れていますが、非荷重運動のため骨密度への効果は限定的です。骨を守るには、重力に抵抗する「荷重運動」を必ず組み込んでください。
オステオサルコペニア——骨と筋肉の「見えない対話」
骨粗鬆症とサルコペニア(加齢性筋肉減少症)は、別々の病態ではありません。オステオサルコペニア(Osteosarcopenia) として合併することで、単独よりも転倒・骨折・死亡リスクが大幅に高まります [14]。
なぜ骨と筋肉はセットで悪化するのか。その答えは「骨筋クロストーク(骨と筋肉の相互信号交換)」というメカニズムにあります [15]。
筋肉→骨への信号(マイオカイン):
- イリシン(Irisin):筋肉が収縮時に放出。骨芽細胞を増殖させ、骨形成を促進
- IGF-1:筋肉から分泌。骨の成長を促す
骨→筋肉への信号(オステオカイン):
- オステオカルシン(Osteocalcin):骨芽細胞が産生。筋肉のエネルギー代謝を改善し、運動パフォーマンスを高める
- FGF23(線維芽細胞増殖因子23):骨細胞から分泌。筋機能に影響
この相互シグナルは、細胞外小胞(エクソソーム)やmicroRNAによっても仲介されており、骨と筋肉が「一つの臓器システム」として機能していることが示されています [15]。
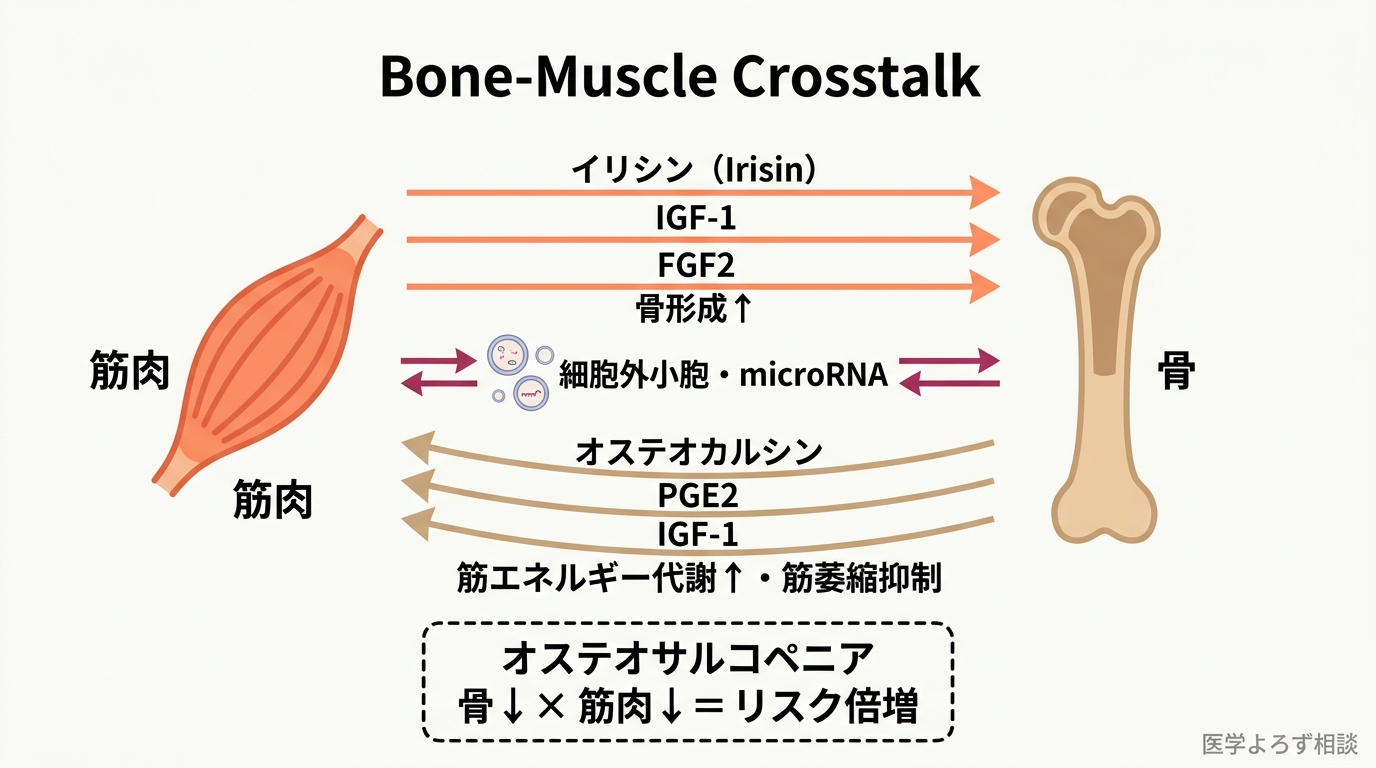
サルコペニアとの相乗リスク
筋力低下→転倒リスク増加→骨折リスク増加という連鎖と、骨からの骨形成シグナル低下→さらなる筋力低下という逆方向の連鎖が両方向で起きます。
これは逆に言えば、筋肉を鍛えることが骨を守り、骨を守ることが筋肉にも良いという好循環も存在することを意味します。
筋肉と老化の科学については、サルコペニア記事(筋肉と長寿——サルコペニア予防の最新エビデンス)でより詳しく解説しています。
科学の現在地——わかっていること、いないこと
確立されたこと
- ロモソズマブ→骨吸収抑制薬の逐次療法が椎体骨折を最も強く抑える(日本GL 2025でも推奨)[17]
- ゾレドロン酸は現時点で骨粗鬆症薬で唯一、死亡率を有意に低下させた実績がある [20]
- デノスマブ10年使用の安全性と有効性は確認されている [6]
- レジスタンストレーニング(≥70% 1RM、週3回)が骨密度改善に最適 [13]
- 骨筋クロストークを通じて筋トレは骨にも好影響を与える [14][15]
まだわかっていないこと・注意が必要なこと
- デノスマブ中止後の管理:いつ、何に切り替えるかの最適プロトコルは現在も研究中
- ロモソズマブの心血管リスク:心疾患既往者への適応は引き続き慎重に考える必要がある [5]
- カルシウム・ビタミンDサプリ:地域在住高齢者への一律投与のエビデンスは弱い [10][11]
- 男性骨粗鬆症:女性ほど大規模なRCTデータが蓄積されておらず、治療指針が男女で異なる部分がある
- TBSの普及:骨の質を評価できる指標だが、測定施設が限られる
実践チェックリスト——40代から始める骨の「貯金」
骨粗鬆症の予防と治療は、年齢ごとに重点が異なります。以下のチェックリストを活用してください。
40代:最大骨量維持期
- レジスタンストレーニング(スクワット・ランジ等)を週2〜3回取り入れる
- カルシウム700〜800mg/日を食事から(牛乳・ヨーグルト・豆腐・小松菜等)
- 週3〜4回、昼間15〜30分程度の日光浴(ビタミンD産生)
- 喫煙している場合は禁煙(喫煙は骨密度を明確に低下させる)
- アルコールは1日2単位以内(過剰飲酒は骨折リスクを上げる)
- 適正体重の維持(低体重は骨密度低下のリスク因子)
50代(特に閉経前後):急速骨量減少の防衛期
- DXA骨密度検査を受ける(腰椎・大腿骨近位部の両方)
- FRAXで10年骨折リスクを計算する
- 閉経症状がある場合、ホルモン補充療法(HRT)について医師に相談する
- 荷重運動の強度を意識的に上げる(「きつい」と感じる強さが必要)
- 転倒リスクの評価(足腰の筋力・バランス・家の中の障害物)
60代以降:骨折予防の最終防衛線
- DXA検査を定期的に(2〜3年ごと)受ける
- Tスコア ≤ −2.5または骨折既往があれば薬物治療を開始・継続
- 骨折したら必ず骨粗鬆症の精査・治療を受ける(連鎖骨折の予防)
- かかと落とし・踏み台昇降などを毎日の習慣にする
- バランス運動(片足立ち・太極拳等)を週2回以上加える
- 必要なサプリメント(カルシウム+ビタミンD)を毎日確実に摂取する
全年代共通:「骨折連鎖」を止める
- 1回骨折したら、次の骨折リスクが3〜5倍になると認識する
- 骨粗鬆症の治療は「入れ歯や血圧薬と同様に継続するもの」
- デノスマブを使用中の場合、自己判断で中止しない(リバウンド骨折のリスク)
- 骨量が回復しても、治療が「不要」になったわけではない
おわりに
「骨の問題は老人の問題」という先入観は、もはや過去のものです。
ピークボーンマスを決定する10代、急速骨量減少が始まる50代の閉経前後、そして骨折連鎖が起きやすい70代以降——骨の問題は生涯を通じた連続したテーマです。
2025年に改訂された日本の骨粗鬆症ガイドラインは、「骨を壊す速度を抑える」から「骨を作る力を取り戻す」への治療パラダイムシフトを明確に打ち出しました [17]。ロモソズマブに代表される骨形成促進薬→骨吸収抑制薬の逐次療法という戦略は、かつては夢だった「失われた骨量の回復」を現実にしています。
しかし薬の力を最大に生かすのも、薬なしで骨を守るのも、土台は同じです。高強度の荷重運動、適切なカルシウムとビタミンDの摂取、禁煙、そして適正体重の維持——これらは40代から始めれば始めるほど、70代の自分に大きな贈り物になります。
骨折が寿命を縮める。その事実を知ったあなたは、今日から「骨の貯金」を始める理由があります。