はじめに:「最近、傷が治りにくくなった」の正体
40代を過ぎたころから、ふとした切り傷が治るのに時間がかかる。風邪をひくと1週間は尾を引く。健康診断のCRP(C反応性タンパク質)がなぜか微妙に高い。
「年のせいだから仕方ない」——本当にそうでしょうか。
2000年、イタリアの免疫学者Claudio Franceschiは、この現象に名前をつけました。Inflammaging(インフラメイジング)。「Inflammation(炎症)」と「Aging(老化)」を掛け合わせた造語です [1]。
興味深いことに、この静かな炎症は、がん、心血管疾患、認知症、糖尿病、フレイル——加齢に伴うほぼすべての疾患の根底に共通して存在しています [1][2]。2023年には、老化の「ホールマーク(特徴的指標)」が12項目に更新され、慢性炎症は正式にその一つとして加えられました [3]。
つまりInflammagingは、単なる「老化のおまけ」ではなく、老化そのものを駆動するエンジンなのです。
この記事では、Inflammagingの分子メカニズムから最新の臨床試験まで、15件のエビデンスに基づいて解説します。「なぜ炎症が消えないのか」を理解し、「今日からできること」を考えていきましょう。
Inflammagingとは何か——3つの火種
通常の炎症は、感染や怪我に対する生体防御反応です。傷が治れば炎症は収まります。ところがInflammagingは違います。明確な感染源がないのに、低いレベルの炎症がずっと燻り続ける。Franceschiはこれを「慢性・低グレード・無菌性炎症」と定義しました [1]。
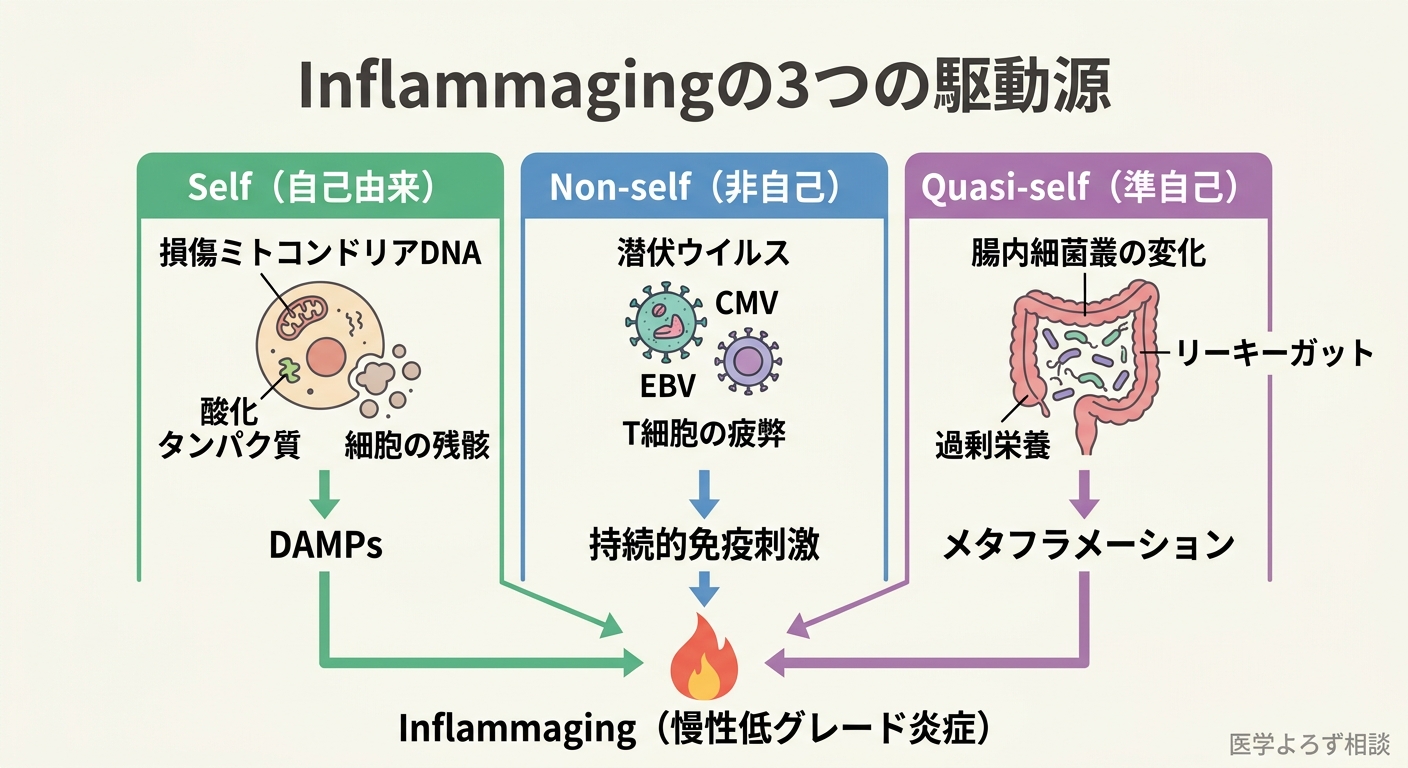
では、火種はどこから来るのでしょうか。Franceschiらの統合モデルによれば、大きく3つのカテゴリに分類されます [2]。
1. Self(自己由来)——壊れた細胞の残骸
加齢に伴い、損傷したミトコンドリアDNA、酸化したタンパク質、細胞の死骸といった「分子ゴミ」が蓄積します。若い頃は免疫系がこれらを素早く処理していましたが、加齢とともにクリアランス能力が低下。これらが「危険シグナル(DAMPs: Damage-Associated Molecular Patterns)」として自然免疫を持続的に活性化します。
2. Non-self(非自己由来)——過去の感染の記憶
サイトメガロウイルス(CMV)やエプスタイン・バーウイルス(EBV)など、体内に潜伏し続けるウイルスが免疫系を慢性的に刺激します。長年にわたる「免疫の記憶」の蓄積が、T細胞の疲弊と炎症性サイトカインの持続的な産生につながります [4]。
3. Quasi-self(準自己)——腸内細菌と栄養素
最も注目されているのがこのカテゴリです。腸内細菌叢は「自己」でも「非自己」でもない存在です。加齢に伴う腸内細菌叢の変化(ディスバイオシス)は、腸管バリアの透過性を高め、細菌由来の炎症性物質(リポ多糖: LPSなど)が血中に漏出する「リーキーガット」状態を引き起こします [2]。さらに、過剰な栄養摂取そのものが炎症を誘発する「メタフラメーション(代謝性炎症)」も、Inflammagingと同じメカニズムで進行します。
細胞老化とSASP——「ゾンビ細胞」が火を焚き続ける
Inflammagingの分子メカニズムで最も解明が進んでいるのが、細胞老化(cellular senescence)とSASP(Senescence-Associated Secretory Phenotype: 老化関連分泌表現型)の関係です。
細胞老化とは
細胞老化とは、DNA損傷やテロメア短縮などのストレスに応じて、細胞が永久に増殖を停止する現象です。これは本来、がん化を防ぐための安全装置として機能しています [7]。
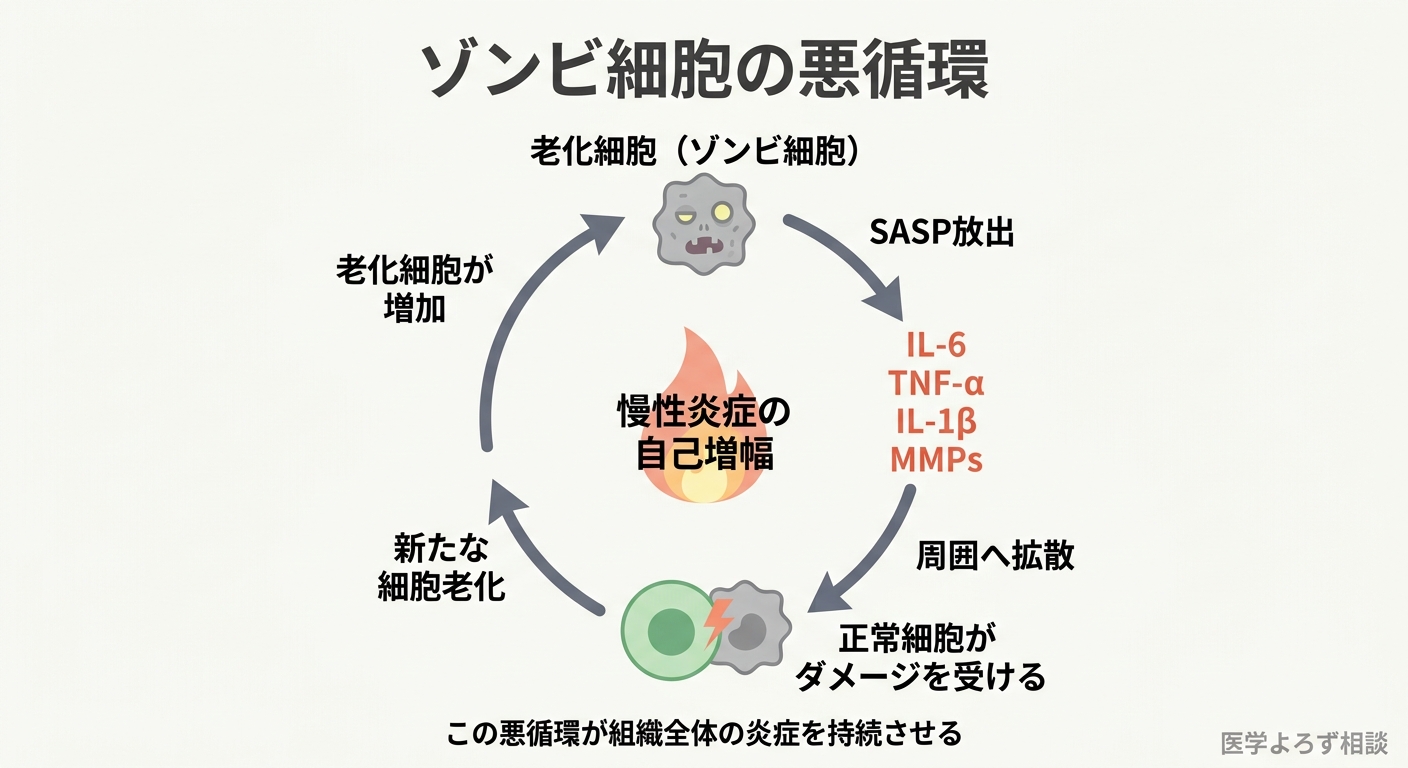
しかし、問題はここからです。老化した細胞は死なずに組織に居座り続けます。研究者たちはこれを「ゾンビ細胞」と呼びます。そしてこのゾンビ細胞は、ただ居座るだけでなく、SASPと呼ばれる炎症性の分泌物を周囲にまき散らします [6][7]。
SASPの正体
2010年、Judith Campisiらの研究グループが、SASPの全貌を初めて体系的に明らかにしました [7]。老化細胞が分泌するSASPには以下が含まれます:
- 炎症性サイトカイン: IL-6、IL-1β、TNF-α——炎症を増幅する分子
- ケモカイン: 免疫細胞を呼び寄せるシグナル
- マトリックスメタロプロテアーゼ(MMPs): 組織の構造を分解する酵素
- 成長因子: 周囲の細胞の挙動を変える
最新のレビュー(Wang et al., 2024)によれば、SASPの組成は一様ではなく、老化の原因や細胞の種類、時間経過によって動的に変化します [6]。つまりSASPは「一つの現象」ではなく、極めて多様で文脈依存的な現象なのです。
悪循環の構造
ここで理解すべき核心は、SASPが悪循環を生むということです。
老化細胞が放出するSASP因子(特にIL-6やTNF-α)は、周囲の正常な細胞にもダメージを与え、新たな細胞老化を誘導します。新たに老化した細胞がさらにSASPを放出する——こうして炎症は自己増幅していきます [3][5]。
2023年のBaechleらの総説は、この悪循環が老化の12のホールマークすべてと双方向的に連関していることを示しました [3]。慢性炎症はテロメア短縮を加速し、ミトコンドリア機能障害を悪化させ、エピジェネティック変化を促進する。そしてこれらの変化がさらに炎症を増幅する。Inflammagingは老化の「結果」であると同時に「原因」でもあるのです。
数字で見るInflammaging——CRPとIL-6が語ること
「慢性炎症」と言われても、目に見えないだけに実感が湧きにくいかもしれません。しかし、血液検査でその痕跡を捉えることができます。
CRPとIL-6——二大バイオマーカー
Inflammagingの研究で最も頻繁に測定されるのが、CRP(C反応性タンパク質)とIL-6(インターロイキン-6)です。
CRPは肝臓で産生される急性期タンパク質で、炎症があると血中濃度が上昇します。一般的な血液検査で測定できるため、健康診断の結果でも確認しやすい指標です。IL-6は炎症性サイトカインの一つで、SASPの主要成分でもあり、Inflammagingの中心的なメディエーターです。
CRPとhs-CRPの違い 海外の研究では「hs-CRP(高感度CRP)」がよく登場します。hs-CRPはより微弱な慢性炎症を検出できる検査法で、心血管リスク評価などに使われます。ただし、日本の一般的な健康診断や血液検査で測定されるのは通常のCRPです。本記事では日本の検査実態に合わせ、以降「CRP」で統一します。なお、引用元の研究がhs-CRPを使用している場合は原著の表記に従っています。
死亡リスクとの関連
2025年に発表された最新のメタアナリシス(Chen et al., 22のコホート研究を統合)は、これらのバイオマーカーとハードアウトカム(死亡率)の関連を明確に示しました [13]:
- CRP上昇: 全死亡リスクが1.54倍(P=0.001)
- IL-6上昇: 全死亡リスクが1.47倍(P=0.001)
- CRP上昇: うつ病のオッズが1.48倍(P<0.001)
つまり、「CRPがちょっと高い」は決して「気のせい」ではなく、統計的に有意な健康リスクの指標なのです。

介入で動かせるか
重要な問いは、「これらのバイオマーカーは介入で下げられるのか」です。Byrneらの2023年のメタアナリシス(フレイル・サルコペニア高齢者を対象とした16研究)は、運動・栄養介入によって [12]:
- CRP: SMD = -0.28(P = 0.05)——有意に改善
- IL-6: SMD = -0.28(P = 0.05)——有意に改善
- TNF-α: SMD = -0.12(P = 0.48)——有意差なし
CRPとIL-6は介入に反応する「動かせるマーカー」であることが示されています。
百寿者の教え——炎症と共存する術
興味深い事実があります。百寿者もInflammagingを経験しています。しかし、彼らは加齢関連疾患を回避し、あるいは大幅に遅らせています。なぜでしょうか。
Santoroらの2021年の総説は、百寿者が「炎症-抗炎症バランス」を維持する独自のメカニズムを持っていることを示しました [4]:
- 抗炎症性サイトカイン(IL-10など)の産生が高い
- 免疫系のリモデリング(適応的変化)が成功している
- 腸内細菌叢の多様性が保たれている
つまり、老化そのものを止めることはできなくても、炎症と抗炎症のバランスを最適化することで、健康長寿は実現可能だということです。免疫老化は必ずしも「衰退」ではなく、「適応的リモデリング」の側面を持っています [4]。
今日からできるInflammaging対策——エビデンスに基づく4つの戦略
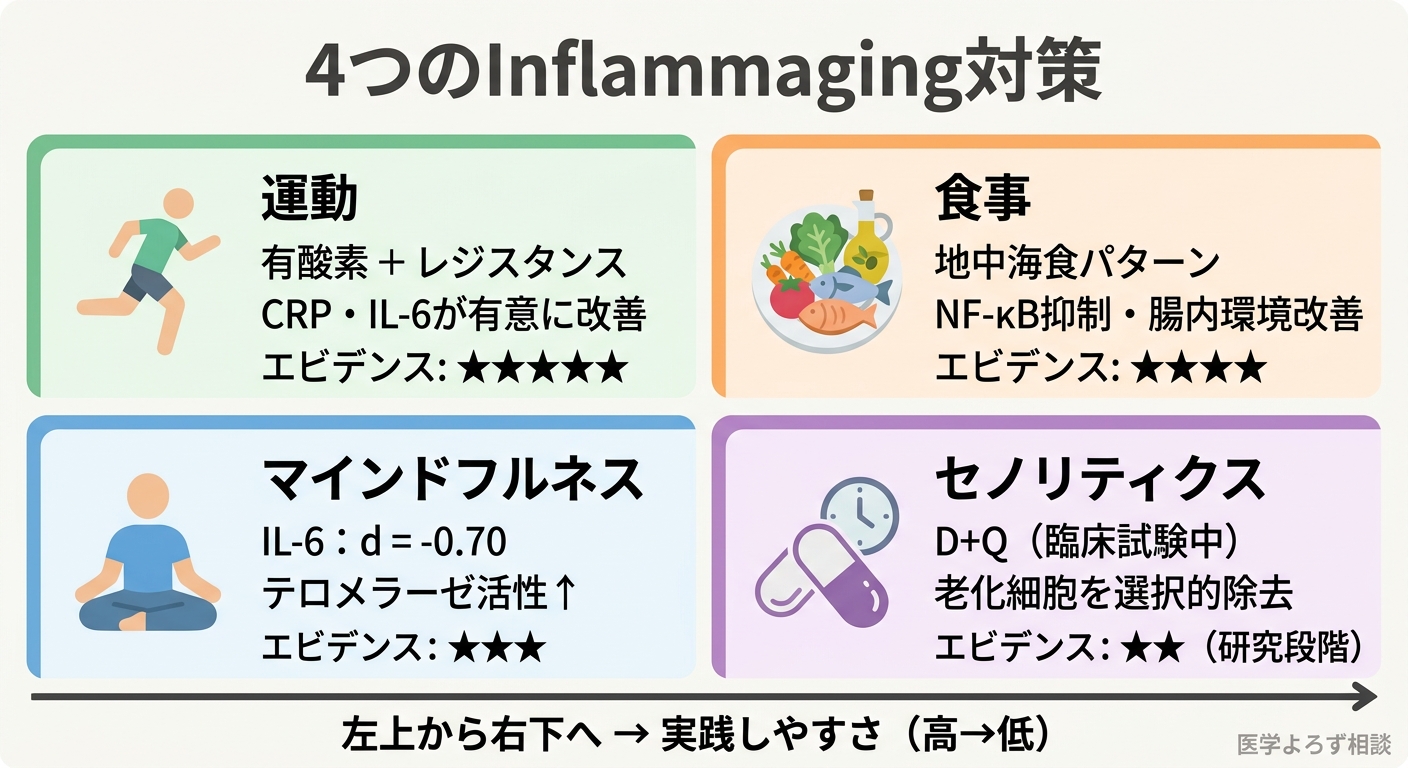
1. 運動——最強の抗炎症薬
運動がInflammagingに効くメカニズムは、Pedersenの「マイオカイン」理論で説明されます [8]。筋肉を収縮させると、IL-6がTNF-α非依存的に放出されます。「IL-6は炎症性サイトカインでは?」と思われるかもしれませんが、筋肉由来のIL-6は異なる経路で作用します。
筋肉由来IL-6は:
- 抗炎症性サイトカイン(IL-1ra、IL-10)の産生を誘導する
- 炎症性TNF-αの産生を抑制する
- 脂肪分解と脂肪酸酸化を促進する
2022年のXingらのメタアナリシス(14 RCTs、中高年T2DM患者)は、運動介入がIL-6(P=0.002)、CRP(P=0.01)、TNF-α(P=0.003)をすべて有意に低減させることを示しました [9]。有酸素運動+レジスタンストレーニングの併用が最も効果的で、長期的な継続がより大きな効果をもたらします。
さらに2025年のNejati Bervanlouらのメタアナリシスでは、運動+タンパク質補給の併用がCRP・IL-6・TNF-αのすべてにおいて運動単独よりも効果的であることが示されています [10]。
2. 食事——地中海食とNrf2活性化
地中海食(野菜、果物、全粒穀物、オリーブオイル、魚を中心とした食事パターン)がInflammagingを軽減するメカニズムは、複数の経路で説明されます [18]:
- NF-κB経路の抑制: 炎症のマスタースイッチであるNF-κBの活性化を抑える
- 腸内細菌叢の恒常性維持: 食物繊維が善玉菌を増やし、腸管バリア機能を維持
- エピジェネティック調節: ポリフェノール由来のmicroRNAが炎症遺伝子の発現を制御
特に注目すべきはNrf2(エヌアールエフツー)経路です [19]。Nrf2は「抗酸化・抗炎症の司令塔」とも呼べる転写因子で、200以上の防御遺伝子を活性化します。しかし、Nrf2の活性は加齢とともに低下します。
Nrf2を活性化する食品成分として、以下が研究されています [19]:
| 食品成分 | 含まれる食品 |
|---|---|
| スルフォラファン | ブロッコリー、ブロッコリースプラウト |
| クルクミン | ターメリック(ウコン) |
| レスベラトロール | 赤ワイン、ブドウの皮 |
| EGCG | 緑茶 |
3. マインドフルネス——心と免疫の接点
2025年のHuangらのメタアナリシス(89研究)は、マインドフルネス介入のInflammagingへの効果を包括的に評価した初の研究です [11]:
- TNF-α: d = -0.40(中程度の効果)
- IL-6: d = -0.70(大きな効果)
- CRP: d = -0.48(中程度の効果)
- テロメア長: d = 0.43(増加)
- テロメラーゼ活性: d = 0.84(大きな増加)
IL-6への効果量(d = -0.70)は、運動介入と同等以上です。マインドフルネスがストレスホルモン(コルチゾール)を低減し、視床下部-下垂体-副腎(HPA)軸を介して全身の炎症応答を制御するメカニズムが想定されています。
4. セノリティクス——「ゾンビ細胞除去薬」の最前線
セノリティクスとは、老化細胞を選択的に除去する薬剤の総称です。最も研究が進んでいるのがダサチニブ+ケルセチン(D+Q)の併用です。ダサチニブは白血病治療薬、ケルセチンはタマネギや果物に含まれるフラボノイドです。
⚠️ 日本での承認状況: ダサチニブ(スプリセル)は慢性骨髄性白血病の治療薬として日本で承認済みですが、抗老化目的での使用は適応外であり保険適用されません。ケルセチンはサプリメントとして市販されていますが、医薬品としてではありません。2026年4月現在、セノリティクスの抗老化目的での臨床使用は、日本を含む世界のどの国でも承認されていません。以下は臨床試験の結果報告であり、自己判断での使用を推奨するものではありません。
現在までに発表された主要な臨床試験の結果を紹介します:
骨代謝(Farr et al., 2024 — Phase 2 RCT)[14]: 閉経後女性60名を対象とした試験で、全体としては主要エンドポイント未達。しかし、老化細胞負荷の高いサブグループ(T細胞p16高発現者)では:
- 骨形成マーカーP1NP: +34%増加(P=0.035)
- 骨吸収マーカーCTx: -11%減少(P=0.049)
- 橈骨骨密度: +2.7%増加(P=0.004)
この結果は、セノリティクスの効果が老化細胞の蓄積量に依存することを示唆しています。全員に効くのではなく、「ゾンビ細胞が多い人」により効く、という精密医療の発想です。2025年には、T細胞p16バリアント5と血漿SASPパネルが、治療応答を予測するバイオマーカーとして確立されました [17]。
アルツハイマー病(Gonzales et al., 2023 — Phase 1)[15]: 軽度AD患者5名の試験で、ダサチニブが80%の参加者の髄液中に検出されました(血液脳関門を通過)。安全性・忍容性は良好で、老化関連サイトカインの低下傾向が確認されています。
特発性肺線維症(Nambiar et al., 2023 — Phase 1 RCT)[16]: IPF患者12名の試験で、全参加者がD+Qの3週間投与を完遂(108/108用量)。重篤有害事象は報告されませんでした。
科学の現在地:わかっていること、いないこと
確立された知見:
- Inflammagingは加齢に伴う慢性・低グレード・無菌性炎症であり、ほぼすべての加齢関連疾患の共通基盤である [1][2]
- CRPとIL-6の上昇は全死亡リスクの有意な予測因子である [13]
- 運動介入はCRP・IL-6・TNF-αを有意に改善する(メタアナリシスで確認)[9][10]
- 細胞老化とSASPがInflammagingの主要な分子メカニズムである [6][7]
- 百寿者はInflammagingを経験しつつも、抗炎症応答の最適化により健康を維持している [4]
未解明点・現在の限界:
- Inflammagingの「正常範囲」と「病的範囲」の閾値が定まっていない
- CRP・IL-6以外の、より特異度の高いバイオマーカーパネルが必要
- セノリティクスの長期安全性データが不足している(最長試験で20週間)
- 腸内細菌叢→Inflammagingの因果関係は示唆段階であり、介入試験での確認が必要
- 個人差(遺伝背景・性差・人種差)の影響が十分に解明されていない
- マインドフルネスの効果機序は仮説段階であり、大規模RCTでの検証が必要 [11]
実践チェックリスト:今日からできるアンチInflammaging
| 領域 | 具体的アクション | エビデンスレベル |
|---|---|---|
| 運動 | 有酸素+レジスタンスを週3回以上、各30分 | MA of RCTs [9][10] |
| タンパク質 | 体重1kgあたり1.2〜1.5gのタンパク質摂取 | MA of RCTs [10] |
| 食事パターン | 地中海食に近いパターン(野菜・果物・魚・オリーブオイル) | Review [18] |
| Nrf2食品 | ブロッコリー(スルフォラファン)、緑茶を習慣的に | Review [19] |
| ストレス管理 | マインドフルネス瞑想を1日10〜20分 | MA [11] |
| 睡眠 | 7〜8時間の質の高い睡眠 | 複数のレビューで推奨 |
| 健診 | 健康診断のCRP値を意識してみましょう | MA [13] |

おわりに:「炎」との付き合い方
Inflammagingの研究を知るたびに、私は一つのことを考えます。
炎症は本来、私たちの体を守る「火」です。感染と闘い、傷を治し、がんを排除する。しかし加齢とともに、その火のコントロールが効かなくなる。消えるべき時に消えない。
百寿者が教えてくれるのは、「火を消す」のではなく「火と上手に付き合う」ということです。適度な運動、バランスの良い食事、ストレスとの健全な距離感——これらは特別なサプリメントでも最先端の薬剤でもありません。
セノリティクスのような新しい治療法は確かに革命的な可能性を秘めています。しかし、まだ臨床試験の段階であり、長期的な安全性は十分に検証されていません。一方で、運動と食事と心のケアは、複数のメタアナリシスで効果が確認された、今すぐ実践できる「処方箋」です。
次の健康診断で、CRPの値を意識してみてください。それがあなたのInflammagingの「今」を知る手がかりになります。そして、運動・食事・ストレス管理といった日々の生活習慣こそが、炎症をコントロールする最も確実な方法です。
本日のまとめ
- Inflammagingの本質: 加齢に伴い「消えない炎症」が全身で燻り、がん・心疾患・認知症など加齢関連疾患の共通基盤となる
- 最新のエビデンス: CRP上昇で全死亡リスク1.54倍、運動介入でCRP・IL-6が有意に改善(メタアナリシス)
- 今日からできること: 有酸素+レジスタンス運動、地中海食、ブロッコリー・緑茶、マインドフルネス、健康診断のCRP値を意識
関連記事:
