はじめに:「老化」は運命か、それとも治療可能な病気か
2023年、一つの論文が科学界を揺るがせました。
生物学の最高峰ジャーナルCellに掲載された「Hallmarks of Aging(老化のホールマーク)」の改訂版 [1]。著者のLopez-Otinらは、老化を12の生物学的プロセスに分解し、その一つひとつが「治療標的になりうる」ことを示しました。引用数は30万件を超え、老化研究のバイブルとなっています。
この論文が投げかけたのは、シンプルだが革命的な問いです。
「老化」は避けられない宿命なのか——それとも、がんや糖尿病と同じように「治療できる病気」なのか?
2024年、WHOはICD-11(国際疾病分類)に拡張コード「XT9T: Ageing-related」を正式に追加しました [12]。老化を「生物学的原因」として疾患に紐づけることが、国際的な枠組みの中で初めて可能になったのです。
そして今、この問いに最も直接的に挑んでいるのがセノリティクス——「老化した細胞を選択的に除去する薬」です。
2019年に世界で初めてヒトに投与されたセノリティクスは [2]、わずか数年で認知症やフレイル(虚弱)の臨床試験にまで到達しました [3]。その裏では、ラパマイシン、メトホルミン、NMNといった「長寿薬候補」の臨床試験も進行しています。
この記事では、セノリティクスを中心に、長寿科学(ジェロサイエンス)の最前線を、エビデンスに基づいて丁寧に解き明かしていきます。
老化の「12のホールマーク」——なぜ私たちは老いるのか
老化を理解するには、まず「何が起きているのか」を整理する必要があります。
Lopez-Otinらが提唱した12のホールマーク [1] は、老化のメカニズムを「原因」「応答」「結果」の3層に分類しています。
原因(Primary hallmarks):
- ゲノム不安定性——DNAの傷が蓄積する
- テロメア短縮——染色体の「キャップ」がすり減る
- エピジェネティック変化——遺伝子の「使い方」が狂う
- プロテオスタシス喪失——タンパク質の品質管理が破綻する
応答(Antagonistic hallmarks):
- 栄養感知異常——「成長モード」から抜け出せなくなる
- ミトコンドリア機能不全——細胞のエネルギー工場が老朽化する
- 細胞老化——「ゾンビ細胞」が居座る
結果(Integrative hallmarks):
- 幹細胞疲弊——再生能力が枯渇する
- 細胞間コミュニケーション変化——臓器間の連携が乱れる
- 慢性炎症——「静かな火事」が全身で燻る
- マクロオートファジー障害——細胞の「掃除機能」が低下する
- ディスバイオシス——腸内環境が崩壊する
これらは独立した現象ではなく、互いに影響し合いながら老化を加速させます。中でも、セノリティクスの標的である「細胞老化」は、慢性炎症や幹細胞疲弊の直接的な原因となるため、老化カスケードの「ハブ」として注目されています。
「ゾンビ細胞」の正体——細胞老化とSASPのメカニズム
細胞老化とは何か
細胞老化(cellular senescence)とは、細胞が分裂を永久に停止しながらも死なずに居座り続ける状態のことです。
若い頃、細胞老化は「がん抑制メカニズム」として働きます。DNAが損傷した細胞が増殖を止めることで、がん化を防いでいるのです。しかし加齢とともに、この本来は防御的なメカニズムが暴走し始めます。
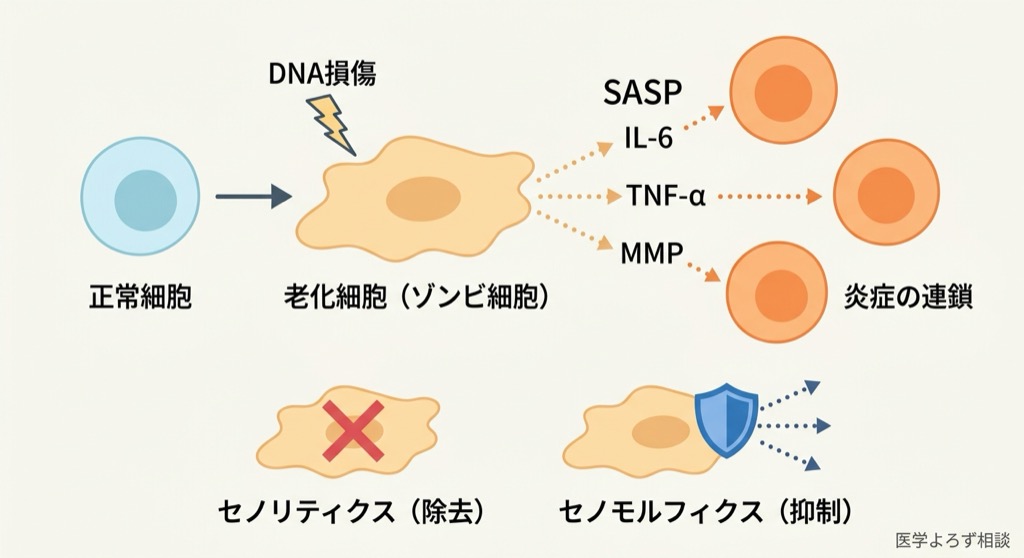
老化細胞は死なない代わりに、周囲に「炎症性の化学物質」を撒き散らし始めます。これがSASP(Senescence-Associated Secretory Phenotype: 老化関連分泌表現型)です [14]。
SASPという「静かな炎症爆弾」
SASPの構成要素には以下が含まれます:
- 炎症性サイトカイン: IL-6、IL-8、TNF-α
- 成長因子: TGF-β、VEGF
- プロテアーゼ: MMP(マトリックスメタロプロテアーゼ)
- ケモカイン: MCP-1、CXCL1
これらは周囲の正常な細胞にも老化シグナルを伝播させ(paracrine senescence)、さらなる老化細胞を生み出します。まるで「ゾンビに噛まれると次のゾンビになる」ように、老化が連鎖的に広がっていくのです。
SASPによる慢性炎症は、動脈硬化、2型糖尿病、アルツハイマー病、変形性関節症、サルコペニア(筋肉減少症)など、ほぼすべての加齢関連疾患に関与することが明らかになっています [14][15]。
セノリティクスとセノモルフィクス——2つの戦略
この「ゾンビ細胞」問題に対して、現在2つの治療戦略が研究されています [14][15]:
| 戦略 | アプローチ | 代表的な薬剤 | 利点 | 課題 |
|---|---|---|---|---|
| セノリティクス | 老化細胞を選択的に殺す | ダサチニブ+ケルセチン (D+Q)、フィセチン | 根本的に老化細胞を除去 | 間欠投与が必要、正常細胞への影響 |
| セノモルフィクス | SASPを抑制する(細胞は殺さない) | ラパマイシン、メトホルミン | 継続投与が可能、副作用が穏やか | 老化細胞自体は残る |
セノリティクス臨床試験——ヒトで何がわかったか
世界初のヒト試験: D+Q(2019年)
セノリティクスの歴史は、2019年のメイヨー・クリニック(米国)から始まりました。
James Kirklandらは、ダサチニブ(白血病治療薬)とケルセチン(植物由来フラボノイド)の2剤併用(D+Q)を、糖尿病性腎臓病の患者9名に3日間だけ投与しました [2]。
結果は画期的でした:
- 脂肪組織中の老化細胞マーカー(p16INK4A、p21CIP1、SA-β-gal)が有意に減少
- 血中のSASP因子も低下
- 重篤な有害事象なし
たった3日間の投与で、ヒトの体から老化細胞が減った——これは「老化は治療できるかもしれない」という仮説を、初めてヒトのデータで支持した瞬間でした。
ただし、非盲検・9名という極めて小規模な試験であり、プラセボ効果やバイアスの可能性は排除できません。これはあくまで「概念実証(proof of concept)」であり、因果関係の証明ではない点を強調しておきます。
STAMINA試験: セノリティクス×認知機能(2025年)
2025年、さらに踏み込んだ結果が報告されました。
STAMINA(Senolytics To Alleviate Mobility Issues and Neurological Impairments in Aging)試験 [3] は、軽度認知障害(MCI)と歩行速度低下を併せ持つ65歳以上の高齢者12名を対象に、D+Qを12週間投与しました(2日間投与→12日間休薬を6サイクル)。
注目すべき結果:
- 安全性: 重篤な有害事象は投与に関連するものなし
- 認知機能: ベースラインのMoCA(モントリオール認知評価)スコアが低い群で、2.0点の有意な改善(95% CI: 0.1-4.0)
- 炎症マーカー: TNF-αの低下が認知機能改善と相関
MoCA 2点の改善は、一般的なMCI患者の年間低下量(約0.5〜1点)を考えると、臨床的に意味のある変化です。しかし、単群・非盲検・12名であり、プラセボ対照RCTでの検証が不可欠です。
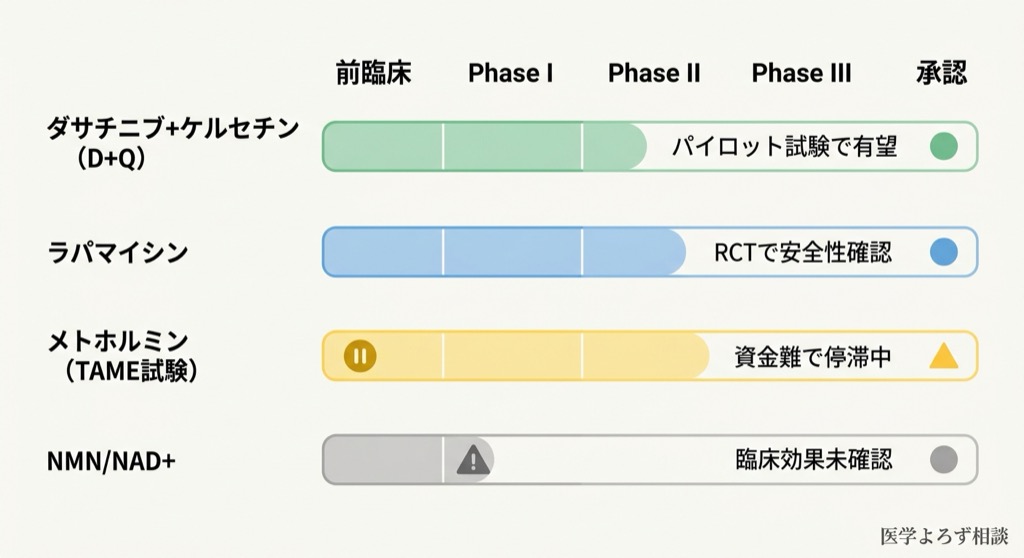
現在の位置づけ: 「セノリティクスが認知機能を改善しうる」という初めてのヒトでの示唆。大規模RCTへの道を開いたパイロット試験として重要ですが、「効く」と断定するのは時期尚早です。
セノリティクスだけじゃない——長寿薬候補たちの現在地
ラパマイシン: PEARL試験の衝撃(RCT、エビデンスレベル II)
ラパマイシンは臓器移植の免疫抑制薬として臨床使用されている薬ですが、mTOR(mechanistic target of rapamycin)経路を阻害することで、動物実験では一貫して寿命延長効果が示されてきました。
2025年に報告されたPEARL試験 [4] は、ラパマイシンのアンチエイジング効果を検証した最大規模のヒトRCTです。
- 対象: 健常高齢者114名
- デザイン: 二重盲検・プラセボ対照・3群(プラセボ / 5mg / 10mg 週1回)
- 期間: 48週間
主な結果:
| アウトカム | 結果 |
|---|---|
| 安全性 | 低用量間欠投与は48週間忍容可能 |
| 除脂肪体重(女性・10mg群) | 約5%増加(有意) |
| 疼痛スコア(女性・10mg群) | 有意に改善 |
| 骨塩量(男性・高用量群) | 改善傾向 |
ポイント: これは「ラパマイシンが老化を止める」ことを証明した試験ではありません。しかし、mTOR阻害が筋肉量や骨密度という加齢で確実に低下する指標をRCTレベルで改善しうることを示した初のデータとして注目に値します。
注意点として、この試験はクラウドファンディングで資金調達された非薬事試験であり、規制上の位置づけは限定的です。
メトホルミン: TAME試験の挑戦と挫折
メトホルミンは2型糖尿病の第一選択薬ですが、大規模観察研究で糖尿病患者の死亡率が非糖尿病者よりも低いという驚くべきデータが報告され、「長寿薬」として注目されました。
Nir Barzilaiらが設計したTAME(Targeting Aging with Metformin)試験 [5] は、3,000名の高齢者を対象に「メトホルミンが加齢関連疾患全般の発症を遅延させるか」を検証する野心的なRCTです。FDAに「老化」を適応症として認めさせる先例を作ることが、科学的目標と並ぶ重要な目的でした。
しかし2026年4月時点で、推定4,500万〜7,000万ドルの必要資金に対し、NIAからの500万ドルしか確保できていません [6]。ARPA-Hが部分的に関与する動きはあるものの、試験開始時期は未定です。
さらに、2025年にAgeing Research Reviewsに掲載されたレビューでは、メトホルミンのアンチエイジング効果自体に不確実性が増大していることが指摘されています [6]。
NMN/NAD+サプリメント: 期待と現実のギャップ
NAD+(ニコチンアミドアデニンジヌクレオチド)は細胞のエネルギー代謝に不可欠な補酵素で、加齢とともに減少します。NMN(ニコチンアミドモノヌクレオチド)やNR(ニコチンアミドリボシド)は、NAD+の前駆体としてサプリメント市場で爆発的に普及しています。
しかし、最も信頼性の高いエビデンスであるシステマティックレビュー/メタアナリシス(SR/MA)は、厳しい現実を突きつけています [7]:
- 12研究、513名のSR/MA: NMN補充は血中NAD+レベルを有意に上昇させた
- しかし、糖脂質代謝、筋肉量、認知機能など臨床的に重要なアウトカムでは有意差なし
- 60歳以上を対象とした別のSR/MAでも、筋肉量・機能への効果は否定的
つまり、「NAD+は上がるが、体は若返らない」というのが現時点でのエビデンスです。
「生物学的年齢」を測る——エピジェネティック時計の革命
なぜバイオマーカーが必要なのか
セノリティクスが「老化を遅らせる」かどうかを検証するには、「老化の速度」を測る方法が必要です。しかし、暦年齢(何歳か)では不十分です。同じ60歳でも、「生物学的に50歳」の人と「生物学的に70歳」の人がいるからです。
ここで登場するのがエピジェネティック時計です。
エピジェネティック時計とは
DNAのメチル化パターン(エピゲノム)は加齢とともに予測可能な変化を示します。この変化を数学モデルで解析し、「生物学的年齢」を推定するのがエピジェネティック時計です。
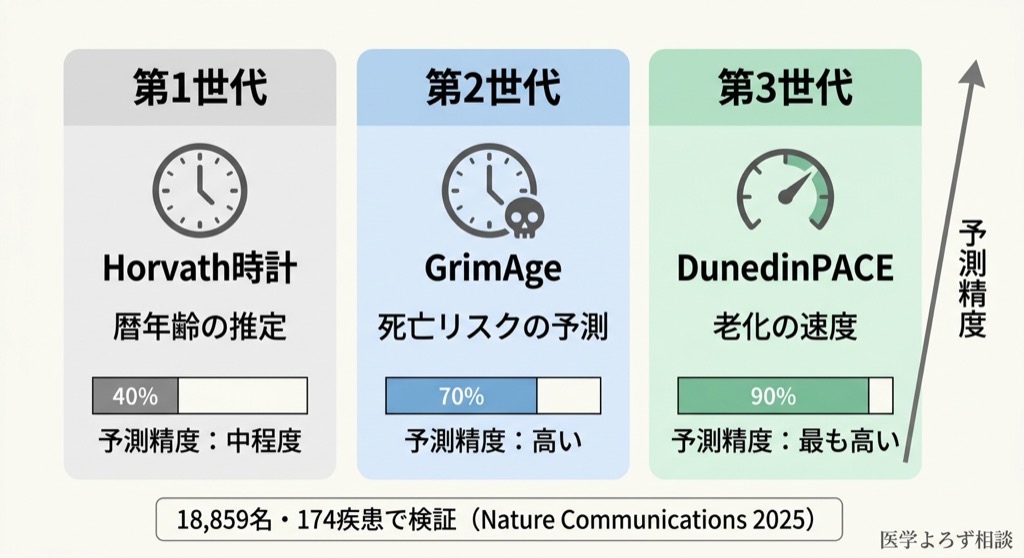
2025年、18,859名・10年追跡の大規模コホート研究 [8] が、14種類のエピジェネティック時計を網羅的に比較しました。その結果は明瞭でした:
第2・第3世代時計(GrimAge、DunedinPACE)は、第1世代(Horvath)より疾患予測能が有意に優れる。
特に注目すべきは、2つの時計が「異なるもの」を測っている点です:
| 時計 | 測定対象 | 特徴 |
|---|---|---|
| GrimAge | 「死亡リスク」 | 炎症・造血系老化と相関。「あなたはあとどれくらい生きられるか」の指標 |
| DunedinPACE | 「老化の速度」 | 機能的負荷の蓄積と相関。「あなたは今どれくらい速く老いているか」の指標 |
メタアナリシス [9] でも、エピジェネティック年齢加速は死亡率・心血管疾患・がん・認知症と有意に関連することが確認されています。
将来的には、セノリティクスやラパマイシンの効果を「生物学的年齢がどれだけ若返ったか」で評価する時代が来る可能性があります。ただし現時点では、これらの時計が「介入の効果判定」に使えるかどうかの検証はまだ途上です。
日本発の研究が切り拓く新地平
長寿科学は欧米主導のイメージがありますが、日本からも世界的に注目される研究が次々と発表されています。
順天堂大学: SGLT2阻害薬のセノリティクス作用(2024年)
2024年、順天堂大学の南野徹教授らのグループが、Nature Agingに衝撃的な論文を発表しました [10]。
糖尿病治療薬として広く使われているSGLT2阻害薬(カナグリフロジン)に、セノリティクス作用があることを発見したのです。
そのメカニズムは巧妙です:
- カナグリフロジンがAMPK(エネルギーセンサー)を活性化
- AMPKがPD-L1(免疫チェックポイント分子)を抑制
- PD-L1が下がることで免疫細胞が活性化
- 活性化した免疫が老化細胞を攻撃・除去
この「免疫を介した老化細胞除去」は、D+Qのような「直接的な細胞死誘導」とは異なる、新しいセノリティクス戦略です。
特筆すべきは、SGLT2阻害薬がすでに数百万人の糖尿病患者に安全に使用されている薬であるという点です。全く新しい薬を開発するのではなく、既存の薬の「隠れた力」を活用する——いわゆるドラッグ・リポジショニングは、セノリティクス実用化の最短経路かもしれません。
ただし、この研究はマウスモデルでの結果であり、ヒトでのセノリティクス効果はまだ検証されていません。
大阪大学: AP2A1——老化と若返りのスイッチ(2025年)
2025年、大阪大学の研究グループは、細胞老化の新しいマーカーかつ治療標的としてAP2A1を発見しました [11]。
AP2A1は老化した細胞のストレスファイバー(細胞骨格)上に発現が増加するタンパク質です。興味深いのは:
- AP2A1をノックダウン(抑制)すると、老化した細胞が「若返る」
- AP2A1を過剰発現させると、若い細胞が「老化する」
つまりAP2A1は、細胞の「老化/若返り」を切り替えるスイッチのような役割を持つのです。
これは、セノリティクス(老化細胞を「殺す」)とも、セノモルフィクス(SASPを「抑える」)とも異なる、第3の戦略——セノリバース(老化細胞を「若返らせる」)——の可能性を示唆しています。
「老化は病気か」——WHOと国際コンセンサスの最新動向
ICD-11: XT9Tコードの意味
2024年、WHOはICD-11に拡張コード「XT9T: Ageing-related」を正式に採用しました [12]。
これは、老化関連の病態に対して「生物学的老化」を原因因子として紐づけることを可能にするコードです。一見地味な分類変更ですが、その影響は絶大です:
- 臨床試験: 「老化」を適応症としたセノリティクスの承認申請が理論上可能に
- 保険制度: 老化関連治療の医療費償還の法的根拠になりうる
- 研究資金: 「老化治療」への公的研究資金配分が正当化される
当初、WHOはこのコードを「pathological(病的)」と記述していましたが、「老化は自然なプロセスだ」という批判を受け、「biological(生物学的)」に修正されました。この経緯自体が、老化を「病気」と定義することの難しさを物語っています。
国際コンセンサス: 老化関連疾患の定義
2024年2月、カーディフで開催されたICCARPの国際会議 [13] に150名の専門家が集まり、「老化関連疾患」の定義基準を策定しました:
- 加齢に伴い発症または進行する
- 機能低下に関連または寄与する
- ヒトでのエビデンスが存在する
各基準は70%以上のコンセンサスで承認されています。これにより、セノリティクスなどの臨床試験のエンドポイント設計や、規制当局との対話に共通言語が生まれました。
科学の現在地: わかっていること、いないこと
確立された知見
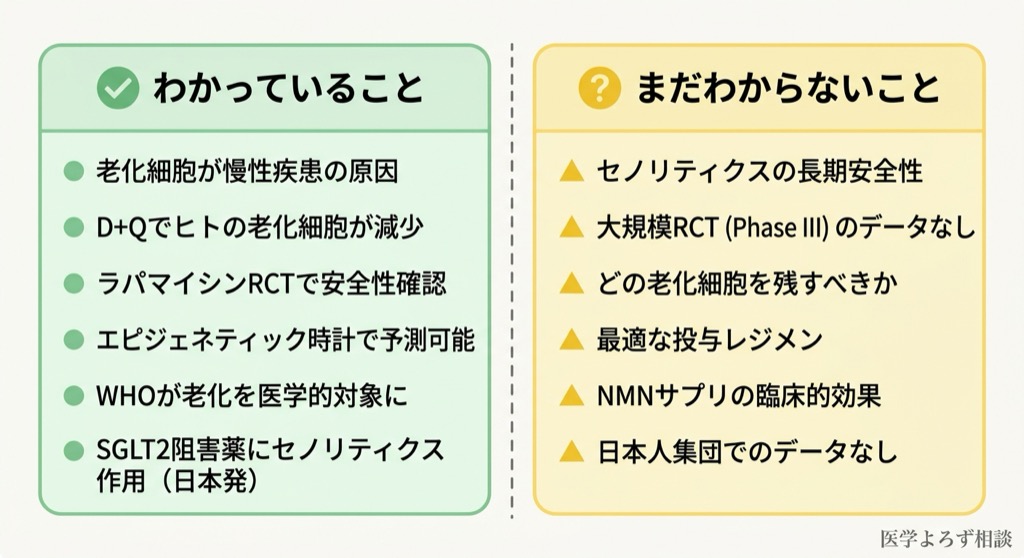
- 細胞老化は加齢関連疾患の主要な駆動因子である(動物モデルで繰り返し実証)
- セノリティクス(D+Q)はヒトで老化細胞を減少させうる(小規模パイロット試験 [2][3])
- ラパマイシンの低用量間欠投与はヒトで安全であり、筋骨格系指標を改善しうる(RCT [4])
- NMNは血中NAD+を上昇させるが、臨床的に重要なアウトカムへの効果は確認されていない(SR/MA [7])
- エピジェネティック時計は疾患リスクを予測でき、世代が進むほど精度が向上する(大規模コホート [8])
- WHOは老化を医学的介入の対象として位置づけた(ICD-11 XT9T [12])
未解明点・限界
- セノリティクスの長期安全性は不明(最長で48週間のデータのみ [4])
- セノリティクスの大規模RCT(Phase III)は存在しない
- どの老化細胞を除去すべきで、どの老化細胞は残すべきかの判断基準がない(老化細胞にも有益な役割がある)
- 最適な投与レジメン(用量・間隔・期間)は未確立
- TAME試験は資金難で開始時期未定であり、メトホルミンのアンチエイジング効果への不確実性が増大 [6]
- エピジェネティック時計が「介入の効果判定」に使えるかはまだ検証途上
- 日本人集団でのセノリティクス臨床データは存在しない
今、あなたにできること——エビデンスに基づく現実的な選択
セノリティクスの臨床応用はまだ先ですが、老化の科学が教えてくれる「今日からできること」は明確です。
エビデンスの強い介入(推奨)
-
定期的な運動: 有酸素運動と筋力トレーニングの組み合わせは、老化細胞の蓄積を抑制し、SASPを低下させることが複数の研究で示されています。特に中強度の有酸素運動(週150分以上)は、エピジェネティック年齢を若く保つことと関連します。
-
カロリー制限・間欠的断食: mTOR経路とAMPK経路の調節を通じて、細胞老化を遅らせる可能性があります。ただし、極端な制限はサルコペニアのリスクを高めるため、専門家の指導下で行うことが望ましいです。
-
質の高い睡眠: 睡眠不足はエピジェネティック年齢加速と関連することが報告されています。7〜8時間の質の高い睡眠を確保することが重要です。
-
禁煙・節度ある飲酒: 喫煙と過度の飲酒は、エピジェネティック年齢を加速させる最大の修正可能リスク因子です。
エビデンスが不十分な介入(現時点では推奨しない)
- NMN/NRサプリメント: NAD+は上昇するが臨床効果は未確認 [7]。高額な投資に見合うエビデンスはまだありません。
- セノリティクスの個人輸入・自己投与: ダサチニブは白血病治療薬であり、重大な副作用のリスクがあります。臨床試験以外での使用は絶対に避けてください。
- ラパマイシンの適応外使用: 免疫抑制作用があり、自己判断での服用は感染症リスクを高めます。
かかりつけ医への相談ポイント
- 持病の管理が最大の「抗老化戦略」。高血圧、糖尿病、脂質異常症の適切な治療は、エピジェネティック年齢加速を抑える可能性があります。
- SGLT2阻害薬を服用中の方は、将来的にセノリティクス効果が追加的なベネフィットとして認められる可能性がありますが、現時点では「老化治療」目的での処方は推奨されません。
- がん検診、ワクチン接種、定期健診を怠らないこと。老化研究の「未来の薬」を待つ間に、「今の医療」を最大限活用することが最善の戦略です。
おわりに:「科学」と「希望」の正しい距離感
救急外来で、あるいは緩和ケアの現場で、私は日々「老い」と向き合っています。
骨折で運ばれてくる高齢者、認知症が進行して家族の顔がわからなくなった方、フレイルで日常生活が困難になった方——「老化」がもたらす苦しみは、現場ではあまりにもリアルです。
だからこそ、セノリティクスの研究に心が動きます。「老化した細胞を取り除けば、これらの苦しみが軽減できるかもしれない」という可能性は、臨床医としての希望です。
しかし同時に、科学者としての冷静さも忘れてはいけません。
セノリティクスはまだPhase I/IIの段階であり、12名や114名の試験結果で「効く」と断定するのは危険です。 NMNサプリメントの例が示すように、「理論的に正しい」ことと「ヒトで効く」ことの間には、深い溝があります。
それでも、老化を12のホールマークに分解し、WHOが老化を医学的介入の対象として認め、エピジェネティック時計で「生物学的年齢」を測れるようになった今——私たちは「老化を治療する」という夢に、科学史上かつてないほど近づいています。
「老化は治療できる病気になるのか」——この問いの答えは、おそらく「まだわからない。しかし、わからないことがどんどん減っている」です。
今日できる最善のことは、エビデンスに基づいた生活習慣を実践しながら、科学の進歩を正しく理解し、過剰な期待にも過剰な悲観にも振れないこと。その冷静さこそが、未来の医療を最大限に活かすための「今の準備」です。
本日のまとめ
- 老化の本質: 12の生物学的ホールマークが複雑に絡み合うプロセスであり、その「ハブ」である細胞老化がセノリティクスの標的
- セノリティクスの現在地: ヒトで老化細胞除去を実証(パイロット試験レベル)。認知機能改善の示唆もあるが、大規模RCTはまだない
- 判断に迷ったら: NMNサプリメントより、運動・睡眠・禁煙が圧倒的にエビデンスが強い。セノリティクスの自己投与は絶対に避け、臨床試験の結果を待つ
関連記事:
