はじめに:あなたの体で、今も「静かな火事」が燃えている
風邪を引いたとき、喉が赤く腫れる。膝を擦りむいたとき、傷口が熱を持つ。これらは急性炎症——体を守るための正常な防御反応です。数日で火は消え、体は元通りになります。
ところが、加齢とともに体内で起きる炎症は、まったく違う性質のものです。
熱も痛みも腫れもない。自覚症状は一切ない。しかし、血液を調べると炎症マーカーがじわじわと上昇している——この現象を、2000年にイタリアの免疫学者 Claudio Franceschi が「Inflammaging(インフラメイジング)」と名付けました [1]。
Inflammaging は直訳すると「炎症(Inflammation)+老化(Aging)」。感染症でもなく、自己免疫疾患でもない。加齢そのものに伴う、慢性的で低レベルの全身性炎症です。
2019年、Furman らは Nature Medicine に発表した包括的レビューで、この慢性炎症が心血管疾患、がん、糖尿病、認知症、腎臓病、非アルコール性脂肪肝炎(NASH)の共通基盤であることを示しました [2]。つまり、老化に伴う主要な疾患の「根っこ」に、一つの共通メカニズムがあるということです。
この記事では、Inflammaging の「なぜ起きるのか」「体に何をするのか」「どう測るのか」「どう対策するのか」を、最新のエビデンスとともに解き明かしていきます。
急性炎症と慢性炎症——まったく異なる「火」の性質
炎症を理解するには、まず「急性」と「慢性」の違いを明確にする必要があります。
| 特徴 | 急性炎症 | 慢性炎症(Inflammaging) |
|---|---|---|
| きっかけ | 感染・外傷・異物 | 明確なきっかけがない |
| 期間 | 数日〜数週間 | 数年〜数十年 |
| 強度 | 強い(発熱・腫脹・疼痛) | 弱い(自覚症状なし) |
| 目的 | 病原体の排除・組織の修復 | なし(制御の破綻) |
| 結果 | 治癒 | 臓器障害の蓄積 |
| 主なマーカー | CRP 大幅上昇 | hs-CRP 軽度上昇、IL-6 上昇 |
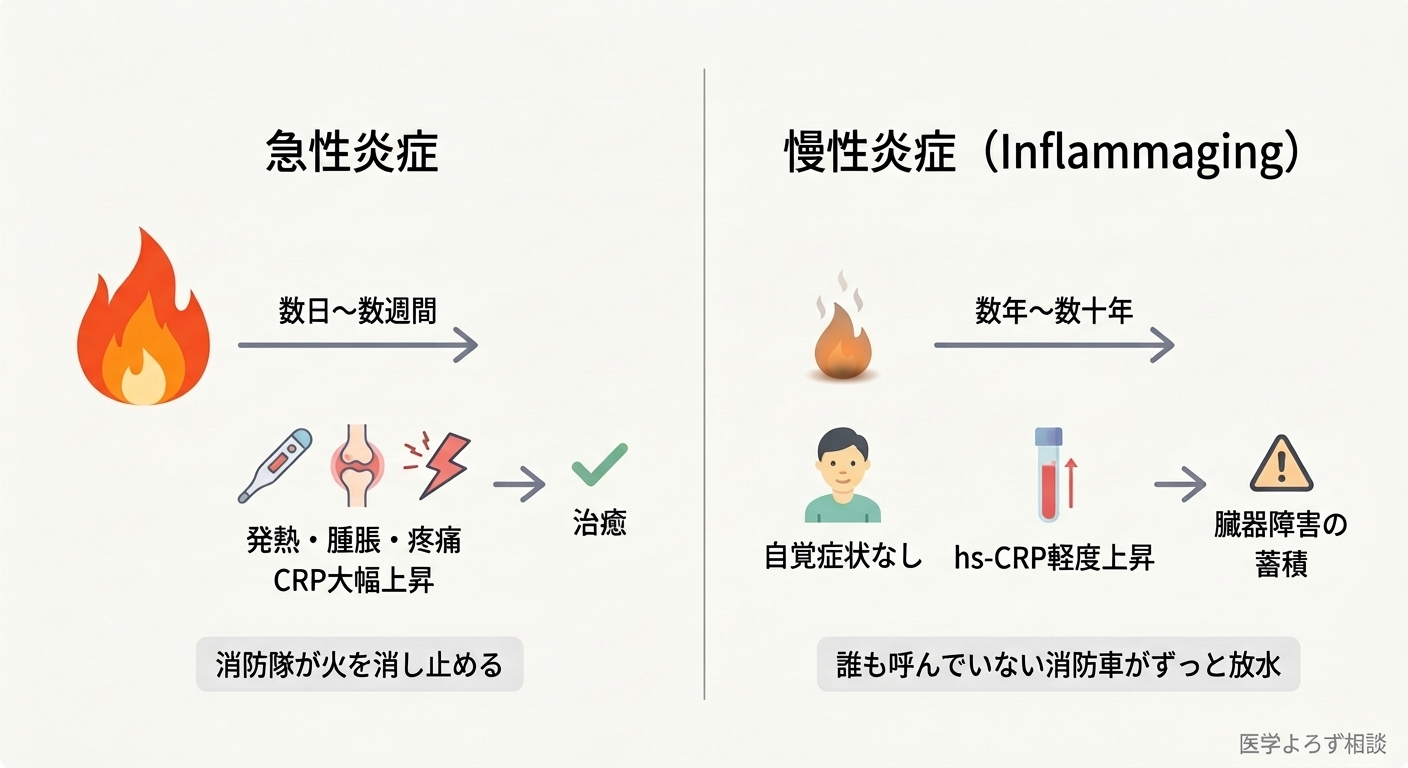
急性炎症は「消火器を持った消防隊」です。火事(感染や損傷)が起きたら駆けつけ、消し止め、撤収する。一方、Inflammaging は「誰も呼んでいないのに、ずっと放水し続ける消防車」のようなもの。消火活動自体が周囲の建物を少しずつ痛めていく——これが慢性炎症の本質です。
Inflammaging の3つの「火種」——非自己・自己・準自己
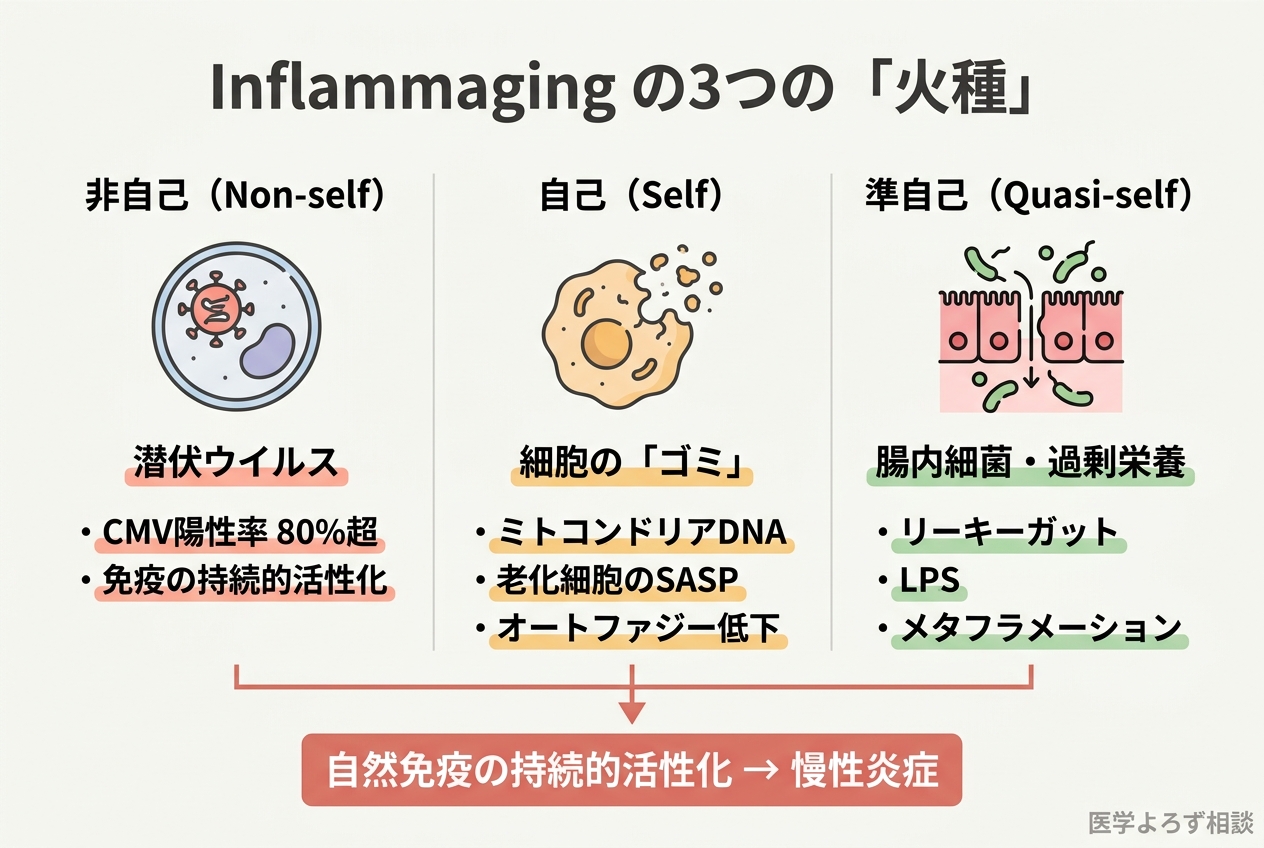
Franceschi は 2018年の Nature Reviews Endocrinology のレビューで、Inflammaging を引き起こす刺激を3つのカテゴリに分類しました [1]。
火種1:非自己(Non-self)——過去の感染の「残り火」
若い頃に感染したウイルスが完全には排除されず、体内に潜伏し続ける——その代表がサイトメガロウイルス(CMV)です。高齢者の CMV 陽性率は80%を超え、免疫系はこのウイルスを監視するために常に「戦闘態勢」を維持しなければなりません [5]。
この持続的な免疫の活性化が、慢性炎症の一因となります。加えて、加齢による免疫機能の低下(免疫老化: immunosenescence)は、病原体の完全な排除を困難にし、この悪循環を加速させます。
火種2:自己(Self)——細胞の「ゴミ」が炎症を起こす
加齢とともに、損傷を受けた細胞から「ゴミ」が放出されます。これをDAMPs(Damage-Associated Molecular Patterns: 損傷関連分子パターン)と呼びます [4]。
具体的には:
- ミトコンドリアDNA(mtDNA): 損傷したミトコンドリアから漏れ出た DNA が、自然免疫の受容体(TLR9)を刺激する [6]
- 細胞外ATP: 壊死した細胞から放出される「危険信号」
- 尿酸結晶: 細胞の代謝廃棄物が結晶化し、インフラマソームを活性化
- 老化細胞のSASP: 老化した細胞が放出する炎症性サイトカインの「カクテル」
これは、家の中にゴミが溜まり続けるようなものです。若い頃は「お掃除機能」(オートファジー)がしっかり働いてゴミを処理できますが、加齢とともにその機能が衰え、ゴミが免疫系を刺激し続けるのです。
火種3:準自己(Quasi-self)——腸内細菌と栄養の「火加減」
3つ目の火種は、体の「内側」にいながら「外側」でもある存在——腸内細菌叢です。
加齢に伴う腸内細菌叢の変化(dysbiosis)は、腸管バリアの機能低下を引き起こします [7]。これにより、通常は腸の中に留まるはずの細菌由来成分(リポ多糖: LPS)が血中に漏れ出す——いわゆる「リーキーガット」の状態です。LPSは強力な炎症刺激物質であり、全身の自然免疫を持続的に活性化します。
さらに、過剰な栄養摂取もまた炎症を促進します。Franceschi はこれを「メタフラメーション(metaflammation: 代謝性炎症)」と名付けました [1]。飽和脂肪酸や精製糖の過剰摂取は、脂肪組織にマクロファージを引き寄せ、炎症性サイトカインの産生を増加させます。
炎症の「増幅装置」——NF-κB と SASP の悪循環
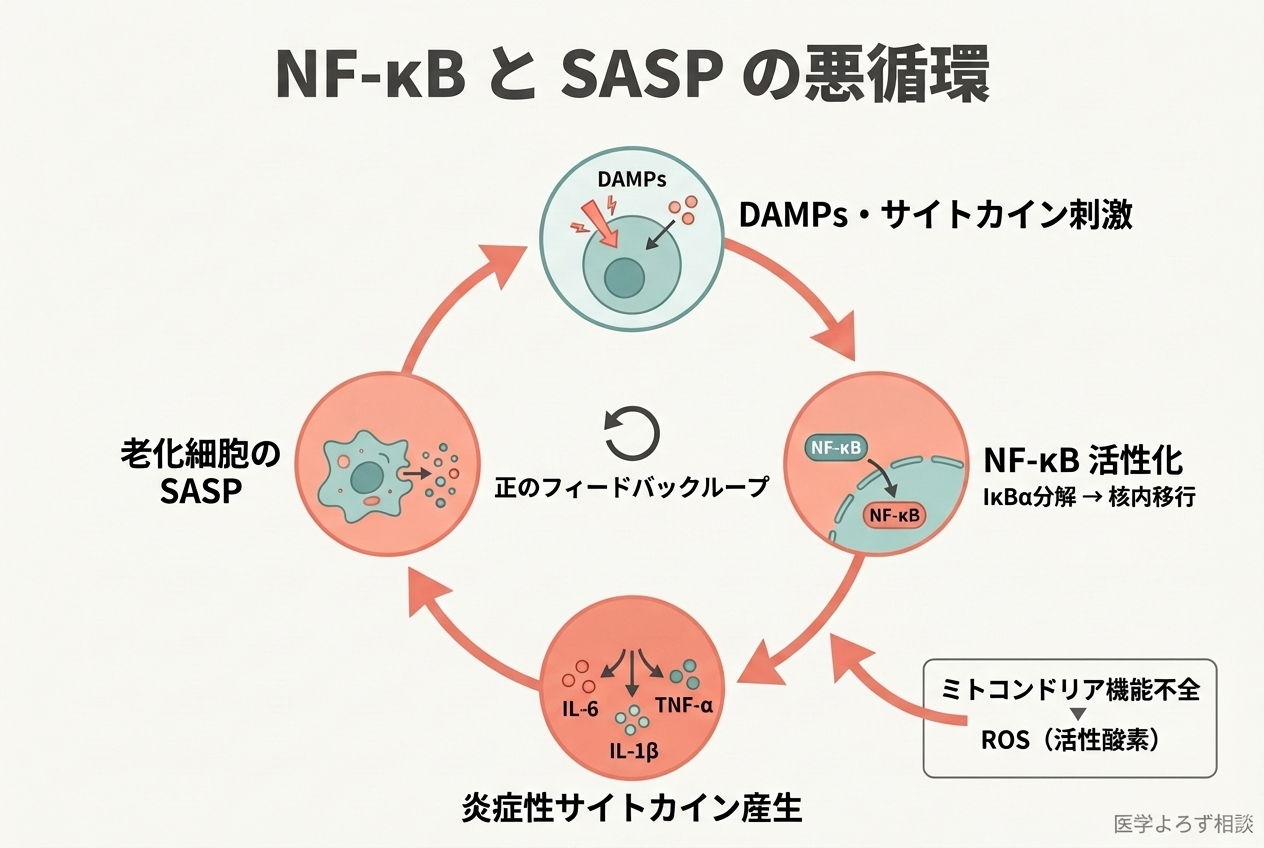
3つの火種がどのように「慢性炎症」として定着するのか——その中心的メカニズムが、NF-κB シグナル経路と SASP(老化関連分泌表現型)の悪循環です。
NF-κB:炎症の「マスタースイッチ」
NF-κB(Nuclear Factor-kappa B)は、炎症反応を制御する転写因子であり、Singh らは「Inflammaging の中心的メディエーター」と位置づけています [4]。
通常、NF-κB は IκBα というタンパク質に結合して細胞質に「封印」されています。しかし、DAMPs やサイトカインなどの刺激を受けると、IκBα が分解され、NF-κB が核内に移行。そこで IL-6、TNF-α、IL-1β などの炎症性サイトカインの遺伝子発現を活性化します。
問題は、これらのサイトカイン自体が再び NF-κB を活性化するという正のフィードバックループが形成されることです。一度「スイッチ」が入ると、自動的に炎症が増幅され続ける仕組みが出来上がります。
SASP:老化細胞の「炎症爆弾」
細胞老化(cellular senescence)とは、DNA損傷などを受けた細胞が分裂を永久に停止する現象です。若い頃はがん抑制メカニズムとして有益ですが、加齢とともに老化細胞が蓄積し、問題が生じます [8]。
老化細胞は死なない代わりに、SASP と呼ばれる炎症性分子の「カクテル」を放出し続けます:
- 炎症性サイトカイン: IL-6、IL-8、TNF-α
- ケモカイン: MCP-1、CXCL1
- 成長因子: TGF-β、VEGF
- マトリックスメタロプロテアーゼ(MMP): 組織の構造を分解する酵素
SASP は NF-κB 経路を介して産生されるため、NF-κB と SASP は相互に増幅し合う悪循環を形成しま���。Giuliani らはさらに、ミトコンドリア機能不全がこの悪循環に活性酸素種(ROS)という「燃料」を供給していることを示しました [6]。
Inflammaging が引き起こす疾患マップ
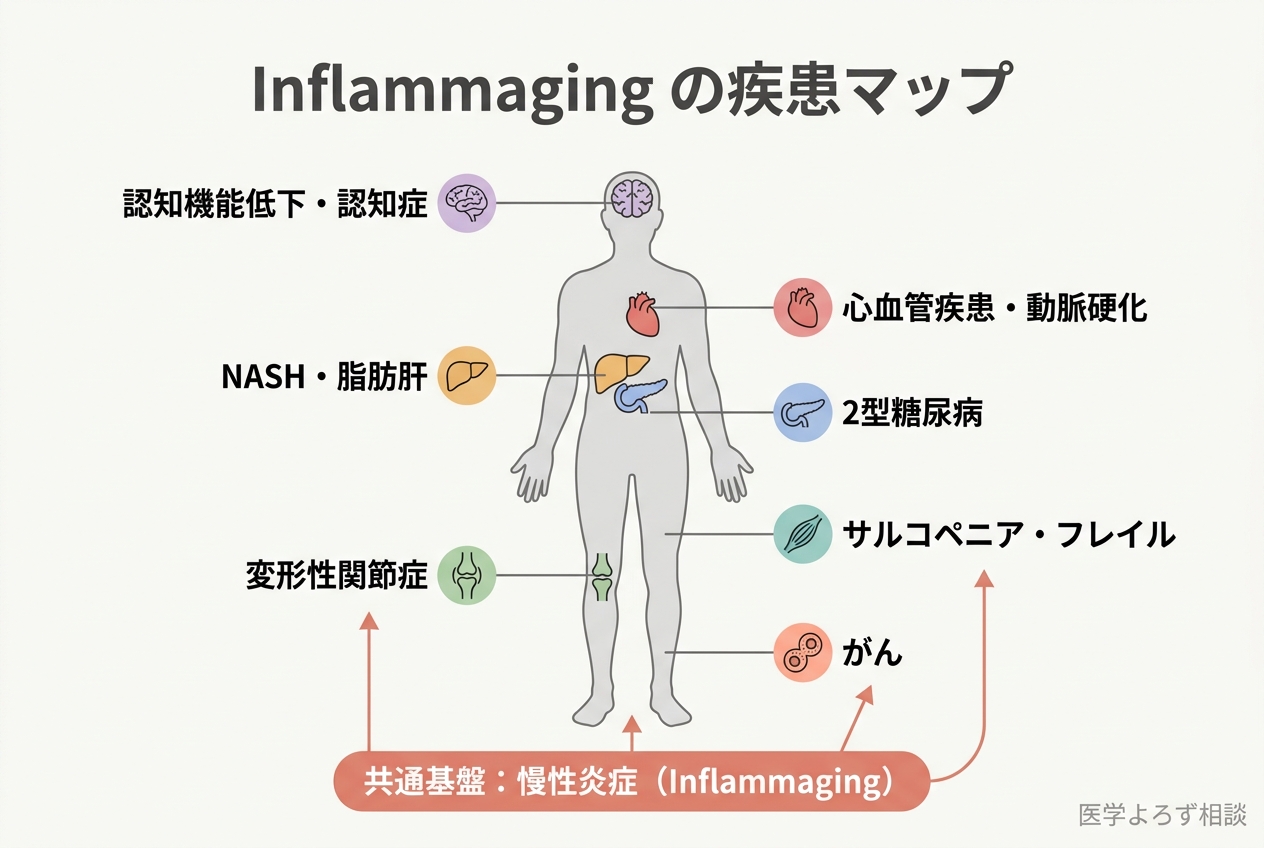
Inflammaging は特定の臓器の疾患ではなく、全身に影響を及ぼす「土壌」のような存在です。Baechle らの 2023年のレビューは、慢性炎症と老化の12のホールマーク(hallmarks of aging)が双方向的に影響し合い、さまざまな加齢関連疾患を引き起こすことを示しています [3]。
心血管系
Khavinson らは、老化した血管内皮細胞・平滑筋細胞の SASP が動脈硬化の進展に直接寄与することを報告しています [8]。IL-6 や TNF-α は血管内皮の機能障害を促進し、酸化 LDL の取り込みと泡沫細胞の形成を加速させます。
脳・認知機能
Fard らの 2022年のシステマティックレビュー(29研究を分析)では、末梢の炎症マーカー(特に IL-6 と CRP)の上昇が、認知機能の低下と逆相関を示すことが明らかになりました [9]。炎症は血液脳関門の透過性を高め、ミクログリア(脳の免疫細胞)を活性化させ、神経炎症を引き起こします。
フレイル(虚弱)
Tran Van Hoi らの 2023年のシステマティックレビュー(44研究)では、IL-6 が24研究中12研究で、CRP が19研究中7研究でフレイルと有意な関連を示しました [10]。炎症性サイトカインはサルコペニア(筋肉量の減少)を促進し、フレイルの主要な経路となっています。
関節
Motta らは、Inflammaging が変形性関節症(OA)の発症と進行に深く関与していることをレビューしています [11]。老化した滑膜細胞の SASP が軟骨分解を促進し、自然免疫と適応免疫の両方が関節破壊に寄与します。
Inflammaging のバイオマーカー——「見えない火事」を可視化する
Inflammaging の厄介な点は、自覚症状がないことです���では、どうすれば「見えない火事」を検出できるのでしょうか。
確立されたバイオマーカー
Tran Van Hoi らの系統的レビュー [10] と Fard らのレビュー [9] を総合すると、現時点で最もエビデンスが蓄積されているのは以下の3つです:
| バイオマーカー | 意味 | 臨床的意義 |
|---|---|---|
| hs-CRP | 高感度C反応性タンパク | 全身性炎症の「スクリーニング」。0.3 mg/dL 以上で心血管リスク上昇 |
| IL-6 | インターロイキン-6 | SASP の主要構成要素。認知機能低下・フレイルとの関連が最も一貫 |
| TNF-α | 腫瘍壊死因子a | NF-κB 経路の活性化を反映。フレイル・サルコペニアとの関連 |
日本の現状
日本は世界一の高齢社会であり、2025年には65歳以上人口が約30%に達しています。厚生労働省の「国民健康・栄養調査」では、高齢者の約20%が hs-CRP の軽度上昇を示しており、Inflammaging は日本の高齢者医療において無視できない問題です。
しかし、現時点では Inflammaging を測定するための確立された臨床検査パネルは存在しません。hs-CRP は一般的な健康診断で測定可能ですが、IL-6 や TNF-α は研究目的の検査に留まっています。将来的には、Kwon と Belsky が提唱する「生物学的年齢(BioAge)」のような複合指標が、Inflammaging の臨床評価に活用される可能性があります [12]。
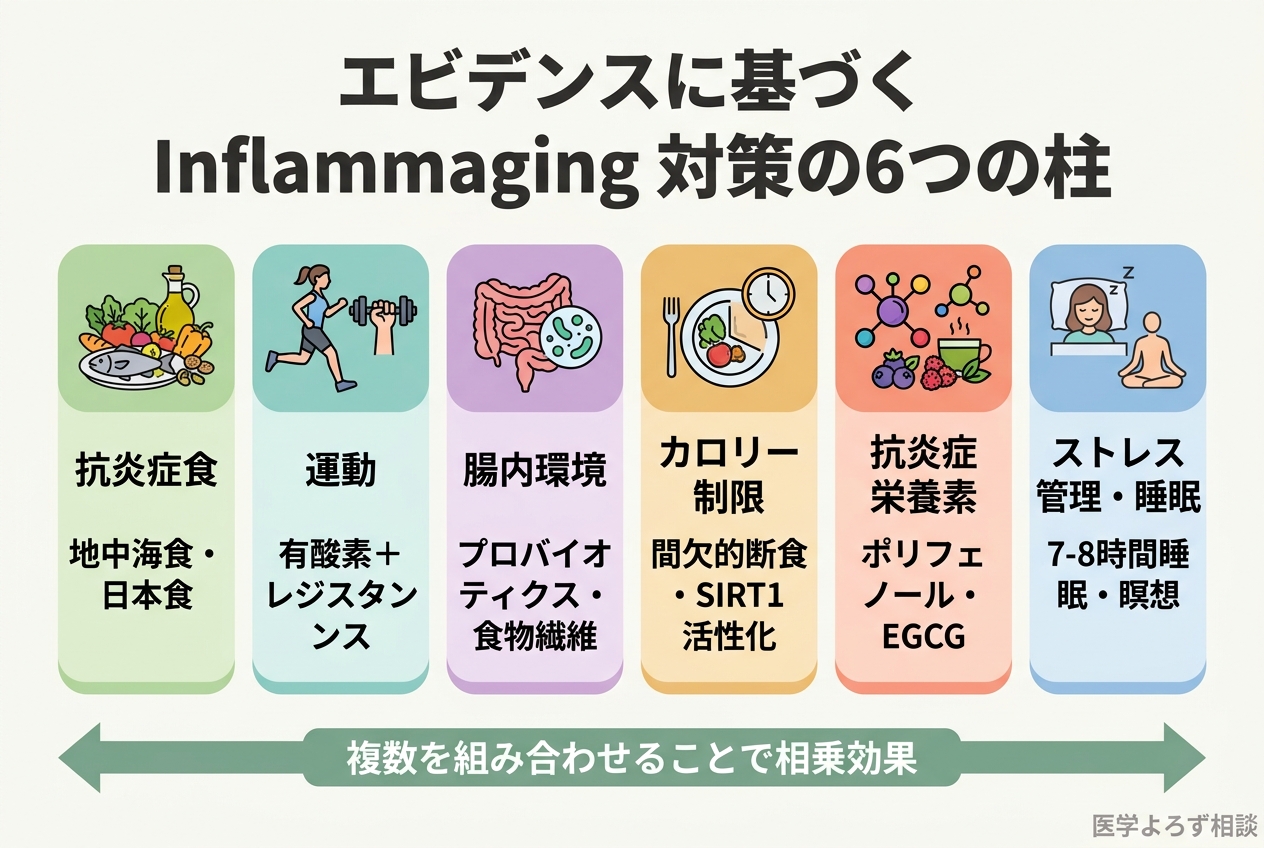
エビデンスに基づく6つの対策
Inflammaging は加齢に伴う現象ですが、そのすべてが「運命」というわけではありません。Singh らは「食事と運動による非薬物的介入で炎症を軽減できる」と結論づけており [4]、複数のシステマティックレビューがこれを裏付けています。
対策1:抗炎症食——地中海食と日本食のエビデンス
Hart らの 2021年のシステマティックレビュー(69研究)では、地中海食スコアが高い群で CRP と IL-6 が有意に低下することが示されました [13]。133件の横断的分析のうち82件で、健康的な食事パターンと低い炎症マーカーの間に有意な関連が認められています。
Di Giosia らは、地中海食の抗炎症作用を以下の3つのメカニズムで説明しています [14]:
- ポリフェノール: オリーブオイル、赤ワイン、ベリー類に含まれるポリフェノールが NF-κB の活性を直接阻害する
- オメガ3脂肪酸: 青魚に豊富な EPA/DHA が、炎症収束分子(レゾルビンやプロテクチン)の産生を促進する
- 食物繊維: 腸内細菌による短鎖脂肪酸(酪酸など)の産生を増加させ、腸管バリア機能を強化する
日本食もまた、抗炎症的な食事パターンとして注目されています。魚介類の豊富な摂取(オメガ3)、大豆製品(イソフラボン)、緑茶(カテキン)、発酵食品(腸内環境の改善)は、地中海食と共通する抗炎症成分を多く含みます。
対策2:運動——有酸素+レジスタンスの併用が最強
Xing らの 2022年のシステマティックレビュー・メタアナリシス(14件の RCT を分析)は、運動介入が炎症マーカーに及ぼす効果を定量的に示しました [15]:
- IL-6: 有意に改善(Z = 3.05; 95% CI: -3.60 to -0.79; P = 0.002)
- CRP: 有意に改善(Z = 2.44; 95% CI: -0.55 to -0.06; P = 0.01)
- TNF-α: 有意に改善(Z = 2.96; 95% CI: -2.21 to -0.45; P = 0.003)
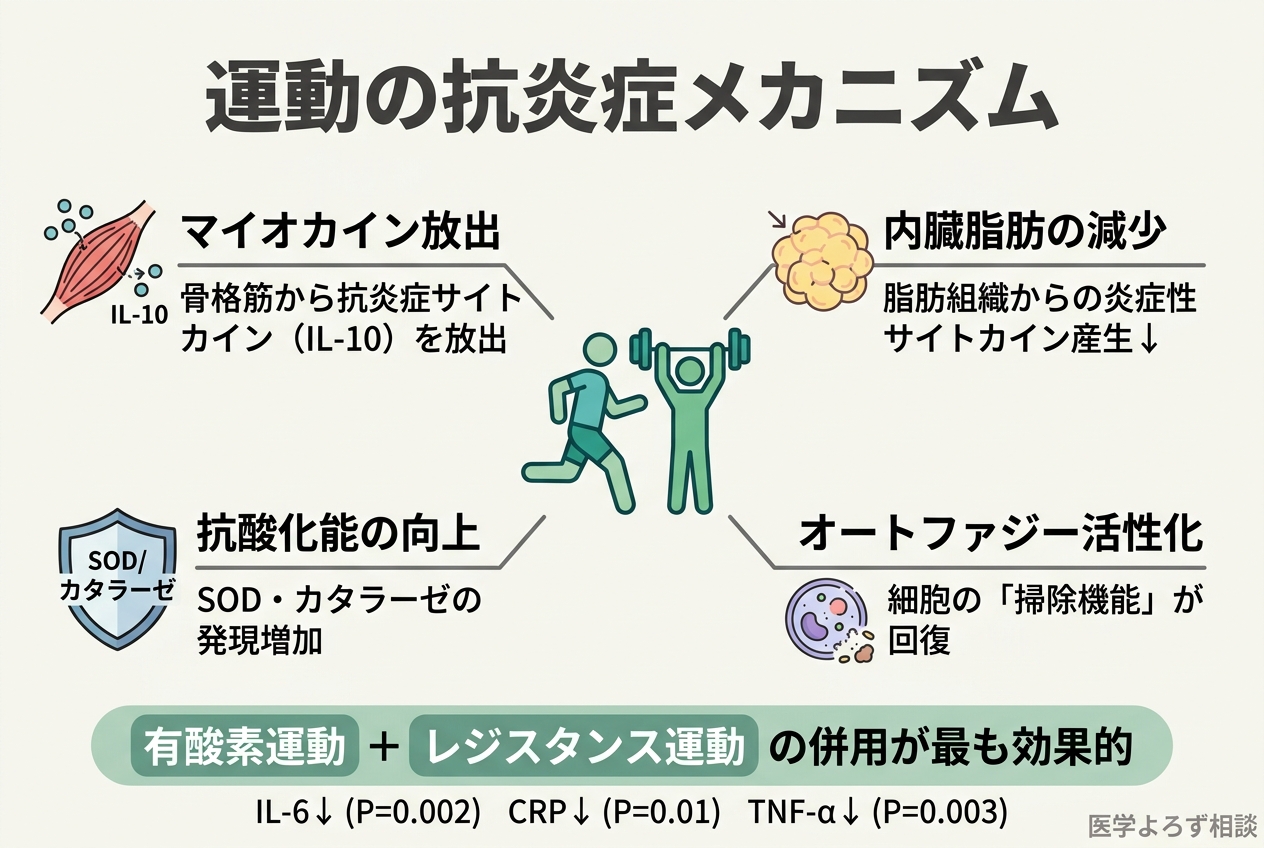
サブグループ解析では、有酸素運動とレジスタンス運動の併用が、単独の運動よりも効果が大きく、長期的な運動プログラムがより有意な改善を示しました。
Byrne らの 2023年のメタアナリシス(フレイル・サルコペニア患者対象、16研究)でも、運動と栄養介入により CRP(SMD = -0.28, P = 0.05)と IL-6(SMD = -0.28, P = 0.05)が改善しています [16]。
運動が抗炎症作用を持つメカニズム:
- 骨格筋から放出されるマイオカイン(IL-10 などの抗炎症性サイトカイン)
- 内臓脂肪の減少による脂肪組織からの炎症性サイトカイン産生低下
- 抗酸化酵素(SOD、カタラーゼ)の発現増加
- オートファジー(細胞の掃除機能)の活性化
対策3:腸内環境の整備
Ling らのレビューが示すように、腸内細菌叢は Inflammaging の重要な調節因子です [7]。加齢に伴い、Bifidobacterium や Faecalibacterium prausnitzii といった抗炎症性の菌種が減少し、Proteobacteria などの炎症促進性の菌種が増加します。
腸内環境を整えるエビデンスに基づくアプローチ:
- プロバイオティクス: Lactobacillus や Bifidobacterium を含む発酵食品の摂取
- プレバイオティクス: 食物繊維(水溶性・不溶性)を十分に摂取し、善玉菌のエサを供給
- ポリフェノール: 緑茶カテキン、ベリー類のアントシアニンが腸内環境を改善
- 抗生物質の適正使用: 不必要な抗生物質の使用を避け、菌叢の多様性を維持
対策4:カロリー制限とその模倣
Kwon と Belsky は、CALERIE試験(健常非肥満者を対象とした世界初のカロリー制限 RCT)のデータを BioAge ツールキットで解析し、25%のカロリー制限が生物学的老化を遅延させることを示しました [12]。
Di Giosia らのレビューでも、カロリー制限が NF-κB の活性を低下させ、サーチュイン(SIRT1)を活性化することで、Inflammaging を抑制する分子経路が解説されています [14]。
実践的には、極端なカロリー制限よりも間欠的断食(16:8法やtime-restricted feeding)がより持続可能なアプローチとして注目されています。
対策5:抗酸化・抗炎症栄養素
Gurau らは、抗老化(anti-senescence)作用を持つ天然化合物について包括的にレビューしています [17]:
| 成分 | 食品源 | 作用メカニズム |
|---|---|---|
| レスベラトロール | 赤ワイン、ブドウ | SIRT1 活性化、NF-κB 抑制 |
| ケルセチン | タマネギ、りんご | セノリティクス作用(老化細胞の除去) |
| EGCG | 緑茶 | 抗酸化、NF-κB 抑制、テロメラーゼ活性化 |
| クルクミン | ウコン | NF-κB 直接阻害、COX-2 抑制 |
| フィセチン | イチゴ、りんご | 老化細胞除去、抗炎症 |
これらのポリフェノール類は、地中海食や日本食に含まれる抗炎症成分と重なる部分が多く、特定のサプリメントに頼るよりも食事全体のパターンを改善することが推奨されます。
対策6:ストレス管理と睡眠
Furman らは、心理的ストレスが慢性炎症の独立したリスク因子であることを強調しています [2]。ストレスは視床下部-下垂体-副腎(HPA)軸を介してコルチゾールを上昇させ、短期的には抗炎症的に働きますが、慢性的なストレスはコルチゾール抵抗性を引き起こし、炎症を促進します。
- 睡眠の質: 睡眠不足は IL-6 と CRP を上昇させる。7〜8時間の質の良い睡眠が推奨される
- マインドフルネス・瞑想: NF-κB の活性を低下させるエビデンスが蓄積されつつある
- 社会的つながり: 社会的孤立は慢性炎症のリスク因子。地域活動や趣味の仲間との交流が重要
科学の現在地:わかっていること、いないこと
確立された知見(Known)
- Inflammaging は加齢に伴う普遍的現象であり、hs-CRP、IL-6、TNF-α の慢性的上昇として観測できる [1][2]
- NF-κB と SASP の正のフィードバックループが慢性炎症の持続メカニズムである [4][8]
- 地中海食や抗炎症食は IL-6・CRP を低下させる(69研究のSR) [13]
- 有酸素+レジスタンス運動の併用は IL-6・CRP・TNF-α を有意に改善する(14 RCT のMA) [15]
- 腸内細菌叢の加齢に伴う変化(dysbiosis)が Inflammaging に寄与する [7]
- 25%のカロリー制限は生物学的老化を遅延させる(CALERIE RCT) [12]
未解明点・限界(Unknown)
- Inflammaging の「閾値」は不明: どの程度の慢性炎症が疾患リスクを有意に高めるのか、個人差も含めて未確立
- 因果関係 vs 相関: 多くの知見は横断研究に基づいており、縦断研究のエビデンスは限定的 [13]
- バイオマーカーの個人差: IL-6 や CRP の基準値は遺伝的背景、性別、BMI により大きく異なり、一律の基準設定が困難 [10]
- セノリティクス(老化細胞除去薬)のヒトでの有効性と安全性: 動物実験では有望だが、長期的なヒト臨床データは不十分
- 腸内細菌叢介入の最適プロトコル: プロバイオティクスの菌株、用量、投与期間の標準化が進んでいない
- 食事パターンの縦断的エビデンス: 横断研究では関連が示されているが、介入研究のエビデンスはまだ限られている [13]
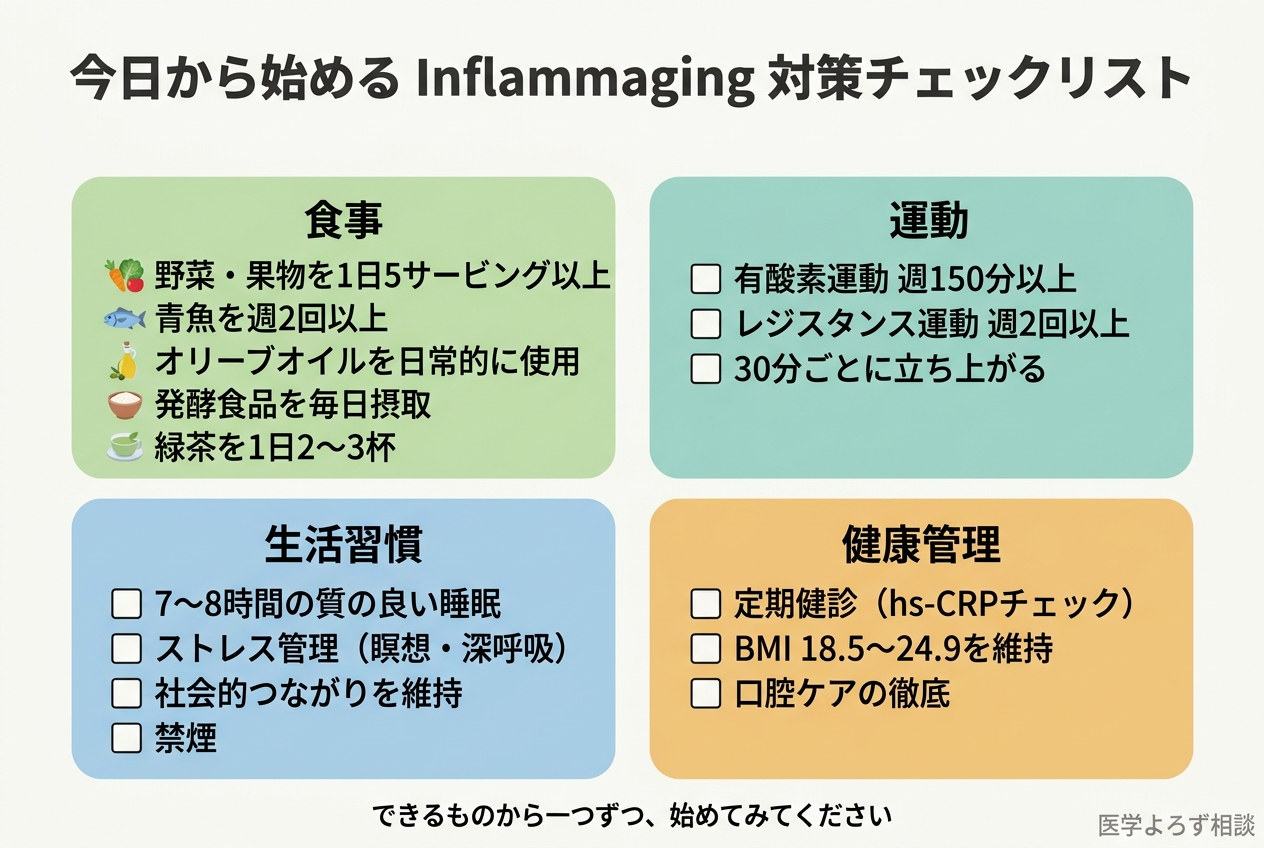
実践チェックリスト:今日から始める Inflammaging 対策
エビデンスに基づき、日常生活で実践できる対策を整理しました。すべてを一度に始める必要はありません——できるものから一つずつ、始めてみてください。
食事
- 野菜・果物を1日5サービング以上摂取する
- 青魚を週2回以上食べる(EPA/DHA の摂取)
- オリーブオイルを日常的に使用する
- 精製糖と加工食品を減らす
- 発酵食品(味噌・納豆・ヨーグルト)を毎日摂取する
- 緑茶を1日2〜3杯飲む
運動
- 中強度の有酸素運動を週150分以上行う(早歩き・水泳・サイクリング)
- レジスタンス運動を週2回以上行う(スクワット・腕立て伏せ・ダンベル)
- 長時間の座位を避け、30分ごとに立ち上がる
生活習慣
- 7〜8時間の質の良い睡眠を確保する
- ストレス管理法を実践する(瞑想・深呼吸・趣味の時間)
- 社会的なつながりを維持する
- 禁煙する(喫煙は NF-κB を直接活性化する)
- 過度な飲酒を避ける
健康管理
- 定期的に健康診断を受ける(hs-CRP をチェック)
- BMI 18.5〜24.9 を維持する(内臓脂肪の蓄積を防ぐ)
- 口腔ケアを徹底する(歯周病は慢性炎症の重要な原因)
おわりに:「静かな火事」を消すのは、日々の小さな選択
Inflammaging は、目に見えず、痛みもなく、検査値の異常も軽微です。だからこそ、見過ごされてきました。
しかし、科学が明らかにしたのは、この「静かな火事」こそが、心血管疾患、認知症、がん、フレイルといった加齢関連疾患の共通の土壌であるということです。
そして同時に、科学はもう一つの重要な事実も示しています——Inflammaging は、食事、運動、睡眠、腸内環境の改善といった非薬物的介入で、確実に軽減できるということです。
外来で患者さんに伝えたいのは、いつもこのことです。
「老化は止められないかもしれない。でも、老化の"速度"は、あなたの毎日の選択で変えられる」
今日の食事に魚を一品加える。明日は30分だけ歩いてみる。寝る前にスマホを手放して、睡眠の質を上げる——その一つひとつが、体内の「静かな火事」を少しずつ鎮めてくれます。
Inflammaging の科学は、まだ発展途上です。しかし、すでに十分なエビデンスが蓄積されています。「できることから、今日から」。それが、最も確実な抗老化戦略です。
本日のまとめ
- Inflammaging の本質: 加齢に伴う慢性的・低レベルの全身性炎症。非自己・自己・準自己の3つの火種が、NF-κB/SASP の悪循環を通じて持続する
- 疾患との関連: 心血管疾患、認知症、がん、糖尿病、フレイルなど加齢関連疾患の共通基盤
- 対策のエビデンス: 抗炎症食(地中海食・日本食)、有酸素+レジスタンス運動の併用、腸内環境の整備、適切な睡眠・ストレス管理が有効
- 判断に迷ったら: 定期的な健康診断で hs-CRP をチェックし、かかりつけ医に相談を
