はじめに:健康診断は「異常なし」——なのに、なぜ疲れが取れないのか
40代を過ぎたあたりから、こんな経験はないでしょうか。
「健康診断では引っかからない。でも、なんとなく疲れやすい」「朝起きたとき、体が重い」「関節がこわばる」「風邪が治りにくくなった」——。
かかりつけ医に相談しても、「年齢のせいですね」で終わってしまう。血液検査の数値は基準値内。画像検査でも異常なし。
しかし、この「なんとなくの不調」の背後には、科学的に明確なメカニズムが潜んでいます。
それがInflammaging(インフラメイジング)——「慢性炎症」と「老化」が手を結んだ、静かな体内の火事です。
2000年にイタリアの免疫学者Claudio Franceschiが提唱したこの概念 [1] は、それから四半世紀を経て、今や老化研究の中心的なパラダイムとなりました。2018年のNature Reviews Cardiologyのレビューでは、Inflammagingが心血管疾患、2型糖尿病、アルツハイマー病、がん、フレイル(虚弱)のすべてに共通する「上流の病態」として位置づけられています [2]。
つまり、Inflammagingは単なる「老化の一側面」ではなく、加齢関連疾患のほぼすべてを貫く根本メカニズムなのです。
この記事では、Inflammagingの5つの「火種」を科学的に解き明かし、その消火活動——エビデンスに基づいた実践的な対策を、最新の臨床研究とともにお伝えします。
Inflammagingとは何か——「老化=慢性炎症」という革命的な視点
急性炎症と慢性炎症:まったく別のもの
まず重要な区別があります。
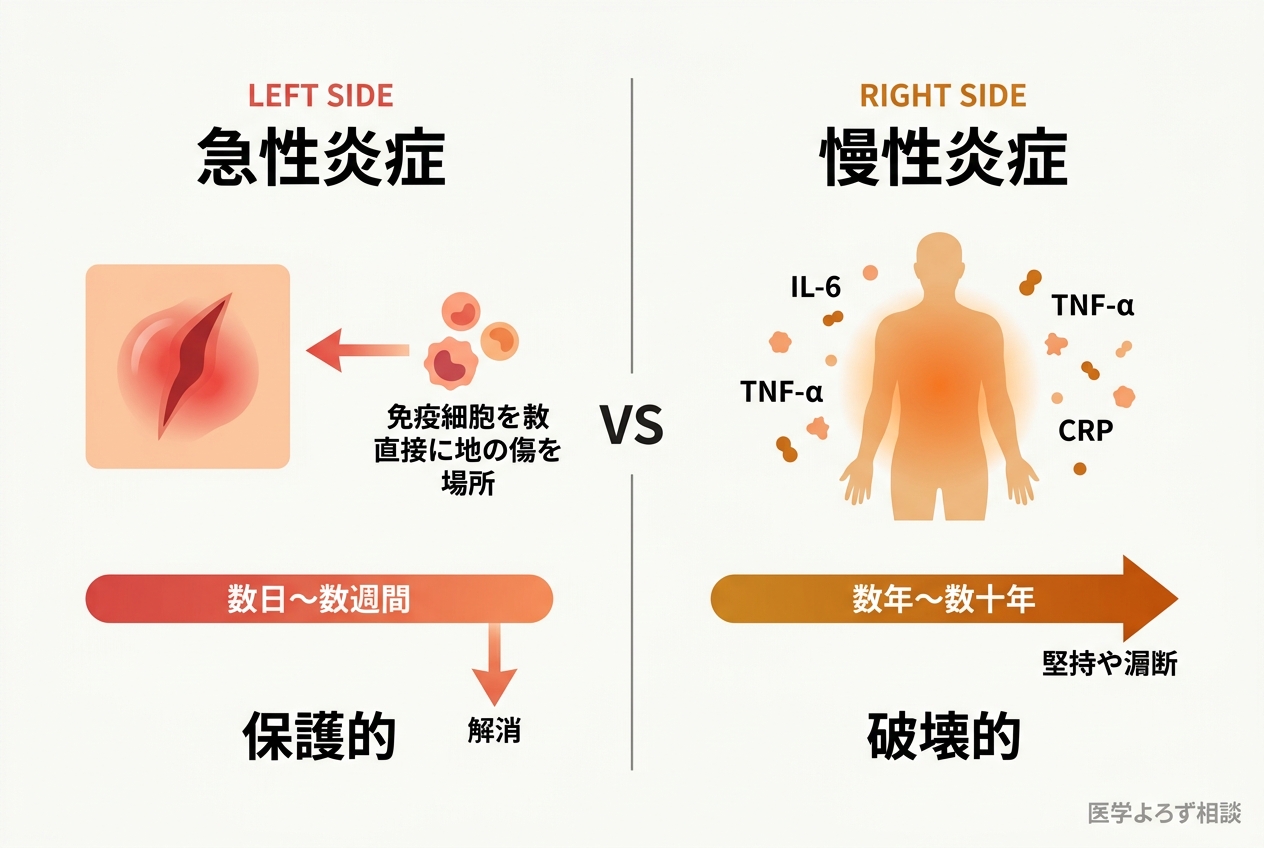
急性炎症は、体を守る正常な反応です。ケガをしたとき、傷口が赤く腫れて熱を持つ。これは免疫細胞が集まり、病原体を排除し、組織を修復している証拠です。通常は数日から数週間で収束します。
一方、慢性炎症はまったく異なります。
明確な感染源もケガもないのに、免疫システムが「低レベルの警戒態勢」を維持し続ける。炎症性サイトカイン——IL-6、TNF-α、IL-1β、CRPといった分子が、血中にわずかに上昇したまま居座る。痛みも腫れもない。本人は気づかない。しかし、この「静かな炎症」が数年、数十年と持続することで、血管内皮を傷つけ、インスリン抵抗性を高め、神経変性を促進し、がん微小環境を整えていくのです [2][3]。
Franceschiのブレークスルー
2000年、Franceschiらは100歳以上の超長寿者(centenarians)の血液を分析し、驚くべき発見をしました [1]。
超長寿者は一般高齢者と比較して、炎症性サイトカインのレベルが上昇しているにもかかわらず、同時に抗炎症性サイトカイン(IL-10など)も高いレベルで維持していたのです。
つまり、「炎症がゼロ」なのではなく、「炎症と抗炎症のバランス」を保てているかどうかが、健康長寿の鍵だったのです。
Franceschiはこの現象を「Inflammaging」と名づけました——inflammation(炎症)とaging(老化)を組み合わせた造語です。加齢に伴い、炎症が優位になり、抗炎症の防御線が破れる。その結果、全身が「慢性的な低レベル炎症」の海に沈んでいく。
5つの「火種」——Inflammagingはどこから来るのか
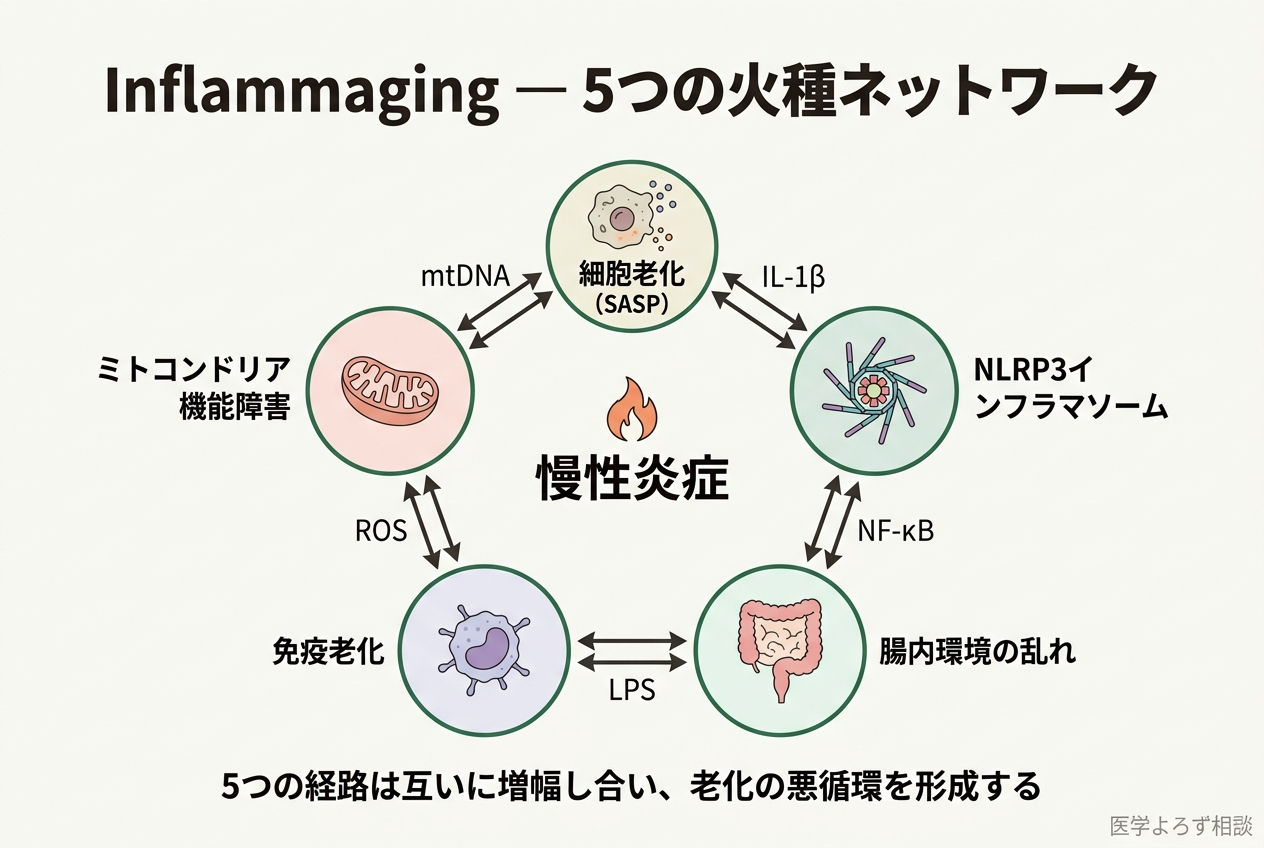
Inflammagingは単一の原因で起こるわけではありません。複数のメカニズムが同時に、そして相互に増幅しながら進行します。ここでは主要な5つの火種を解説します。
火種1:ゾンビ細胞のSASP——老化細胞が撒き散らす炎症
細胞は強いストレス(DNA損傷、テロメア短縮、がん遺伝子の活性化など)を受けると、増殖を永久に停止する「細胞老化(cellular senescence)」の状態に入ります。これ自体はがん抑制の防御機構です。
問題は、老化した細胞が静かに眠るわけではないことです。
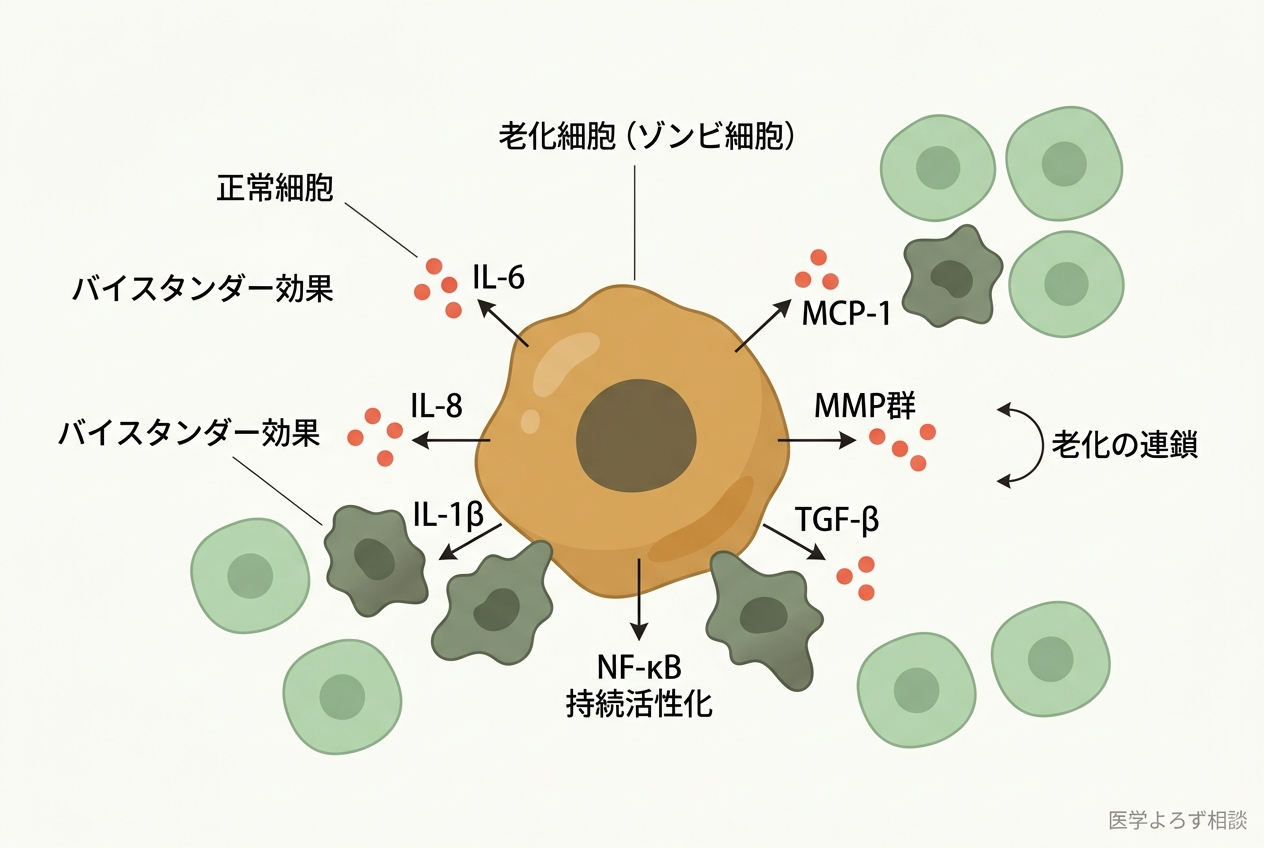
老化細胞はSASP(Senescence-Associated Secretory Phenotype:老化関連分泌表現型)と呼ばれる現象を通じて、IL-6、IL-8、IL-1β、MCP-1、MMP群、TGF-βなど数百種類の炎症性因子を周囲に撒き散らします [4]。
Coppeらの2010年のレビューによれば、SASPの構成は組織によって異なりますが、共通してNF-κBシグナルの持続的活性化が中心的な役割を果たしています [4]。さらにSASPは「バイスタンダー効果」を持ち、周囲の正常細胞をも老化に誘導する——つまり、老化が老化を呼ぶ正のフィードバックループが形成されるのです。
火種2:NLRP3インフラマソーム——炎症の増幅装置
NLRP3インフラマソームは、自然免疫の中核をなすタンパク質複合体です。
通常は病原体や組織損傷のシグナルを感知して活性化し、カスパーゼ-1を介してIL-1βとIL-18を成熟・放出させる——いわば「炎症の着火装置」です [5]。
加齢に伴い、この着火装置が過敏になります。
Swansonらの2019年のNature Reviews Immunologyのレビュー [5] は、NLRP3が加齢性疾患の多くで異常活性化していることを示しました。アルツハイマー病ではアミロイドβがNLRP3を活性化し [6]、2型糖尿病ではパルミチン酸(飽和脂肪酸)や高血糖がトリガーとなります。動脈硬化では酸化LDLやコレステロール結晶がNLRP3を刺激し、プラーク内の炎症を増幅させます。
重要なのは、NLRP3がSASPと相互作用する点です。老化細胞が放出するIL-1βがNLRP3をさらに活性化し、NLRP3が産生するIL-1βがさらに老化細胞のSASPを促進する——二重の正のフィードバックが形成されます。
火種3:腸内細菌叢のディスバイオシスと代謝性エンドトキセミア
加齢に伴い、腸内細菌叢の多様性が低下します。
特に、短鎖脂肪酸(酪酸、プロピオン酸、酢酸)を産生する有益菌(Faecalibacterium、Bifidobacterium、Roseburia等)が減少し、代わりに炎症を促進する菌種(Enterobacteriaceae等)が増加します [7]。
Thevaranjanらの2017年の研究は、このディスバイオシスがInflammagingの直接的な原因となることを実験的に証明しました [7]。加齢マウスの腸内細菌叢を無菌の若齢マウスに移植すると、若齢マウスの全身性炎症が上昇したのです。
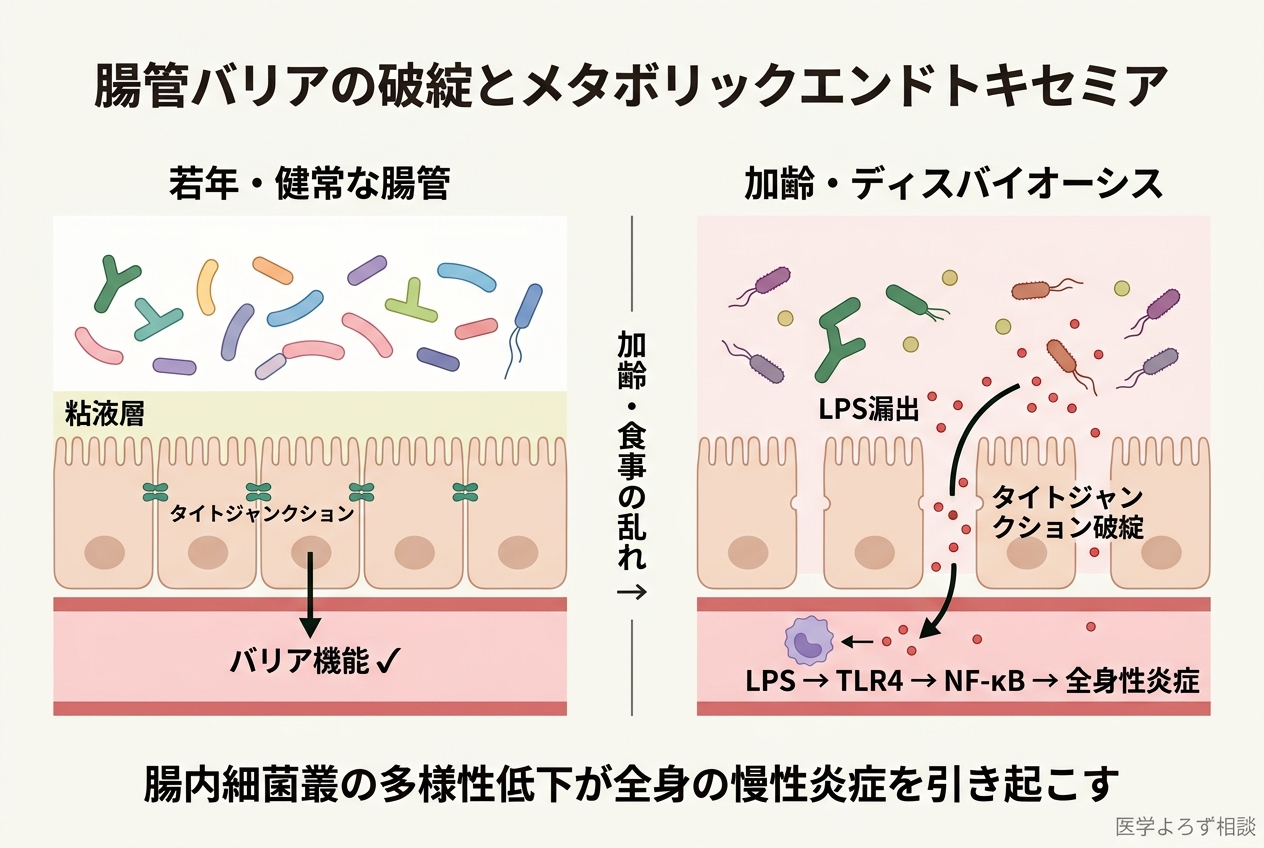
メカニズムの中心にあるのが代謝性エンドトキセミアです。腸管バリア(タイトジャンクション)の機能が加齢とともに低下し、グラム陰性菌の細胞壁成分であるLPS(リポ多糖)が血中に漏出する。LPSは自然免疫細胞のTLR4(Toll様受容体4)を刺激し、NF-κBを活性化して全身性の炎症を引き起こします [7][8]。
火種4:免疫老化(Immunosenescence)
免疫システムそのものも老化します。
胸腺の退縮は思春期から始まり、50歳までに胸腺組織の大部分が脂肪に置換されます。結果としてナイーブT細胞の供給が激減し、免疫レパートリーの多様性が失われます [9]。
代わりに増加するのが、老化T細胞(CD28-CD57+CD8+ T細胞)です。これらの細胞は増殖能を失っていますが、大量のIFN-γやTNF-αを産生し続ける——免疫機能は低下しているのに、炎症だけは増えるという矛盾した状態です。
Fulopらの2018年のレビュー [9] は、この免疫老化がInflammagingの主要なドライバーの一つであることを包括的に論じています。CMV(サイトメガロウイルス)の慢性潜伏感染も重要です。成人の50-80%が保有するCMVに対して、加齢とともに免疫リソースの過大な割り当てが起こり、他の防御が手薄になると同時に慢性的な炎症を生みます。
火種5:ミトコンドリア機能不全と酸化ストレス
ミトコンドリアは細胞のエネルギー工場ですが、加齢とともにその機能が低下します。
電子伝達系の効率が落ち、活性酸素種(ROS)の産生が増加する。ROSはミトコンドリア自身のDNA(mtDNA)を損傷し、損傷したmtDNAが細胞質に漏出する。この漏出したmtDNAがcGAS-STING経路を活性化し、I型インターフェロンや炎症性サイトカインの産生を誘導する——これがミトコンドリア由来の炎症シグナルです [10][11]。
Lopez-Otinらの2016年のレビュー [10] は、ミトコンドリア機能不全がSASP、NLRP3活性化、免疫老化のすべてと相互作用し、Inflammagingの統合的な増幅装置として機能することを示しました。
CANTOS試験が切り拓いた地平——「炎症を消せば病気は減る」の証明
Inflammagingが「仮説」から「治療標的」に昇格する決定的な転機となったのが、CANTOS試験(Canakinumab Anti-inflammatory Thrombosis Outcomes Study)です [12]。
2017年にNew England Journal of Medicineに発表されたこのランダム化比較試験は、Paul Ridkerらが率いた、被験者10,061人、追跡期間中央値3.7年の大規模RCTです。
対象は心筋梗塞既往があり、かつ高感度CRP(hs-CRP)が2 mg/L以上の患者——つまり「残余炎症リスク」を持つ集団です。
介入は画期的でした。 IL-1β(Inflammagingの中心的サイトカイン)を直接中和するモノクローナル抗体カナキヌマブを、コレステロールに一切触れずに投与したのです。
結果:
- カナキヌマブ150mg群では、主要心血管イベント(心筋梗塞・脳卒中・心血管死)が15%減少(HR 0.85, 95%CI 0.74-0.98, p=0.021)[12]
- LDLコレステロールは変化なし——純粋に炎症を抑えることで心血管リスクが低下した
- 驚くべき副次的発見として、肺がんの発生率が67%減少(HR 0.33, 95%CI 0.18-0.59)[13]
この結果は、「炎症は単なる結果ではなく、疾患の原因である」ことを、10,000人規模のRCTで初めて証明しました。
ただし、カナキヌマブには重大なトレードオフがありました。致死的感染症のリスクが上昇し、全死亡率は有意な改善を示しませんでした(HR 0.94, 95%CI 0.83-1.06)[12]。現時点で心血管疾患への適応は承認されていません。

「静かな炎症」を鎮める——エビデンスに基づく5つの実践戦略
CANTOS試験は「炎症を標的にする」戦略の有効性を証明しましたが、モノクローナル抗体は現実的な選択肢ではありません。では、私たちが日常生活の中で実践できるInflammaging対策は何でしょうか。
戦略1:運動——最も強力な抗炎症薬
Zhengらの2019年のシステマティックレビュー・メタアナリシス [14](RCT 18件、被験者1,250名)は、定期的な運動がCRP、IL-6、TNF-αのすべてを有意に低下させることを示しました。
特に効果が大きかったのは:
- 中等度の有酸素運動(ウォーキング、軽いジョギング、水泳)を週150分以上
- レジスタンス運動(筋力トレーニング)の併用
運動がInflammagingを抑制するメカニズムは複数あります。骨格筋から放出される抗炎症性マイオカイン(IL-6の一過性放出→IL-10誘導)、内臓脂肪の減少によるアディポカインプロファイルの改善、ミトコンドリアバイオジェネシスの促進、そして腸内細菌叢の多様性向上です [14][15]。
戦略2:地中海食——抗炎症食のゴールドスタンダード
Galicia-Garciaらの2020年のレビュー [16] および複数のメタアナリシスの知見を統合すると、地中海食が炎症マーカーに与える効果は以下の通りです。
- IL-6の有意な低下
- IL-1βの有意な低下
- TNF-αの有意な低下
地中海食の抗炎症効果の主役は:
- エクストラバージンオリーブオイル: オレオカンタールがCOX-1/COX-2を阻害(イブプロフェンと類似の機序)
- 魚介類のω-3脂肪酸(EPA/DHA): レゾルビン・プロテクチンの産生を促進し、炎症の「消火」を助ける
- ポリフェノール類(ブルーベリー、赤ワイン、緑茶): NF-κBシグナルの抑制
- 食物繊維: 腸内細菌による短鎖脂肪酸(特に酪酸)の産生を促進
戦略3:腸内環境の最適化
腸内細菌叢がInflammagingの主要な火種である以上、腸内環境の整備は戦略の中心に位置します [7][8]。
実践的なアプローチ:
- プレバイオティクス: 食物繊維を1日25g以上摂取する(野菜、果物、全粒穀物、豆類)。食物繊維は腸内の有益菌の「エサ」となり、酪酸の産生を促進する
- 発酵食品: ヨーグルト、納豆、味噌、キムチ、ザワークラウトなどを日常的に摂取する
- 加工食品・添加物の制限: 乳化剤(ポリソルベート80、カルボキシメチルセルロース)は腸管バリアを直接損傷する可能性がある
- プロバイオティクス: エビデンスが確立された菌株(Lactobacillus rhamnosus GG、Bifidobacterium longum等)を検討する
戦略4:睡眠の質の確保
Irwinらの2016年のメタアナリシス [17](研究72件、被験者50,000名以上)は、睡眠障害とCRP・IL-6の上昇に有意な関連があることを示しました。
特に7時間未満の短時間睡眠と、睡眠の質の低下(中途覚醒、入眠困難)が、炎症マーカーの上昇と関連していました。
睡眠中は成長ホルモンの分泌、免疫細胞の再配置、グリンパティックシステム(脳の老廃物排出機構)が活性化します。慢性的な睡眠不足はこれらすべてを阻害し、Inflammagingを加速させます [17]。
戦略5:慢性ストレスの管理
心理的ストレスはHPA軸(視床下部-下垂体-副腎軸)を慢性的に活性化し、コルチゾールの調節異常を引き起こします。慢性的な高コルチゾール状態は、逆説的に免疫系のグルココルチコイド抵抗性を誘導し、NF-κBの抑制が外れることで炎症が増幅されます [2]。
エビデンスが蓄積されている実践:
- マインドフルネス瞑想(1日10-20分のマインドフルネスがCRP、IL-6を低下させるRCTが複数報告されている)
- 社会的つながりの維持(孤独は喫煙に匹敵する炎症促進因子)
- 自然環境への曝露(森林浴の免疫調節効果)

科学の現在地:わかっていること、いないこと
確立された知見:
- 加齢に伴い、炎症性サイトカイン(IL-6、TNF-α、CRP)が慢性的に上昇する [1][2]
- SASP、NLRP3、腸内細菌叢の変化、免疫老化、ミトコンドリア機能不全が複合的にInflammagingを駆動する [2][4][5][7][10]
- IL-1βの薬理学的阻害が心血管イベントを減少させる(CANTOS試験)[12]
- 運動と地中海食が炎症マーカーを有意に低下させる [14][16]
- 睡眠障害が全身性炎症と関連する [17]
未解明点・限界:
- Inflammagingの「引き金」と「結果」の因果関係は完全には解明されていない——炎症が老化を促進するのか、老化が炎症を惹起するのか、おそらくその両方だが比重は不明
- 個人差の分子基盤がわかっていない——なぜ同年齢でもInflammagingの程度に大きな差があるのか、遺伝的要因と環境要因の寄与率は未確定
- Inflammagingの最適なバイオマーカーが確立されていない——hs-CRPは感度が不十分で、IL-6やTNF-αは日内変動が大きい。GlycAやGDF-15などの新規マーカーの研究が進行中 [18]
- セノリティクス(老化細胞除去薬)のヒトでの有効性はまだ初期段階——動物実験では劇的な効果があるが、大規模RCTは進行中
- 抗炎症介入の最適なタイミング・強度・期間が不明——早すぎる介入は免疫監視を弱め、感染症やがんのリスクを高める可能性がある
実践チェックリスト:あなたのInflammaging度を確認する
あなたのInflammagingリスクを確認してみましょう。以下の項目に複数該当する場合は、生活習慣の見直しを検討してください。
リスク因子チェック:
- □ BMI 25以上(内臓脂肪型肥満は特にリスクが高い)
- □ 運動習慣がない(週150分未満の中等度運動)
- □ 加工食品・超加工食品の摂取が多い
- □ 野菜・果物の摂取が1日350g未満
- □ 睡眠時間が6時間未満、または睡眠の質が悪い
- □ 慢性的なストレスを感じている
- □ 喫煙している
- □ 歯周病がある(歯周病菌はInflammagingの重要な促進因子)
医療機関で確認できる指標:
- hs-CRP(高感度C反応性蛋白): 1.0 mg/L未満が理想的
- HbA1c: 5.6%未満
- 空腹時血糖: 100 mg/dL未満
- 腹囲: 男性85cm未満、女性90cm未満(日本のメタボリックシンドローム基準)

おわりに:「静かな炎症」を消す旅は、今日から始められる
Inflammagingの研究は、私たちに重要なメッセージを伝えています。
老化は「何もできない宿命」ではない。 少なくとも、そのスピードと程度は私たちの選択で変えられる。
CANTOS試験は、炎症を標的にするアプローチが有効であることを10,000人規模で証明しました。しかし、モノクローナル抗体のような薬を使わなくても、運動、食事、睡眠、ストレス管理、腸内環境の最適化——これらの生活習慣の改善が、薬と同等、あるいはそれ以上の抗炎症効果を持つことも、エビデンスが示しています。
外来で「年齢のせいですね」と言われたとき、それは正しくもあり、不完全でもあります。年齢とともに炎症が増えるのは事実ですが、その炎症を放置するか、積極的に鎮めるかは、あなた自身の選択です。
この記事をきっかけに、まず一つ——週に30分のウォーキングでも、食卓にオリーブオイルを加えることでも——「静かな炎症を消す」第一歩を踏み出していただければ幸いです。
本日のまとめ
- Inflammagingの本質: 加齢に伴う慢性的な低レベル炎症であり、心血管疾患・糖尿病・認知症・がん・フレイルのすべてに共通する上流の病態
- 5つの火種: SASP(ゾンビ細胞)、NLRP3インフラマソーム、腸内細菌叢ディスバイオシス、免疫老化、ミトコンドリア機能不全が相互に増幅
- 対策の根拠: CANTOS試験がIL-1β阻害の有効性を証明。運動・地中海食・睡眠改善も同等の抗炎症効果を示すエビデンスあり
- 判断に迷ったら: かかりつけ医にhs-CRPの測定を依頼し、自分のInflammaging度を客観的に把握する
