はじめに:「治らない病気」が「治療できる病気」に変わる瞬間
「アルツハイマー病に効く薬はない」——長らく、医療者も患者家族も、そう信じるしかありませんでした。過去 20 年間に 100 以上の治療薬候補が臨床試験で失敗し、「アミロイド仮説そのものが間違っているのではないか」という疑念すら広がっていたのです。
しかし 2023 年、その風景は一変しました。抗アミロイド抗体薬レカネマブ(レケンビ)が米国 FDA のフル承認を取得し、同年 12 月には日本でも保険適用が開始。2024 年にはドナネマブ(キスンラ)も FDA 承認を受け、アルツハイマー病治療は「対症療法の時代」から「疾患修飾療法の時代」へと、パラダイムシフトを遂げつつあります。
本記事では、これらの新薬の臨床エビデンスを数値で読み解きながら、安全性の課題、血液バイオマーカーがもたらす診断革命、日本での治療アクセスの現状、そして「その効果は本当に意味があるのか」という批判的視点まで、医師の立場から包括的に解説します。
アミロイドカスケード仮説:敵を知る
脳に沈着する「ゴミ」の正体
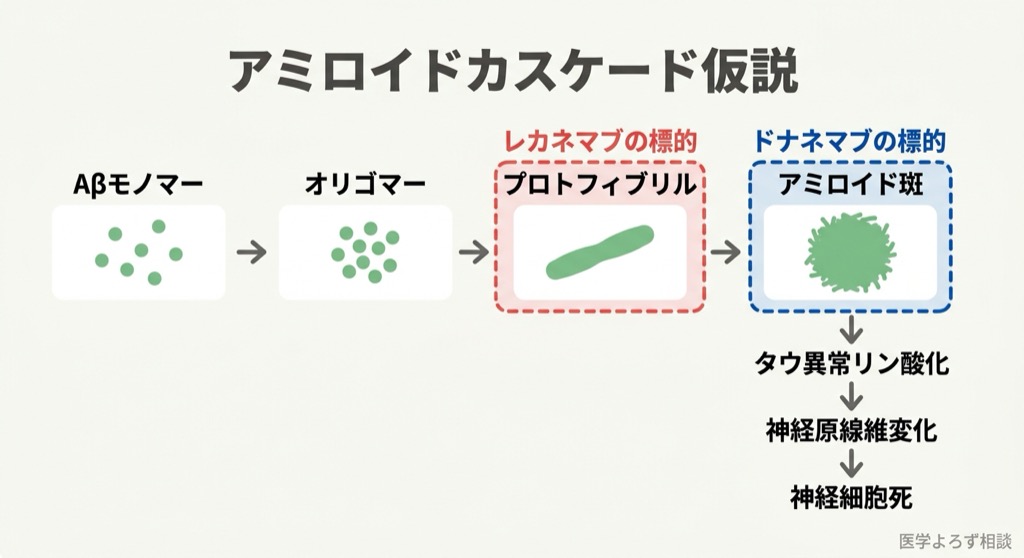
アルツハイマー病の脳では、アミロイドβ(Aβ)と呼ばれるタンパク質が異常に蓄積します。正常な脳でも Aβ は産生されますが、通常は分解・除去されます。遺伝的要因や加齢などにより、この除去機能が低下すると、Aβ が「モノマー → オリゴマー → プロトフィブリル → フィブリル → アミロイド斑」と段階的に凝集していきます。
このうち、とくに神経毒性が強いとされるのが プロトフィブリル(可溶性の中間凝集体)です。プロトフィブリルはシナプス周囲に集積し、シナプス伝達を阻害し、神経炎症を誘発します。その下流で タウタンパク質の異常リン酸化 が進行し、神経原線維変化(NFT)を形成。最終的に神経細胞死に至る——これがアミロイドカスケード仮説の骨格です。
なぜ今まで薬が効かなかったのか
過去の抗アミロイド薬が失敗した主な理由は 3 つあります。第一に、すでに認知症が進行した患者を対象としていたこと( = 手遅れ)。第二に、アミロイドの「正しい形態」を標的にできていなかったこと。第三に、効果を検証するのに十分な期間と規模の試験が行われなかったこと。レカネマブとドナネマブは、これらの教訓を踏まえて設計された第三世代の抗体薬です。
レカネマブ:Clarity AD 試験の全貌
試験デザインと主要結果
Clarity AD は、エーザイとバイオジェンが共同で実施した第 3 相ランダム化二重盲検プラセボ対照試験です [1]。早期アルツハイマー病(MCI または軽度認知症で、アミロイド PET 陽性)の患者 1,795 名を対象に、レカネマブ 10 mg/kg を 2 週間ごとに 18 カ月間静注しました。
主要評価項目である CDR-SB(Clinical Dementia Rating-Sum of Boxes) のベースラインからの変化量は、レカネマブ群 1.21 対プラセボ群 1.66 で、差は −0.45 ポイント(27% の進行抑制、p < 0.001) でした [1]。CDR-SB は認知機能と日常生活動作を 6 領域(記憶、見当識、判断力、社会活動、家庭・趣味、身の回り)で評価する尺度で、0.5〜1.0 ポイントの変化が臨床的に意味のある最小差(MCID)とされています。
副次評価項目でも一貫した効果が示されました。ADAS-Cog14(認知機能スケール)で 26% の減速、ADCOMS で 24% の減速、ADCS-MCI-ADL(日常生活動作)で 37% の減速。いずれもプラセボに対して統計的に有意でした。
アミロイドへのインパクト
PET 画像解析では、レカネマブ群のアミロイド量が劇的に減少しました。ベースラインのアミロイド PET 値(Centiloid 換算)は約 77 CL でしたが、18 カ月後には約 −55 CL の減少を示し、多くの患者がアミロイド陰性の閾値を下回りました。さらに、アミロイド除去量と CDR-SB 改善度には用量反応関係が認められています [9]。
36 カ月延長試験:早期介入の意味
Clarity AD のオープンラベル延長試験(OLE)では、当初レカネマブを投与されていた「早期開始群」と、プラセボから切り替えた「遅延開始群」が 36 カ月時点で比較されました [2]。結果として、早期開始群は遅延開始群に対して認知機能の優位性を維持しており、アミロイド除去も持続していました。この「遅延開始試験デザイン」は、レカネマブの効果が単なる対症的なものではなく、疾患の自然経過そのものを修飾する——すなわち真の disease-modifying 効果を持つことを示唆する重要なエビデンスです。

ドナネマブ:TRAILBLAZER-ALZ 2 試験
レカネマブとの違い
ドナネマブ(イーライリリー社)はレカネマブとは異なるメカニズムで作用します。レカネマブが可溶性のプロトフィブリルを主な標的とするのに対し、ドナネマブは アミロイド斑に沈着した N 末端ピログルタミン酸化 Aβ(N3pG-Aβ) を標的とします。つまり、すでに脳に蓄積した「古い」アミロイドを集中的に除去する戦略です。
TRAILBLAZER-ALZ 2 の結果
TRAILBLAZER-ALZ 2 は 1,736 名の早期アルツハイマー病患者を対象とした第 3 相 RCT です [3]。特徴的なのは、タウ PET による層別化が行われた点です。
タウ低〜中等度群(全体の約 69%):
- iADRS(統合 AD 評価スケール): +3.25 ポイント(35% の進行抑制)
- CDR-SB: −0.67 ポイント(36% の進行抑制)
全体集団:
- iADRS: +2.92 ポイント(22% の進行抑制)
- CDR-SB: −0.70 ポイント(29% の進行抑制)
さらに、ドナネマブには「投与完了」の概念があります。アミロイド PET でアミロイドが十分に除去された患者はプラセボに切り替えられました。76 週時点で、ドナネマブ群の約 47% がこの基準を満たし、治療を完了しています。
延長試験から見えたこと
ドナネマブの OLE データでは、遅延開始群もアミロイド除去を達成できたものの、早期開始群は認知機能面での優位性を維持していました [4]。レカネマブと同様に、「早く始めるほど良い」というメッセージは一貫しています。
二大抗体薬の比較:ネットワークメタアナリシスから
直接比較はないが、間接比較は可能
レカネマブとドナネマブの直接比較試験(head-to-head RCT)は実施されていません。しかし、抗アミロイド免疫療法全体を対象としたネットワークメタアナリシスでは、ドナネマブとレカネマブが CDR-SB に対する効果で最も優れた抗体薬 として評価されています [8]。
両薬を多面的に比較すると、以下のようになります。
| 項目 | レカネマブ | ドナネマブ |
|---|---|---|
| 標的 | プロトフィブリル(可溶性) | N3pG-Aβ(沈着型) |
| 投与 | 2 週間ごと静注(継続) | 4 週間ごと静注(完了可能) |
| CDR-SB 進行抑制 | 27% | 29〜36%(タウ層別で変動) |
| ARIA-E 発生率 | 12.6% | 24.0% |
| 治療関連死亡 | 報告なし(Phase 3) | 3 例 |
| FDA 承認 | 2023 年(フル承認) | 2024 年 |
| 日本保険適用 | 2023 年 12 月〜 | 未定(2026 年 4 月時点) |

ARIA:治療効果の裏にある安全性の課題
ARIA とは何か
ARIA(Amyloid-Related Imaging Abnormalities)は、抗アミロイド抗体薬に特有の副作用です。大きく 2 種類に分けられます。
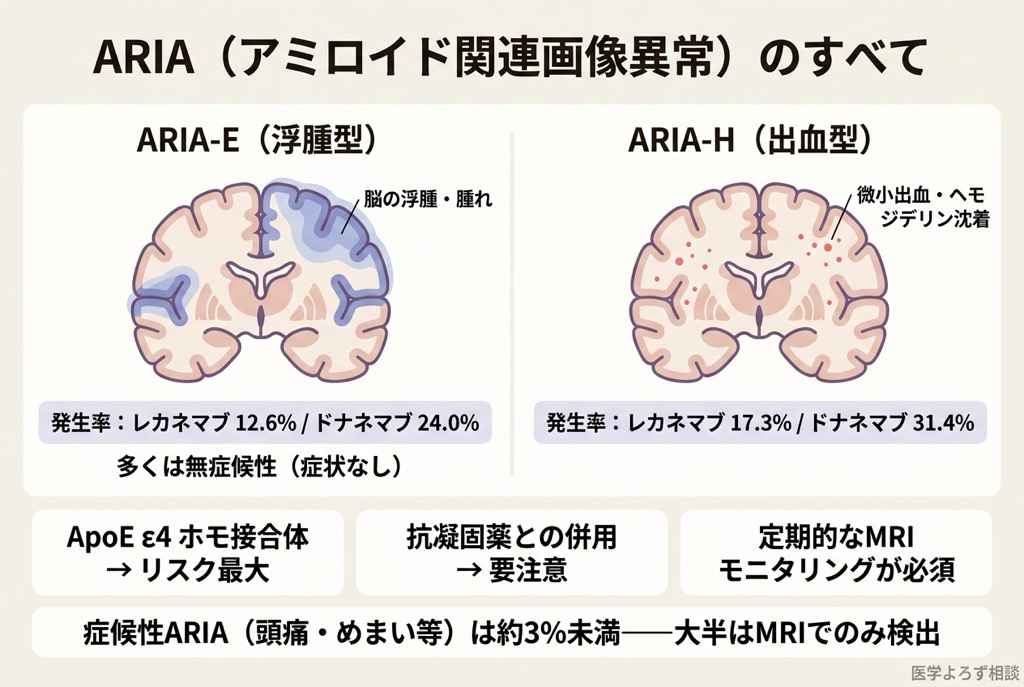
- ARIA-E(浮腫型): 脳実質や脳溝に一過性の浮腫が出現。MRI の FLAIR 画像で高信号として検出される。多くは無症候性だが、頭痛・混乱・視覚障害などの症状を呈することもある。
- ARIA-H(出血型): 微小出血(microbleed)や脳表ヘモジデリン沈着(superficial siderosis)として出現。
ARIA の発生メカニズムは完全には解明されていませんが、抗体がアミロイドを除去する過程で血管壁のアミロイド(脳アミロイド血管症: CAA)も攻撃し、血管透過性が亢進することが一因と考えられています。
臨床試験での発生率
Clarity AD(レカネマブ)では ARIA-E が 12.6%、ARIA-H が 17.3% に認められました [1]。一方、TRAILBLAZER-ALZ 2(ドナネマブ)では ARIA-E が 24.0%(うち症候性 6.1%)と約 2 倍。さらに、ドナネマブ群では治療関連死亡が 3 例 報告されています [3]。
ARIA のリスクは ApoE ε4 の保有状態と強く相関します。特に ε4 ホモ接合体(ε4/ε4)ではリスクが顕著に高まります [7]。ただし、レカネマブの ε4 ホモ接合体を対象としたサブ解析では、ARIA リスクが高いにもかかわらず認知機能への治療効果は保たれていたことが示されています [13]。
リアルワールドデータ:日本からの報告
東京都健康長寿医療センターの 120 名の日本人患者を対象としたリアルワールドデータ [5] は、実臨床での安全性を示す貴重な資料です。
- 全 ARIA: 20%(ARIA-E 4%、孤立性 ARIA-H 16%)
- 症候性 ARIA: 0%
- 投与中止: 16%(主に疾患進行による)
注目すべきは、RCT と比較して ARIA-E の発生率が明らかに低い点です。これはシステマティックレビュー/メタアナリシスでも確認されており、リアルワールドエビデンス(RWE)では RCT よりもやや低い ARIA-E 発生率が報告されています [6]。適切な患者選択と定期的な MRI モニタリングにより、ARIA は管理可能であることが示唆されます。
血液バイオマーカー革命:p-tau217 が変える診断の風景
なぜ血液検査が「革命」なのか
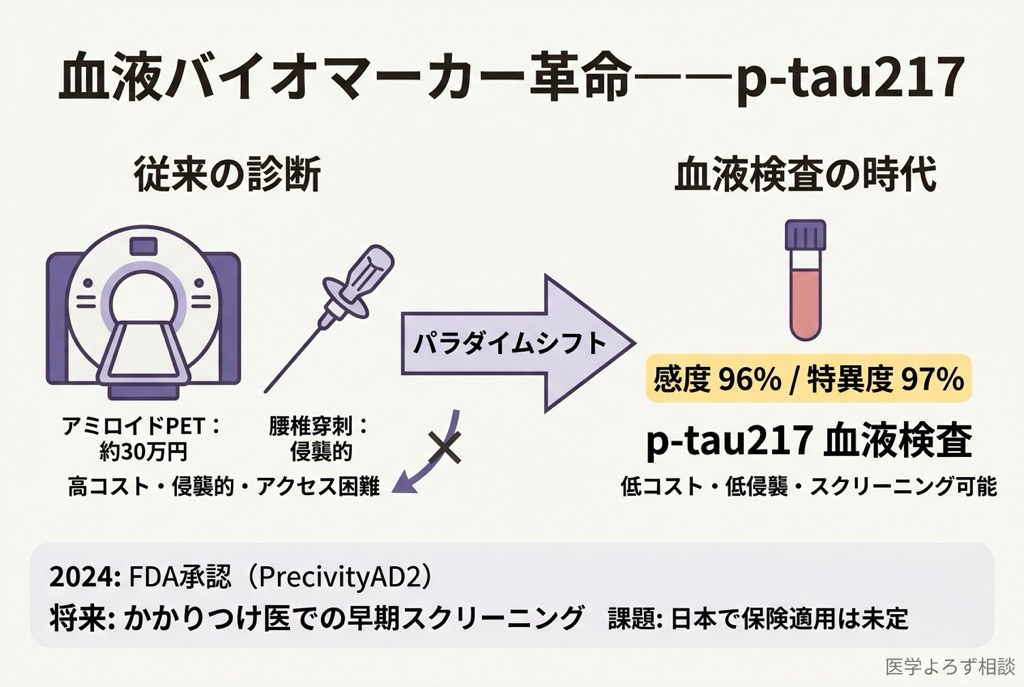
アルツハイマー病の確定診断には、これまでアミロイド PET(1 回 30〜50 万円)または腰椎穿刺による脳脊髄液(CSF)検査が必要でした。高額で侵襲的なこれらの検査は、大規模スクリーニングには不向きです。
ところが近年、血漿 p-tau217(リン酸化タウ 217) が画期的な血液バイオマーカーとして急速に臨床実装されつつあります。p-tau217 はアミロイド PET と 90% 以上の一致率を示し、採血だけでアルツハイマー病の病理学的診断が可能になりつつあります。
Mayo Clinic のデータが示す地殻変動
Mayo Clinic からの報告 [11] は、この変化のスピードを如実に示しています。抗アミロイド療法が実臨床に導入されて以降、血漿 p-tau217 の検査オーダーは四半期あたり +238% 増加。一方で、従来の CSF 検査オーダーは減少傾向にあります。診断ワークフローそのものが、「侵襲的な検査から非侵襲的な血液検査へ」と劇的にシフトしているのです。
この変化は単なる利便性の向上にとどまりません。血液検査によるスクリーニングが普及すれば、アルツハイマー病の「早期発見 → 早期治療介入」という理想的なパスウェイが初めて現実的になります。レカネマブの OLE データが示すように、「早く始めるほど効果が大きい」以上、診断のボトルネック解消は治療効果の最大化に直結します。
日本の治療アクセス:保険適用・ガイドライン・現場の実際
保険適用と費用
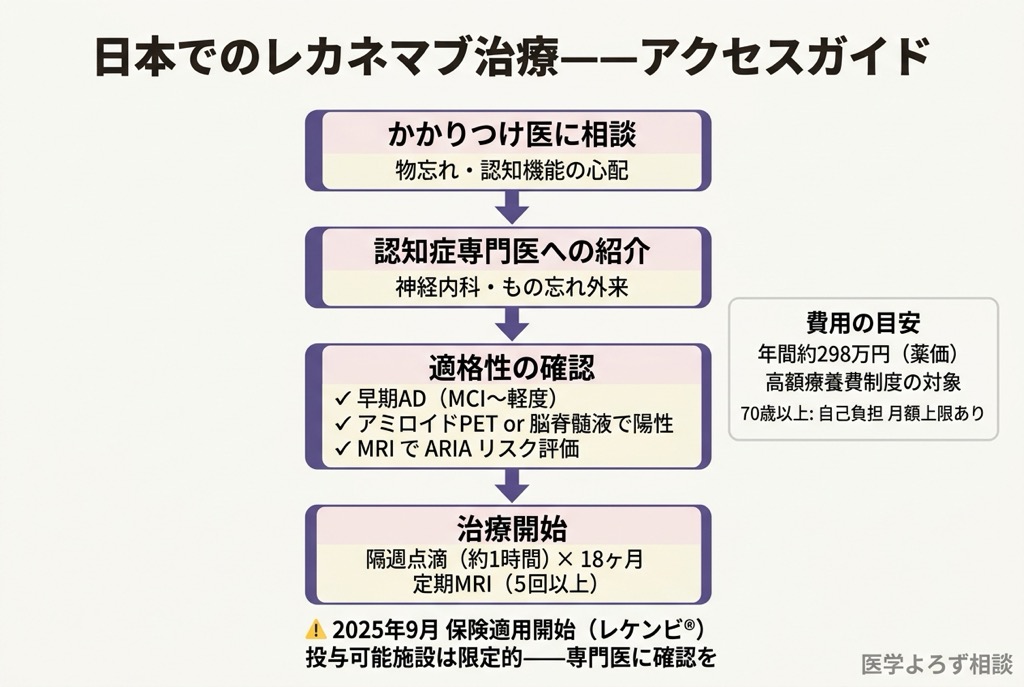
レカネマブは 2023 年 12 月に日本で保険適用となりました。薬価は体重 50 kg の患者で年間約 298 万円ですが、高額療養費制度の適用により、自己負担は所得に応じて月額 5〜25 万円程度に抑えられます。ただし、投与前後の MRI モニタリング費用やアミロイド PET 検査費用が別途必要です。
適正使用ガイドライン
厚生労働省は 2023 年 12 月に レカネマブ適正使用ガイドライン を策定しました [14]。主な要件は以下の通りです。
- 対象: 早期アルツハイマー病(MCI〜軽度認知症)でアミロイド陽性が確認された患者
- 施設要件: 認知症専門医、MRI 管理体制、ARIA 管理体制を有する施設
- モニタリング: 投与開始後 14 週間は定期 MRI を実施
- 禁忌: 抗凝固薬使用中、重度 CAA、5 個以上の微小出血
日本認知症学会は 2023 年 9 月に バイオマーカーガイドライン第 2 版 を公開し、アミロイド PET・CSF・血液バイオマーカーの使い分けを整理しています [15]。
治療アクセスの課題
実臨床での最大の障壁は、「適格患者の同定」です。認知症の中でアルツハイマー病は約 60〜70% を占めますが、その中で「早期」段階の患者を適時に拾い上げ、アミロイド陽性を確認し、施設要件を満たす医療機関につなげるまでのパスウェイは、まだ十分に整備されていません。特に地方では専門施設へのアクセスが限られ、都市部との治療格差が懸念されています。
批判的視点:この効果は本当に「意味がある」のか
MCID 論争
EMA(欧州医薬品庁)は 2026 年にレカネマブとドナネマブの双方を承認しましたが、「臨床的意義」については議論が続いています [10]。CDR-SB で 0.45 ポイントの差は、18 カ月間の試験としては統計的に有意ですが、一般的に MCID とされる 0.5〜1.0 ポイントを下回っています。
批判的な論説 [12] では、以下の懸念が指摘されています。
- 効果が MCID に達していない可能性: 患者や介護者が実感できるレベルの差ではない可能性
- 脳体積減少: レカネマブ群でプラセボ群よりも脳体積の減少が大きい(「偽萎縮」と解釈されることが多いが、長期的影響は不明)
- 方法論的懸念: CDR-SB の評価者盲検の維持が困難(ARIA の発生により割付けが推測される)
- コスト対効果: 年間約 300 万円のコストに見合うベネフィットか
反論と文脈
一方で、擁護側からはいくつかの反論があります。第一に、進行抑制率(27〜36%)は他の神経変性疾患の疾患修飾療法と比較して遜色ない水準です。第二に、OLE の遅延開始試験で持続的な効果が示されていることは、蓄積する利益が長期では MCID を超える可能性を示唆します。第三に、治療の「意味」は個人レベルで異なり、半年でも自立生活を延長できれば、本人・家族にとっては大きな意味を持ちます。
また、ApoE ε4 の保有状態、年齢、タウ病理の程度によって有効性と安全性が異なることがシステマティックレビューで明らかになっており [7]、今後は「誰に、いつ投与すべきか」を精密に決定する個別化医療が鍵となります。
わかっていること・まだわからないこと
わかっていること(Known)
- レカネマブは 18 カ月で CDR-SB を 27% 減速させ、統計的に有意である [1]
- ドナネマブはタウ低〜中等度患者で CDR-SB を 36% 減速させる [3]
- 早期開始群は 36 カ月後も遅延開始群に対し認知機能の優位性を維持する [2][4]
- アミロイド除去量と認知機能改善には用量反応関係がある [9]
- ARIA は定期 MRI モニタリングで管理可能であり、RWE では RCT より低率である [5][6]
- 血漿 p-tau217 は診断ワークフローを変革しつつある [11]
- ApoE ε4 ホモ接合体でも治療効果は保たれる(ARIA リスクは高い)[13]
- ネットワークメタアナリシスで両薬は最も有効な抗アミロイド抗体薬と評価されている [8]
- EU は 2026 年に両薬を承認したが、ARIA 管理を条件としている [10]
まだわからないこと(Unknown)
- 5 年、10 年の長期有効性と安全性
- 脳体積減少(偽萎縮)の長期的な臨床的意味
- 最適な投与期間(いつ中止できるか、中止後のリバウンド)
- ドナネマブの「治療完了」後の再発率と再治療の必要性
- 血液バイオマーカー単独で治療適応を判断できる段階に達しているか
- MCI 以前の前臨床期(プレクリニカル AD)への介入効果
- 他の病態(タウ、炎症、シナプス障害)を標的とする併用療法の可能性
- 日本の地方部での治療アクセス格差の解消策
- 異なる民族・遺伝的背景における有効性の差
ご家族のための実践チェックリスト
以下は、ご家族や患者さんが「新しい治療」を正しく理解し、適切に行動するためのチェックリストです。
Step 1:まず確認すべきこと
- もの忘れの自覚がある場合、まず「もの忘れ外来」を受診する
- 認知症専門医による正確な診断を受ける(アルツハイマー病かどうかの鑑別)
- 現在の認知機能の段階を確認する(MCI・軽度・中等度・重度)
Step 2:治療の適格性を確認する
- アミロイド PET または CSF 検査でアミロイド陽性が確認されているか
- 血漿 p-tau217 検査が利用可能な施設か確認する
- MCI〜軽度認知症の段階か(中等度以降は現時点で適応外)
- 抗凝固薬の使用や脳微小出血の有無を確認する
Step 3:治療のリスクとベネフィットを理解する
- CDR-SB 27〜36% 減速の意味を主治医と確認する
- ARIA のリスクと MRI モニタリングの必要性を理解する
- 年間のコスト(高額療養費制度適用後の自己負担)を確認する
- 2 週間ごとの通院(点滴)が継続可能か
Step 4:治療以外にできること
- 運動習慣の維持(中等度の有酸素運動、週 150 分以上)
- 血圧・糖尿病・脂質異常症の管理(修正可能な危険因子)
- 社会的つながりと知的活動の維持
- 介護保険の申請・サービスの活用を検討する
おわりに:「治る」わけではない、でも「変わった」
レカネマブとドナネマブは、アルツハイマー病を「治す」薬ではありません。27〜36% の進行抑制という効果は、人生を劇的に変えるほどのものではないかもしれません。MCID に達していないという批判は正当であり、私たちはこの数字の意味を冷静に見つめる必要があります。
しかし、歴史的な文脈で見れば、この一歩は小さくありません。100 以上の薬剤が失敗した後に、初めて Phase 3 RCT で有意な進行抑制を示した疾患修飾薬が 2 つも誕生したこと。血液バイオマーカーにより、脳の病理を採血で推定できるようになりつつあること。「早く始めるほど効果がある」というエビデンスが、早期発見の意味を根本から変えたこと。
次の 10 年で、タウを標的とする抗体薬、抗炎症薬、シナプス保護薬との併用療法が登場するでしょう。アミロイド除去はその出発点に過ぎません。
もし、ご自身やご家族の「もの忘れ」が気になったら——まずは、かかりつけ医に相談してください。早期に見つけることが、将来の選択肢を最大化する、今できる最善の行動です。
関連記事:
