はじめに:「16時間断食」は本当に長寿の鍵なのか
「16:8ダイエット」「オートファジー断食」——SNSを開けば、間欠的断食(Intermittent Fasting: IF)の成功体験が溢れています。
しかし2024年、アメリカ心臓協会の学術集会で衝撃的なデータが発表されました。NHANESデータベースの大規模解析で、1日の食事時間を8時間以内に制限している人は、心血管死亡リスクが91%高いという結果が報告されたのです [5]。
「断食は健康にいい」と「断食は死亡リスクを高める」——一見矛盾する2つの結論。いったいどちらが正しいのでしょうか。
この記事では、130のRCTを統合したアンブレラレビューから、ヒトで初めて「老化のペース」の減速を実証したCALERIE試験まで、15件のエビデンスに基づいて間欠的断食の真実に迫ります。結論から言えば、「何時間」よりも「何を・いつ・誰が」の方がはるかに重要です。
間欠的断食とは何か——3つの方式
間欠的断食は、食べる「量」ではなく「タイミング」を制限する食事法です。主に3つの方式があります [11]。
1. 時間制限食(Time-Restricted Eating: TRE)
1日の食事を特定の時間帯(通常8〜12時間)に限定する方法です。最も有名な「16:8」は、16時間断食して8時間の食事ウィンドウを設ける方式。朝食を抜く「遅い型」と夕食を早める「早い型」があります。
2. 隔日断食(Alternate-Day Fasting: ADF)
断食日(0〜500kcal)と自由摂食日を交互に繰り返します。最も研究データが多い方式ですが、日常生活での実践は難しく、アドヒアランスが課題です [11]。
3. 5:2ダイエット
週5日は通常食、2日(非連続)を低カロリー(500〜600kcal)にする方式。ADFより緩やかで、ヨーロッパの肥満学会(EASO)もMNT(Medical Nutrition Therapy)の選択肢として言及しています [5]。

130のRCTが示した「効果」と「限界」
2021年、JAMA Network Openに掲載されたPatikornらのアンブレラレビューは、IFに関する11のメタアナリシス(130のRCT)を統合した最もメタレベルの高い解析です [1]。
結果は明確でした:
有意に改善が認められた指標(27%):
- BMI・体重・脂肪量
- LDLコレステロール・総コレステロール・中性脂肪
- 空腹時血糖・空腹時インスリン・HOMA-IR(インスリン抵抗性)
- 血圧
しかし、冷静に読み解くべきポイントもあります:
- エビデンスの質はGRADE基準で「中〜低」。つまり、今後の研究で結論が変わる可能性がある
- 試験の中央値は参加者38名、追跡期間3ヶ月。長期データが圧倒的に不足
- 除脂肪体重(筋肉量)の減少も確認された——これは特に高齢者にとって重大なリスク
2024年のYaoらのメタアナリシスは、IFと通常のカロリー制限(CR)を直接比較し、脂肪減少効果が「同等」であることを示しました [2]。つまりIFは「魔法の食事法」ではなく、カロリー制限を実践しやすくするための「仕組み」として理解するのが科学的に正確です。

なぜ「食べない時間」が体を変えるのか——4つの分子メカニズム
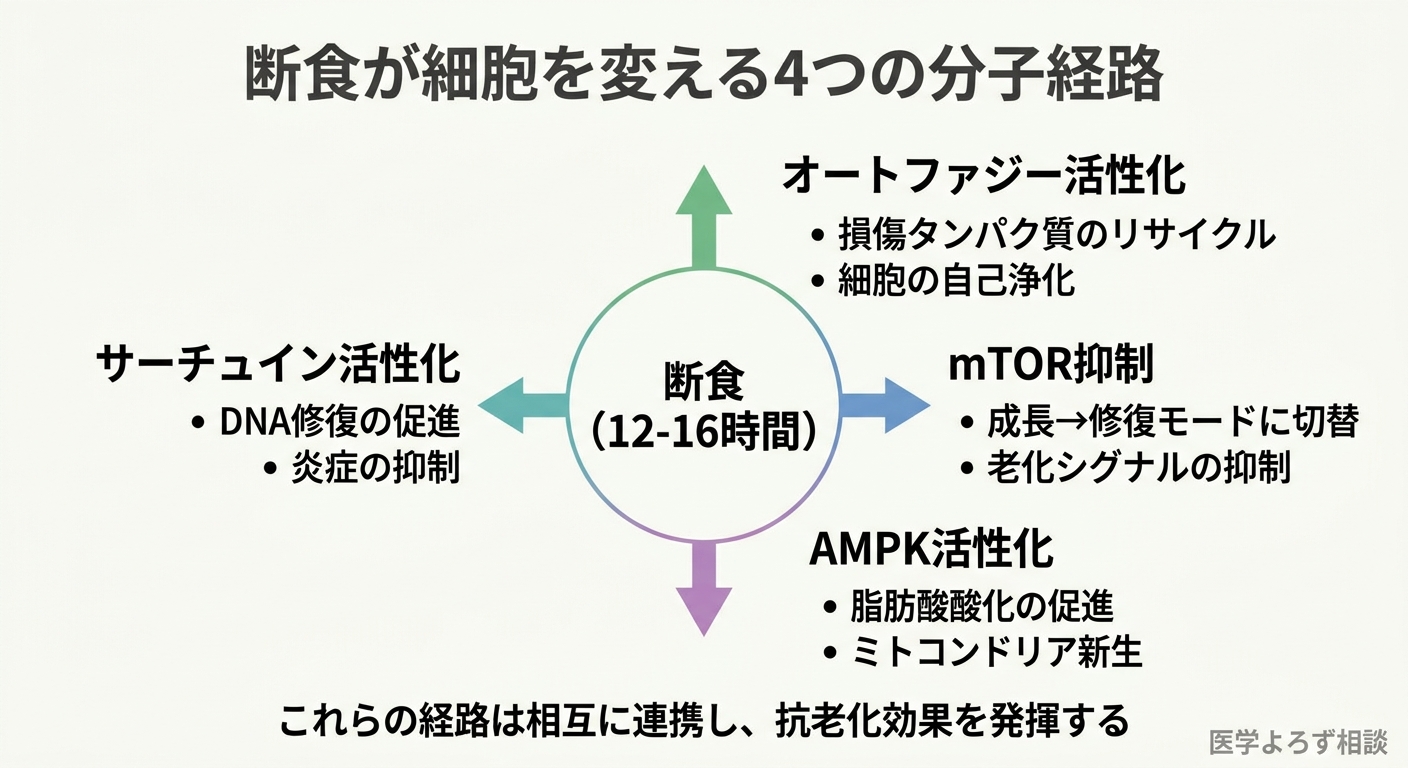
IFの効果は単なるカロリー制限では説明できません。「食べない時間」そのものが分子レベルで以下の変化を引き起こします [10]。
1. オートファジー(自食作用)の活性化
栄養が枯渇すると、細胞は損傷したタンパク質やミトコンドリアを「自分で食べて」リサイクルする仕組みが活性化します。これがオートファジーです。2016年にノーベル医学生理学賞を受賞した大隅良典教授の発見により、その分子メカニズムが解明されました。
ヒトでは、断食開始から約12〜16時間後にオートファジーが有意に活性化するとされています。ただし、ヒトでのオートファジー活性を直接測定した大規模研究はまだ限られています [10]。
2. mTOR経路の抑制
mTOR(mammalian Target of Rapamycin)は「成長と老化のマスタースイッチ」です。栄養豊富な状態ではmTORが活性化し、細胞の成長を促進する一方で老化も加速します。断食はmTORを抑制し、細胞の修復モードに切り替えます。
3. AMPK経路の活性化
AMPKはエネルギーセンサーとして機能する酵素で、断食によって活性化されます。脂肪酸酸化の促進、ミトコンドリア新生、炎症の抑制など、多面的な抗老化効果を発揮します。
4. サーチュイン経路の活性化
NAD+依存性の脱アセチル化酵素であるサーチュイン(特にSIRT1)は、断食時に活性化し、DNA修復・炎症抑制・代謝調節に寄与します。
CALERIE試験——ヒトで「老化のペース」は遅くなるか
間欠的断食の議論で避けて通れないのが、カロリー制限(CR)の大規模ヒトRCTであるCALERIE試験です。
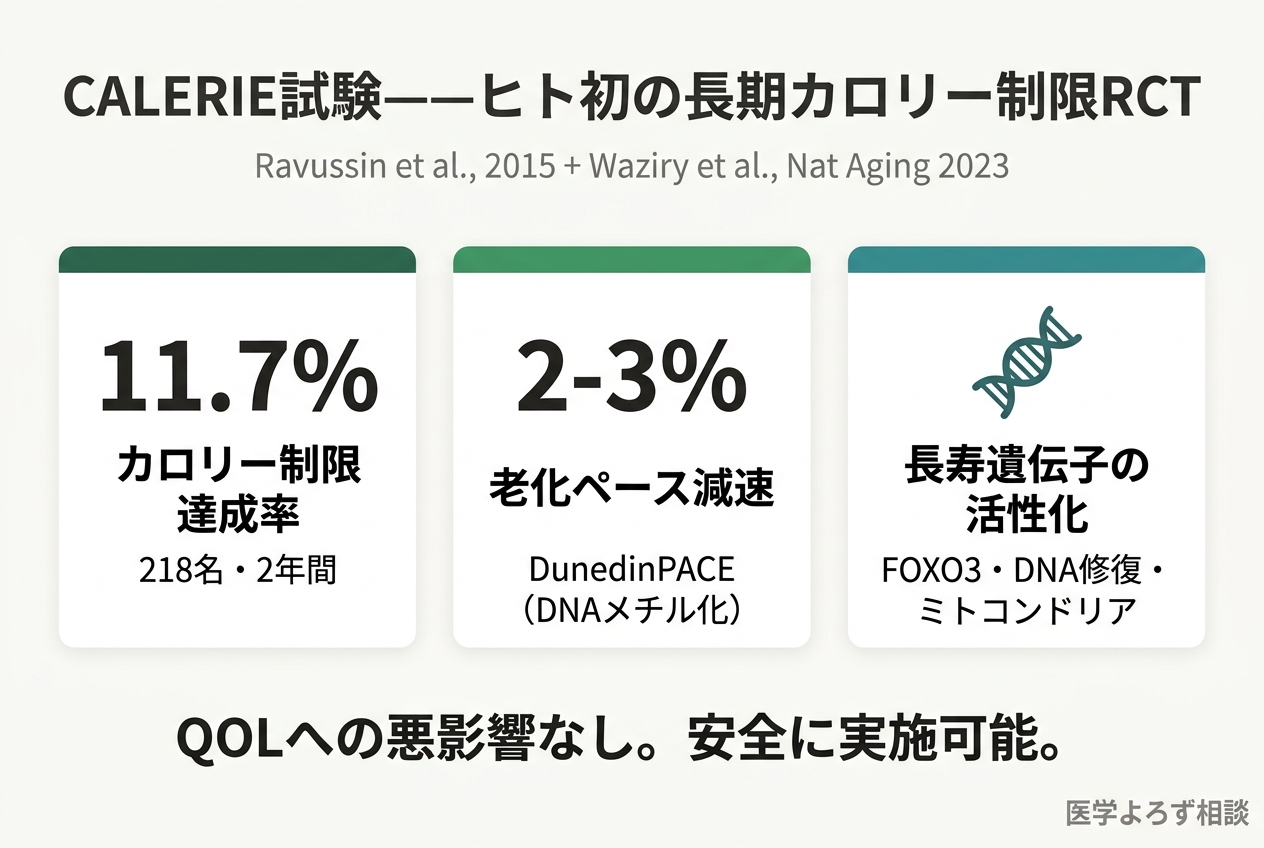
CALERIE Phase 2は、218名の非肥満健常者(21〜51歳)を対象に、25%のカロリー制限を2年間実施した世界初の長期RCTです [7]。結果、参加者は平均11.7%のCRを達成し、以下が確認されました:
- T3(甲状腺ホルモン)の有意な低下(代謝率の適応的低下)
- TNF-α(炎症マーカー)の低下
- 心代謝リスク因子の改善
- QOL(生活の質)への悪影響なし
さらに2023年、Nature Aging誌に掲載されたCALERIE試験の二次解析では、2年間のCRがDunedinPACE(DNAメチル化で測定する「老化のペース」)を有意に減速させることが示されました [8]。これはヒトのRCTで「老化のペースを遅くできる」ことを初めて実証した画期的なデータです。
ただし、PhenoAge・GrimAgeなどの他のエピジェネティック時計では有意差が得られず、効果サイズは小さいものでした。研究者らは「わずかな老化ペースの減速でも、集団レベルでは大きな健康効果をもたらしうる」と結論しています。
同じCALERIE試験の筋肉遺伝子発現解析では、CRがプロテオスタシス(タンパク質恒常性)、DNA修復、ミトコンドリア生合成、FOXO3代謝に関連する遺伝子の発現を改善することも示されています [9]。
「8時間制限食で死亡リスク91%増」の真相
2024年に報告されたNHANES解析(約2万人)の「8時間制限食で心血管死亡リスク91%増」という結果は、大きな波紋を呼びました [5]。
しかし、この研究を正しく理解するには、いくつかの重要な留意点があります:
- 観察研究であり、因果関係の証明ではない
- 食事時間は2日間の食事記録のみで評価——日常的に8時間制限食をしていたとは限らない
- 朝食欠食が含まれる可能性が高い——朝食欠食は独立した死亡リスク因子として知られている
- 交絡因子(社会経済的状況、生活習慣など)の完全な除外は不可能
Wangらの2024年のメタアナリシスでは、肥満者における朝食欠食が全死亡リスク・CVD死亡リスクと関連することが確認されています [5]。つまり、「8時間制限食」の問題は「断食」そのものではなく、「朝食を抜くことによるリスク」が紛れ込んでいる可能性が高いのです。
Cochraneの2021年のシステマティックレビューも、IFによる心血管疾患予防のエビデンスは「不十分」と判定しています [4]。RCTの追跡期間が短すぎて、死亡率や心血管イベントへの影響を評価できる段階ではないのが実情です。
科学の現在地:わかっていること、いないこと
確立された知見:
- IFはBMI・体重・脂肪量・血糖・脂質・血圧を改善する(130 RCTsのアンブレラレビュー)[1]
- この効果はカロリー制限と「同等」であり、IFはCRの実践手段の一つ [2]
- 2年間のCR(11.7%)はヒトの老化ペースを遅くする(CALERIE/DunedinPACE)[8]
- CRは長寿関連遺伝子(FOXO3、DNA修復、ミトコンドリア生合成)を活性化する [9]
- IF/CRは心代謝リスク因子を改善し、安全に実施可能(QOLへの悪影響なし)[7]
未解明点・現在の限界:
- IFの「最適な時間帯」のエビデンスは不十分(早い食事時間帯の方が有利な可能性はあるが、RCTでの直接比較は少ない)
- IFの長期(5年以上)の安全性データがない
- IFとCRの長寿効果の比較はヒトでは未検証
- 高齢者・糖尿病患者・摂食障害リスクのある人でのIFの安全性データが不足 [3]
- 除脂肪体重(筋肉量)の減少——特に高齢者ではサルコペニアリスクに直結
- 「8時間制限食と死亡リスク上昇」は因果関係が確立されていない観察研究
実践ガイド:エビデンスに基づく間欠的断食の始め方
| 項目 | 推奨 | エビデンスレベル |
|---|---|---|
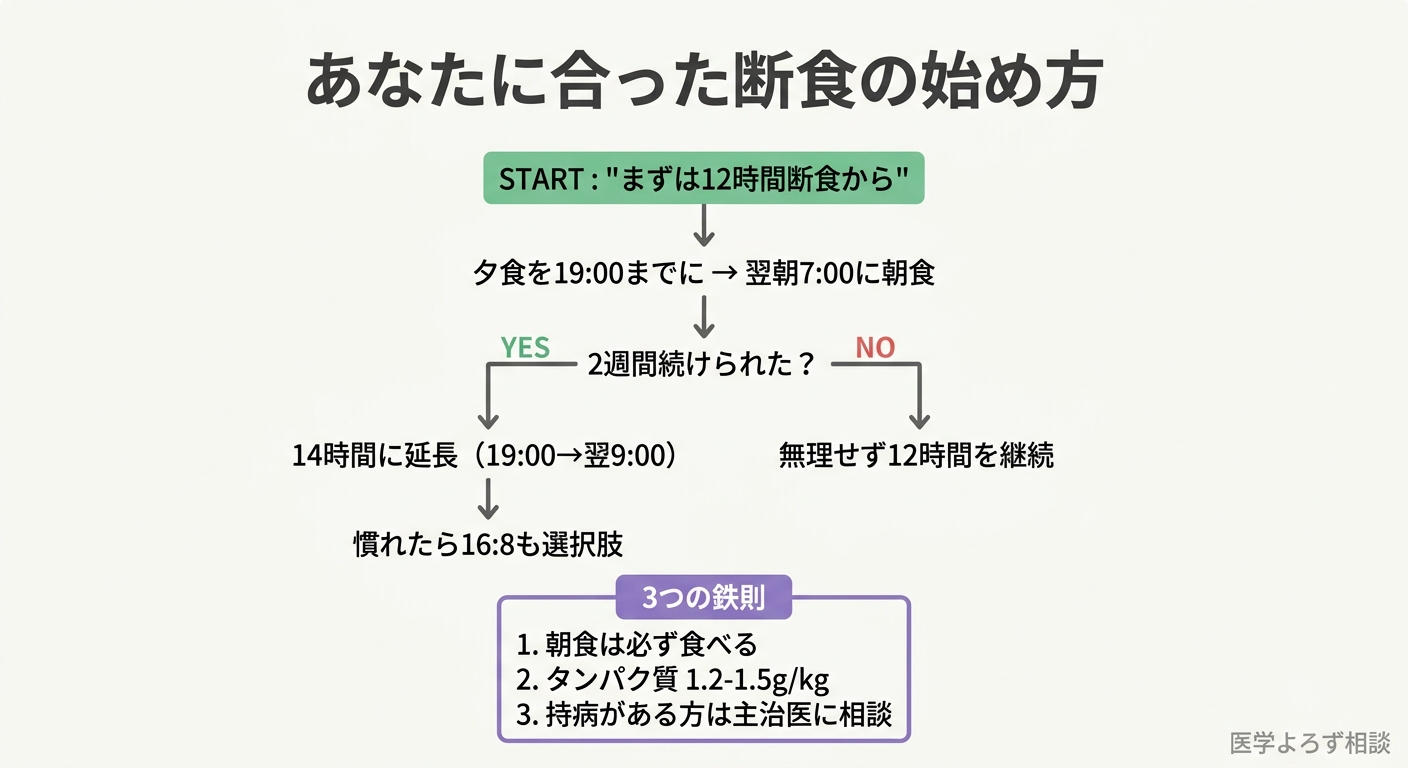
| 方式 | 12〜14時間断食(初心者)→ 慣れたら16時間 | Review [11] |
| 食事時間帯 | 朝〜夕方(早い時間帯)を優先 | 観察研究 [5] |
| 朝食 | スキップしない(朝食欠食は独立したリスク因子) | MA [5] |
| タンパク質 | 体重1kgあたり1.2〜1.5g(筋肉量維持) | Umbrella Review [1] |
| 運動 | レジスタンストレーニング併用(筋肉量維持に必須) | Review [3] |
| 水分 | 断食時間中も水・お茶・コーヒー(無糖)はOK | Review [11] |
| 避けるべき人 | 摂食障害歴・妊婦・授乳中・1型糖尿病・低体重(BMI<18.5) | Review [3] |
| 主治医相談 | 糖尿病治療中・降圧薬服用中は必ず主治医に相談 | GL [5] |
おわりに:「何時間」より大切なこと
間欠的断食の研究を追いかけて確信したことがあります。
「16時間断食」や「5:2」の数字は、メディアが作り出した「答え」です。しかし、科学が教えてくれるのは、もっとシンプルな原則——「食べすぎない」「食べない時間を作る」「朝に食べて夜は軽く」——これだけです。
CALERIE試験が示したのは、わずか11.7%のカロリー制限でも老化のペースが遅くなるということ。毎日のご飯を少し減らし、夜遅い食事を控える。それだけで十分なのかもしれません。
派手な断食法を追い求める前に、まず「自分は夕食後に何を食べているか」を振り返ってみてください。そこに答えがあることが多いものです。
本日のまとめ
- 間欠的断食の本質: カロリー制限を実践しやすくする「仕組み」。魔法の食事法ではない
- 最新のエビデンス: 130 RCTsで代謝改善は確認。ただしGRADE基準は中〜低。長期データ不足
- 今日からできること: 12時間断食(夕食後〜翌朝)から始める。朝食は抜かない。タンパク質を意識する
関連記事:
