はじめに:あなたの細胞には37兆個の「発電所」がある
あなたの体を構成する約37兆個の細胞。そのひとつひとつの中に、数百から数千もの小さな「発電所」が存在しています。
ミトコンドリア。
細胞が必要とするエネルギー(ATP)の約90%を生み出す、生命維持の根幹を担うオルガネラ(細胞小器官)です[9]。心筋細胞には約5,000個、肝細胞には約2,000個——エネルギー需要の高い臓器ほど、ミトコンドリアが密集しています。
では、この発電所が壊れたらどうなるか。
心臓手術中の虚血再灌流障害。脳卒中後の神経細胞死。パーキンソン病における黒質ドーパミンニューロンの変性。ミトコンドリアの機能不全は、これらすべての病態の根底に存在しています[9]。従来の治療は「壊れた発電所を修理する」アプローチでしたが、損傷が重度の場合、修理では追いつきません。
ならば、「新しい発電所を外から届ける」ことはできないだろうか。
この大胆な発想が、2013年にボストン小児病院の研究チームによって現実のものとなりました[1]。そして2026年現在、ミトコンドリア移植は心臓外科の臨床から神経変性疾患、腎臓病、さらには自己免疫疾患へと、その可能性を急速に広げています。
この記事では、ミトコンドリア移植の科学——なぜ他人のオルガネラが自分の細胞に受け入れられるのか、臨床でどのような成果が出ているのか、そして2026年に何が変わったのかを、最新のエビデンスに基づいて解説します。
20億年前の共生者——ミトコンドリアという不思議な存在
ミトコンドリア移植の科学を理解するには、まずこのオルガネラの「出自」を知る必要があります。
約20億年前、太古の真核細胞がαプロテオバクテリアを細胞内に取り込みました。共生関係が成立し、取り込まれた細菌はやがて細胞の一部として定着した——これが「細胞内共生説」です[7]。ミトコンドリアが独自のDNA(mtDNA)を持ち、二重膜構造で包まれ、自己分裂する能力を保持しているのは、かつて独立した生物だった名残です。
この「元・細菌」という出自が、ミトコンドリア移植を可能にする生物学的基盤となっています。
なぜ免疫拒絶が起きないのか。 通常、他者の細胞を移植すれば免疫系が攻撃します。しかしミトコンドリアは細胞ではなく「オルガネラ」です。細胞表面のMHC(主要組織適合性複合体)を持たないため、免疫系の標的になりにくい。実際に、これまでの前臨床研究および臨床報告において、自家ミトコンドリア移植による免疫反応・自己免疫反応・DAMP反応の誘発は確認されていません[2][6][15]。
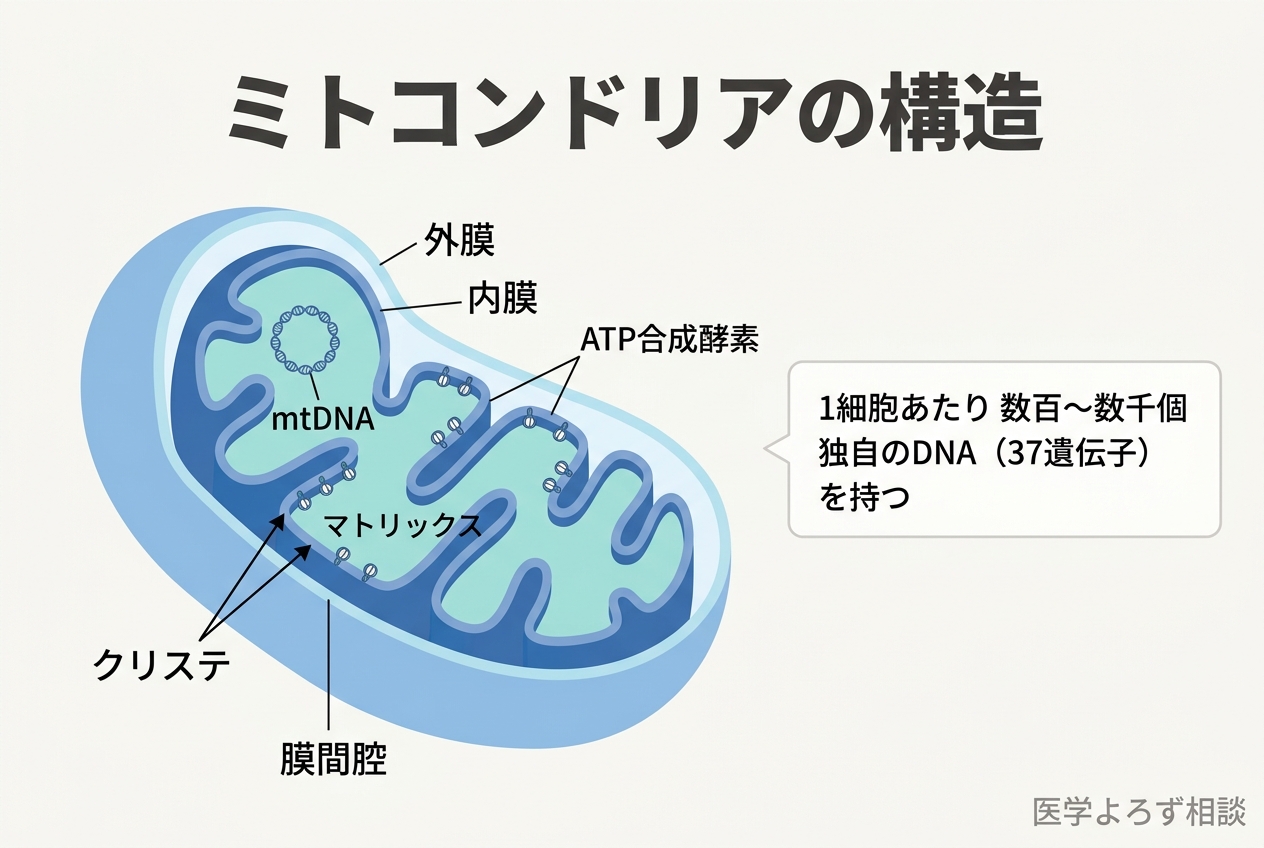
ミトコンドリアの4つの重要な機能
ミトコンドリアは単なる「エネルギー工場」ではありません。
- ATP合成: 酸化的リン酸化により、細胞が必要とするエネルギーの約90%を生成[9]
- カルシウムイオンの恒常性: 細胞内Ca²⁺濃度の調節を通じて、細胞シグナリングを制御
- 活性酸素種(ROS)の管理: 適切な量のROSはシグナル伝達に必要だが、過剰になると酸化ストレスによる細胞障害を引き起こす
- アポトーシス(細胞死)の制御: シトクロムcの放出を介して、損傷細胞の「計画的な除去」を決定する
ミトコンドリアが機能不全に陥ると、これら4つの機能すべてが破綻します。ATPが枯渇し、カルシウムの暴走が起き、ROSが大量発生し、制御不能な細胞死が連鎖する——これが虚血再灌流障害や神経変性疾患の分子レベルの実態です[9]。
概念実証——ウサギの心臓から始まった革命
2013年:ランドマーク実験
ミトコンドリア移植の歴史は、ボストン小児病院のJames McCully博士のチームから始まります。
2013年、Masuzawaらはニュージーランドホワイトウサギの心筋虚血再灌流モデルにおいて、自家ミトコンドリア移植の効果を検証しました[1]。手順は驚くほどシンプルです。
- 同じ個体の腹直筋から少量の筋組織を採取(生検)
- 酵素処理と差速遠心法でミトコンドリアを単離(約30分)
- 単離した生きたミトコンドリアを虚血心筋に直接注入
結果は劇的でした。梗塞サイズが34.2%から7.9%に縮小。再灌流開始から10分以内に心収縮機能が正常化し、その効果は4週間後も維持されました。しかも不整脈の誘発はなし[1]。
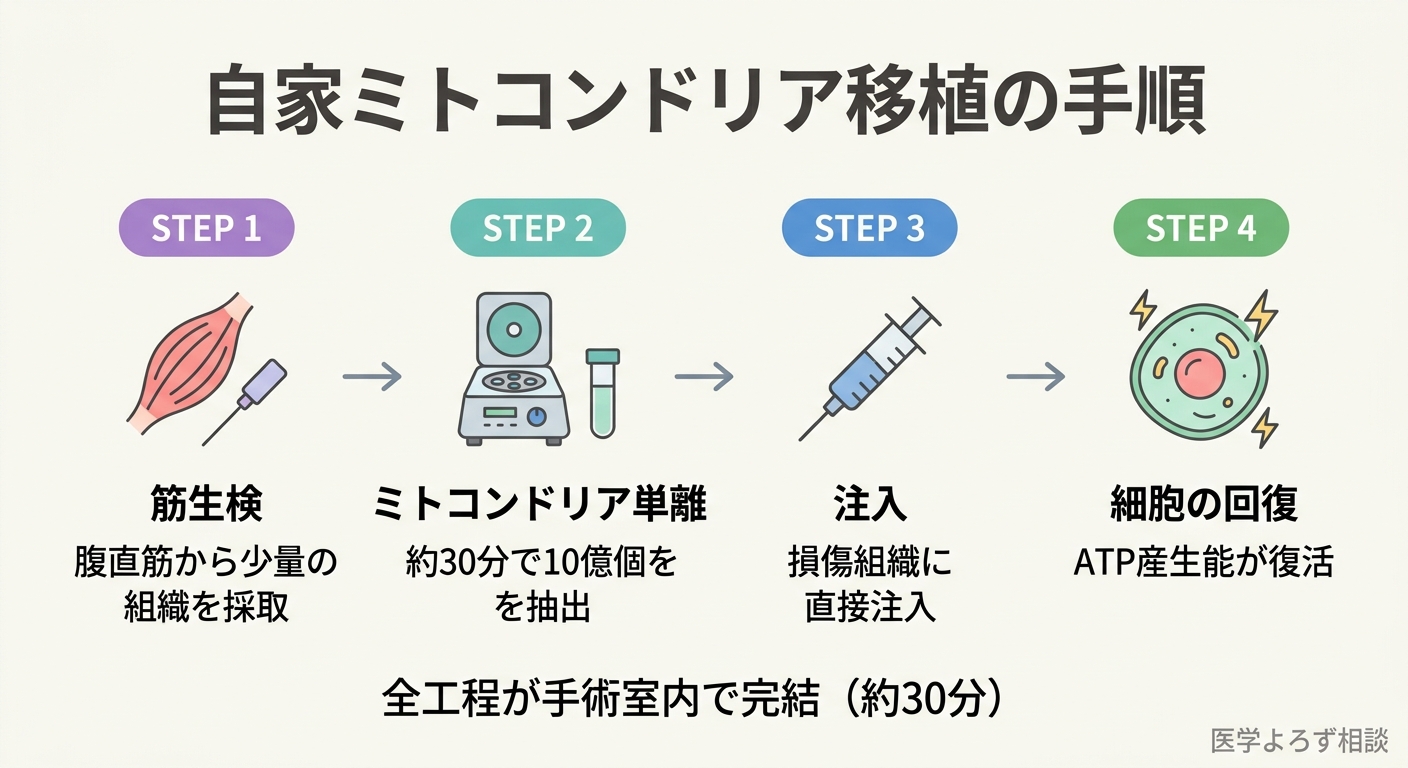
このスピードは臨床上きわめて重要です。心臓手術中の虚血は「分単位」で心筋を損傷するため、30分で準備が完了するミトコンドリア移植は、従来の細胞治療(培養に数週間を要する)とは根本的に異なるタイムラインで介入できます。
2017年:ヒト初の臨床応用
ランドマーク実験からわずか4年。同じボストン小児病院のSitaram Emani博士が、ミトコンドリア移植のfirst-in-human(ヒト初)臨床応用を報告しました[3]。
対象は、先天性心疾患の手術後に虚血再灌流障害を起こし、ECMO(体外式膜型人工肺)から離脱できなくなった小児患者です。従来の治療では回復が見込めない、きわめて重篤な状態でした。
Emani博士は患者自身の腹直筋からミトコンドリアを単離し、虚血心筋に直接注入しました。移植は安全に実施され、心室機能の回復が確認されたのです[3]。
2021年:統計的に示された有効性
Guarientoらは、さらに規模を拡大した後ろ向き比較研究を報告しました[4]。小児24例(ミトコンドリア移植群10例、対照群14例)を対象に、心術後ECMO依存の心原性ショックにおけるミトコンドリア移植の有効性を検証しています。
| 項目 | ミトコンドリア移植群(n=10) | 対照群(n=14) | P値 |
|---|---|---|---|
| ECMO離脱成功率 | 80% | 29% | .02 |
| 機能回復までの日数(中央値) | 2日 | 9日 | .02 |
| 心血管イベント発生率 | 20% | 79% | <.01 |
| 心室ストレイン | -23.0% | -16.8% | .03 |
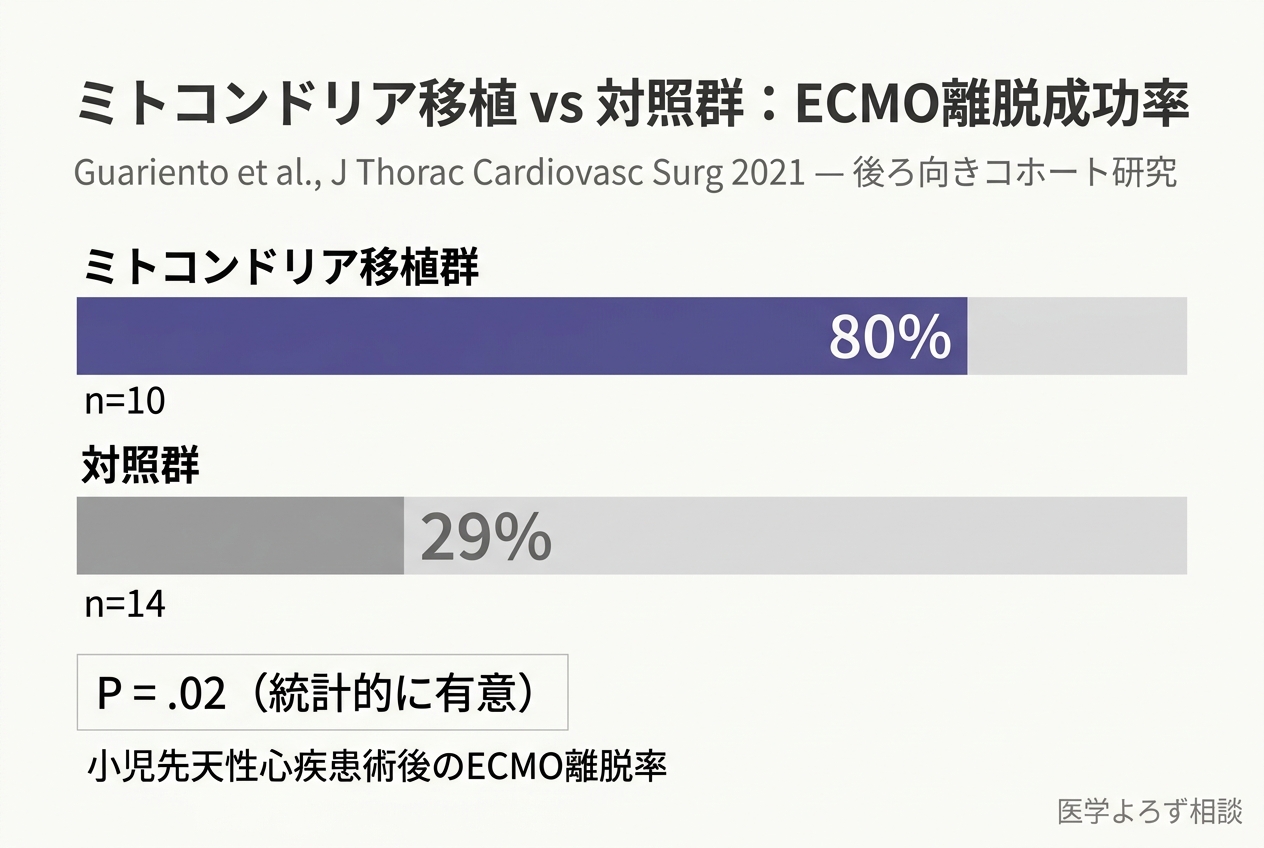
ECMO離脱成功率80%対29%——この差は臨床的にきわめて大きい。ECMO依存の心原性ショックは生命を脅かす緊急事態であり、離脱できなければ予後は極めて不良です。ミトコンドリア移植がこの困難な状況を劇的に改善した意義は計り知れません。
ただし、重要な留意点があります。これは単施設の後ろ向き研究であり、サンプルサイズは24例と小規模です。また、治療群と対照群の患者背景の違い(選択バイアス)を完全に排除できていません。ランダム化比較試験(RCT)による検証が次のステップとして不可欠です。
なぜ外来ミトコンドリアは細胞に統合されるのか
ここで、ひとつの根本的な疑問に向き合いましょう。
「なぜ、外から注入されたミトコンドリアが、他の細胞の中に入り込み、機能できるのか?」
じつは、ミトコンドリアの細胞間移行は人工的な操作がなくても起きている自然現象です[7]。
3つの天然経路
Borcherding & Brestoff(2023)のNature総説は、ミトコンドリアの細胞間移行メカニズムを以下のように体系化しました[7]。
- トンネルナノチューブ(TNTs): 細胞間に形成される直径50〜700nmの管状構造。細胞同士が直接つながり、ミトコンドリアを「手渡し」する。最も効率的な移行経路
- 細胞外小胞(EVs): エクソソームやマイクロベシクルにミトコンドリアの成分(あるいは丸ごと)が包まれて分泌される。血流に乗って遠隔の細胞に到達可能
- 細胞融合・直接接触: ギャップジャンクションやリガンド-受容体結合を介した直接的な移行
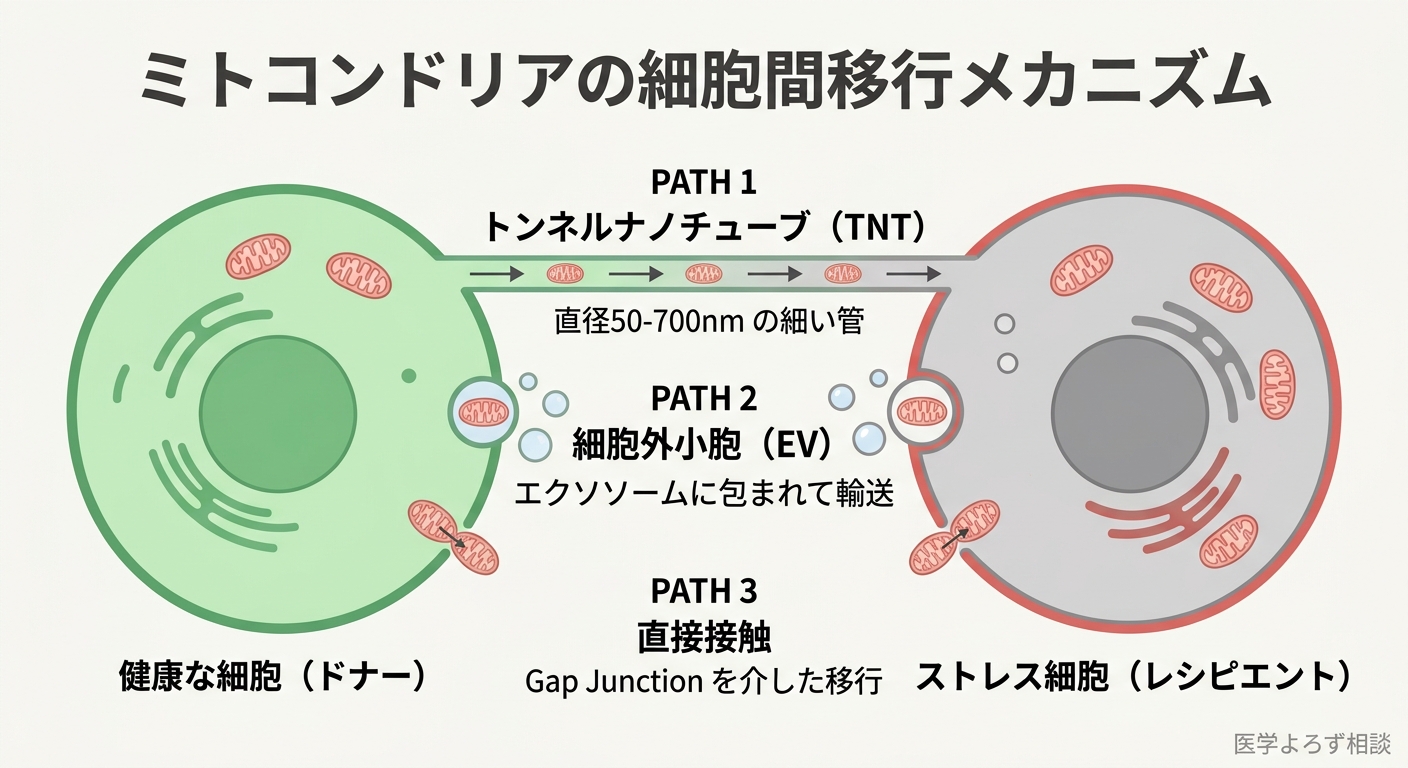
治療的移植における取り込み
治療として外から注入されたミトコンドリアはどうか。McCullyらの研究によれば、注入されたミトコンドリアはエンドサイトーシス(細胞が物質を取り込む基本的なメカニズム)によって2〜8時間以内に標的細胞に取り込まれます[1][6]。取り込まれたミトコンドリアは細胞内のミトコンドリアネットワークに融合し、機能的に統合されることが確認されています。
興味深いことに、移植ミトコンドリアは即座にATPを供給するだけでなく、ホスト細胞自身のミトコンドリア生合成シグナル(PGC-1αなど)を活性化する——いわば「修理マニュアル」まで伝える二段階の効果が報告されています[5]。
用語の国際標準化
この分野は急速に発展しているため、用語の混乱が問題になっていました。2025年、McCully、Brestoff、Singh、Picardら30名以上の国際的専門家が集結し、Nature Metabolism誌で用語の標準化を提唱しました[10]。
- ミトコンドリア移行(mitochondrial transfer): 細胞間で自然に起こるミトコンドリアの移動
- ミトコンドリア移植(mitochondrial transplantation): 治療目的でミトコンドリアを単離・投与する人為的操作
このコンセンサスステートメントは、今後の研究の共通言語として機能することが期待されています[10]。
2026年の3大ブレークスルー
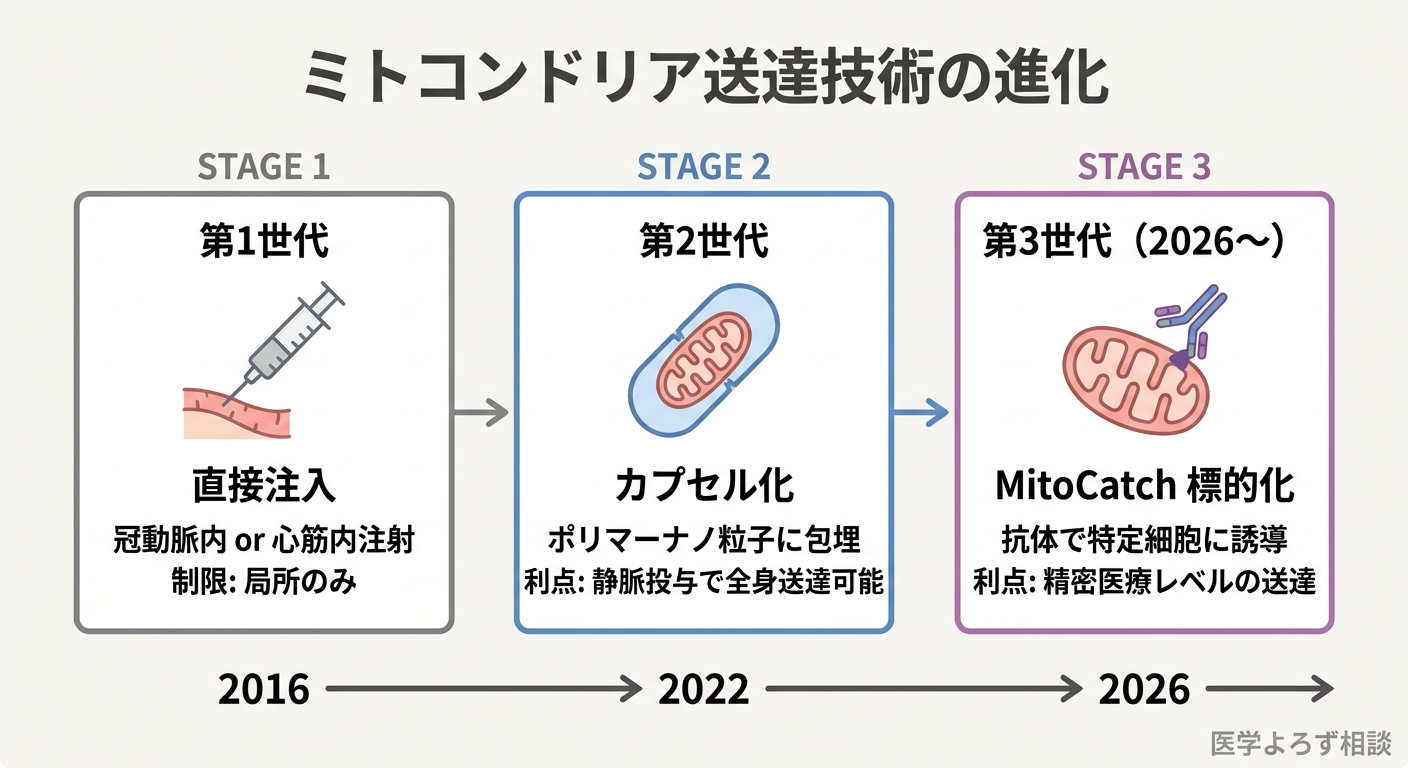
ミトコンドリア移植の初期研究は「筋肉から取り出して、損傷部位に注入する」というシンプルなアプローチでした。しかし2026年、この分野は技術的に大きく飛躍しています。
ブレークスルー1:カプセル化ミトコンドリア(Du et al., Cell 2026)
中国科学院広州生物医薬・健康研究院のDuらは、Cell誌に画期的な論文を発表しました[13]。
課題: 裸のミトコンドリアを血中に投与しても、大半が分解されてしまう。全身投与の効率が悪い。
解決策: 赤血球膜由来の小胞でミトコンドリアを封入する「ミトコンドリアカプセル」技術を開発。
赤血球の膜で包むことで、ミトコンドリアを血中の分解から保護しつつ、生体適合性を確保しました。この技術により、全身投与(静脈注射)が実用的になりました。
成果:
- mtDNA枯渇症候群マウス(Dguok⁻/⁻)のミトコンドリア機能を補完
- リー症候群マウス(Ndufs4⁻/⁻)の症状を改善
- パーキンソン病マウスモデルで神経細胞死を抑制し、運動機能を回復
- サルでの安全性も確認
Duらはこの技術を「オルガネラセラピー」と名づけ、細胞の「部品交換」という再生医療の新概念を提唱しています[13]。
ブレークスルー2:標的化ミトコンドリア送達(Ayupov et al., Nature 2026)
スイス・バーゼル大学IOBのAyupovらは、Nature誌でさらに精巧な技術を報告しました[14]。
課題: ミトコンドリアを注入しても、目的の細胞型に効率よく届かない。
解決策: 「MitoCatch」システム——特異的タンパク質バインダーをミトコンドリア表面に結合させ、標的細胞のみにミトコンドリアを選択的に送達する技術。
これは、いわばミトコンドリアに「宛先ラベル」を貼るような発想です。バインダーの親和性を調整することで、送達効率のチューニングまで可能になりました[14]。
成果:
- 網膜細胞、神経細胞、心筋細胞、内皮細胞、免疫細胞への選択的送達を実証
- 移植ミトコンドリアが細胞内で融合・分裂し、機能的に統合されることを確認
- 視神経萎縮患者由来ニューロンのin vitro生存を促進
- マウスin vivoでの神経損傷後の回復を実証
ブレークスルー3:細胞外小胞を介した送達(Ikeda et al., JACC 2021)
スタンフォード大学のIkedaらは、ヒトiPSC由来心筋細胞から分泌されるミトコンドリアリッチ細胞外小胞(M-EVs)が、裸のミトコンドリアと比較して300分の1のタンパク量で同等のミトコンドリア機能回復効果を示すことを報告しました[5]。
M-EVsはミトコンドリア本体だけでなく、ミトコンドリア生合成に関わるmRNA(PGC-1αなど)も運搬します。つまり、即時的なエネルギー補充と、長期的なミトコンドリア再生という二段階の効果が期待できるのです[5]。iPSC技術との融合により、量産化への道も開けています。
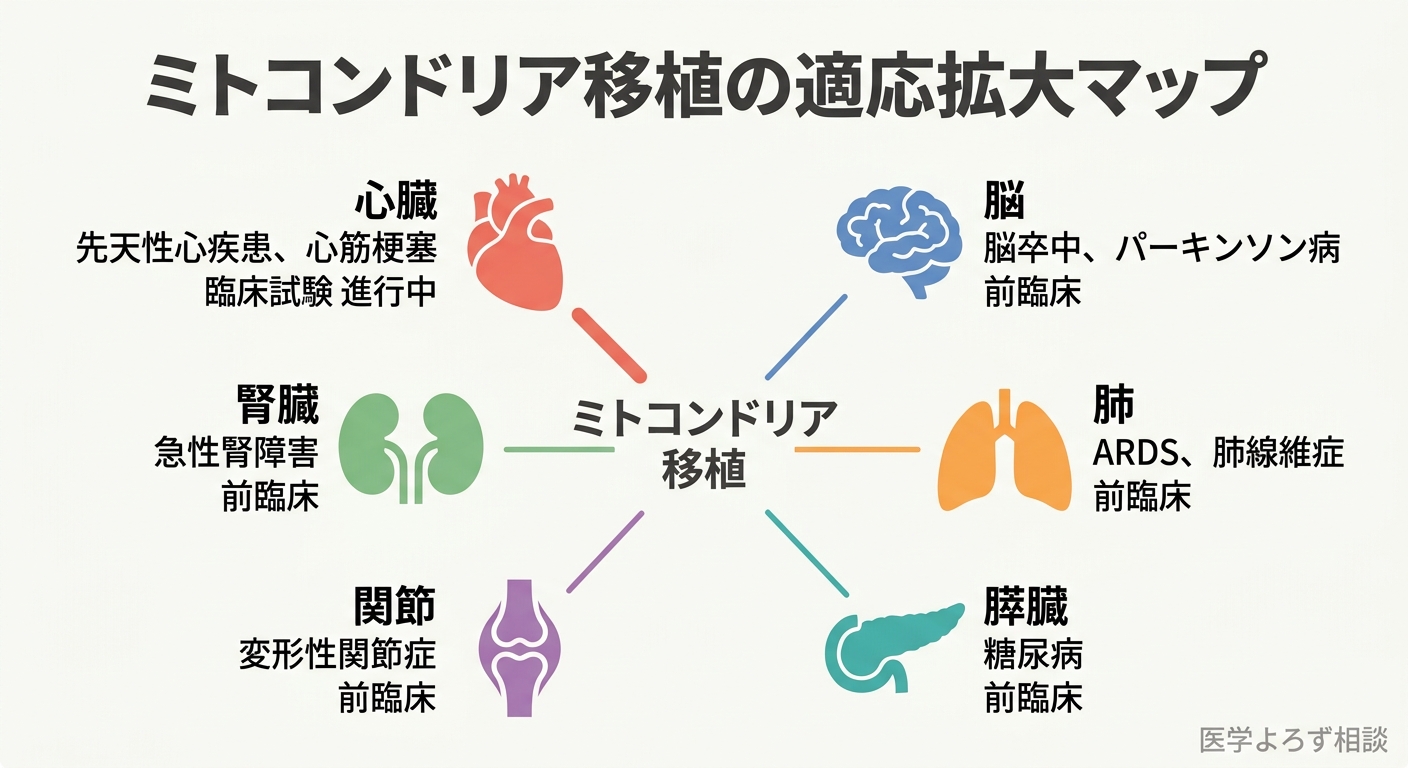
心臓を超えて——適応疾患の急速な拡大
ミトコンドリア移植は心臓外科から始まりましたが、2026年現在、その適応は多臓器・多疾患に急速に拡大しています。
腎臓病
McCullyらは2026年のNature Reviews Nephrology誌で、急性腎障害(AKI)から慢性腎臓病(CKD)への進展におけるミトコンドリア機能障害の役割を詳述しました[15]。持続的なミトコンドリア障害がAKI後のCKD進展を駆動するメカニズムを解説し、動脈内投与による腎臓への標的送達が前臨床モデルで有効であることを示しています。
神経変性疾患
Du et al.(2026)のCell論文は、パーキンソン病マウスモデルにおいてカプセル化ミトコンドリアが黒質ドーパミンニューロンの細胞死を抑制し、運動機能を回復させたことを報告しています[13]。Ayupov et al.(2026)のNature論文でも、視神経萎縮患者由来のニューロンにおける生存促進効果が確認されています[14]。
関節リウマチ(自己免疫疾患)
Lee et al.(2026)は、ミトコンドリア移植が関節リウマチの線維芽細胞様滑膜細胞(FLS)のミトコンドリア・リソソーム機能を回復させ、異常なcGAS-STING1シグナルを抑制し、Th17/Tregバランスを改善することを報告しました[16]。さらに、金ナノ粒子結合ミトコンドリア(GNP-Mito)による関節への標的化送達も実証しています。
糖尿病・代謝疾患
Li et al.(2026)のレビューは、ミトコンドリア移行がインスリン分泌促進、インスリン抵抗性改善、血管内皮細胞の遊走促進に寄与することを体系的にまとめました[17]。代謝疾患へのミトコンドリア移植応用の包括的展望を示しています。
ミトコンドリア遺伝子疾患
Li et al.(2025)のSignal Transduction and Targeted Therapy誌レビューは、さらに先を見据えています[11]。ミトコンドリア遺伝子編集技術(DdCBE、TALEDなど)と移植技術を融合させ、ex vivoでミトコンドリアを編集→選別→移植するという新しいパラダイムを提案しています。
日本での承認状況
2026年4月現在、ミトコンドリア移植は日本において薬事承認された治療法ではありません。 世界的にも、FDA(米国食品医薬品局)が承認したミトコンドリア移植製品は存在しません。
現在のエビデンスの大半は前臨床研究(動物実験)であり、ヒトでの臨床データはボストン小児病院での小児心臓外科領域に限定されています(Phase I相当)[4][8]。
Kubat et al.(2025)はNature Communications誌で、ミトコンドリアベースのナノ治療薬の臨床実用化に向けて、以下の課題を指摘しています[12]:
- スケーラブルなミトコンドリア単離・品質管理プロセスの確立
- 標準化された効力評価法の開発
- 規制フレームワークの整備
- 長期安全性データの蓄積
臨床応用は今後10年単位で段階的に進むと考えられ、現時点で一般の患者が受けられる治療ではありません。「ミトコンドリア移植」を謳う未承認治療には十分ご注意ください。
科学の現在地:わかっていること、いないこと
確立された知見
- ミトコンドリアは細胞間で自然に移行する普遍的な生物学的現象である[7]
- 自家ミトコンドリア移植は、動物モデルおよびヒト小児患者で安全に実施できる[1][3][4]
- 移植ミトコンドリアはエンドサイトーシスで2〜8時間以内に標的細胞に取り込まれ、機能的に統合される[1][6]
- 小児心原性ショックにおいて、ミトコンドリア移植はECMO離脱率を有意に改善した(80% vs 29%、P=.02)[4]
- ミトコンドリア移植は免疫反応・自己免疫反応・不整脈原性を誘発しない[2][6][15]
未解明点・限界
- 大規模RCTが未実施: ヒトでの有効性を示す最大の研究はn=24の後ろ向き比較研究[4]。プラセボ効果や選択バイアスを排除したRCTが不可欠
- 長期安全性が不明: 移植ミトコンドリアの長期的な細胞内運命、mtDNAの異質性(ヘテロプラスミー)への影響は十分に追跡されていない
- 最適な投与法が未確定: 直接注入、血管内投与、カプセル化、EV送達——どの方法がどの疾患に最適かは確立されていない
- 用量反応関係が不明確: 何個のミトコンドリアを投与すれば十分なのか、用量依存性の検証が限定的
- ドナー源の標準化: 自家(自分の筋肉)か同種(他者の細胞)か、どちらが優れているかの比較データが乏しい
- 品質管理基準が未確立: ミトコンドリアの「生存率」「機能性」をどう評価するかの国際基準がない[12]
実践チェックリスト:私たちが今できること
ミトコンドリア移植はまだ臨床研究の段階ですが、ミトコンドリアの健康を守るために今日からできることがあります。
ミトコンドリアを守る生活習慣
- 有酸素運動: 週150分以上の中等度有酸素運動は、ミトコンドリア生合成(PGC-1α経路)を活性化する最も確実な方法
- レジスタンストレーニング: 筋肉量の維持はミトコンドリアの絶対量を維持することに直結する
- 良質な睡眠: 7〜9時間の睡眠。睡眠不足はミトコンドリアの品質管理機構(マイトファジー)を低下させる
- 地中海式食事パターン: 抗酸化物質とオメガ3脂肪酸を豊富に含む食事パターンは、ミトコンドリアの酸化ストレスを軽減する
- 過度のアルコールを避ける: アルコールはミトコンドリアの電子伝達系を直接障害する
この情報を受けて考えてほしいこと
- 「ミトコンドリア移植」を謳う自由診療には慎重に: 2026年4月現在、承認された治療は存在しません。高額な未承認治療を勧める情報源には十分注意してください
- ミトコンドリア病の疑いがある場合: 小児科(遺伝子診療科)やミトコンドリア病の専門外来にご相談ください。日本ミトコンドリア学会のウェブサイトで専門施設を検索できます
- 最新情報をフォローしたい方: ClinicalTrials.gov で "mitochondrial transplantation" を検索すると、進行中の臨床試験を確認できます
おわりに:オルガネラセラピーが切り拓く地平
ミトコンドリア移植は、再生医療の概念を根本から拡張する技術です。
従来の再生医療は「細胞を移植する」ことが基本でした。しかしミトコンドリア移植は「オルガネラ(細胞小器官)を移植する」——細胞よりもさらに小さな単位での介入を可能にしました。Duらが名づけた「オルガネラセラピー」[13]という概念は、壊れた細胞を丸ごと置き換えるのではなく、壊れた部品だけを交換するという、より精密で侵襲の少ないアプローチです。
2013年のウサギの心臓実験から始まり、2017年にヒト初の臨床応用が実現し、2021年に統計的有効性が示され、2026年にはカプセル化・標的化という次世代技術が登場しました。わずか13年間のこの進歩は、この分野の勢いを物語っています。
もちろん、大規模RCTによる検証、長期安全性の確認、規制フレームワークの整備など、臨床実用化までには多くの階段が残されています。しかし、20億年前に私たちの祖先細胞が細菌を取り込んだとき、それが生命の歴史を変えるとは誰も予想できなかったでしょう。
ミトコンドリア移植は、その「第二の共生」を人為的に再現する試みです。
細胞の発電所が壊れたとき、外から新しい電池を届ける。このシンプルで力強い発想が、これからの再生医療をどこまで変えるのか——その答えは、まさにこれから書かれようとしています。
本日のまとめ
- ミトコンドリア移植の本質: 損傷細胞に生きたミトコンドリアを届け、エネルギー産生能を直接回復させる「オルガネラセラピー」
- 臨床エビデンスの現状: 小児心原性ショックでECMO離脱率80%(対照群29%)と有望だが、大規模RCTは未実施。前臨床段階の疾患が大半
- 2026年の技術革新: カプセル化(全身投与)、MitoCatch(標的送達)、EV送達(高効率)の3技術が「精密ミトコンドリア医療」への道を開く
- 判断に迷ったら: 「ミトコンドリア移植」を謳う未承認治療は避け、進行中の臨床試験の動向をフォローする。日常ではミトコンドリアの健康を守る生活習慣を
関連記事:
