はじめに:腕時計が「主治医」になる日は来るのか
朝起きたら、腕時計が「昨夜の深い睡眠は47分でした」と教えてくれる。食後に手元をちらりと見ると、血糖値が150 mg/dLまで跳ね上がっている。ジョギング中にスマートウォッチが振動し、「不規則な心拍リズムを検知しました」と通知が光る——。
こうした光景は、もはやSFではありません。Apple Watch、Fitbit、Oura Ring、FreeStyleリブレといったウェアラブルデバイスは、かつて病院の中だけで測定されていた生体データを、24時間365日、私たちの日常に届けてくれるようになりました。
しかし、ここで立ち止まって考えてみましょう。これらのデータは、本当に「予防医療」として信頼できるのか? メーカーの宣伝と科学的エビデンスの間には、しばしば大きな溝があります。
本記事では、2024〜2026年の最新メタアナリシス・システマティックレビュー15件を中心に、ウェアラブルデバイスの3大領域——連続血糖モニタリング(CGM)、睡眠トラッキング、スマートウォッチ心電図——の「科学的な現在地」を、臨床医の視点から正直にお伝えします。
連続血糖モニタリング(CGM)——「健康な人」にも意味があるのか
CGMとは何か
連続血糖モニタリング(Continuous Glucose Monitoring: CGM)は、皮下に挿入した小さなセンサーが間質液中のグルコース濃度を5分ごとに測定し、スマートフォンにリアルタイムで表示する技術です。もともとはインスリン治療中の糖尿病患者のために開発されましたが、近年は「糖尿病でない人」への利用が急速に拡大しています。
日本でも2024年以降、FreeStyleリブレ2がドラッグストアで購入可能になり、健康意識の高い層を中心に「自分の血糖パターンを知りたい」というニーズが高まっています。
エビデンスは何を示しているか
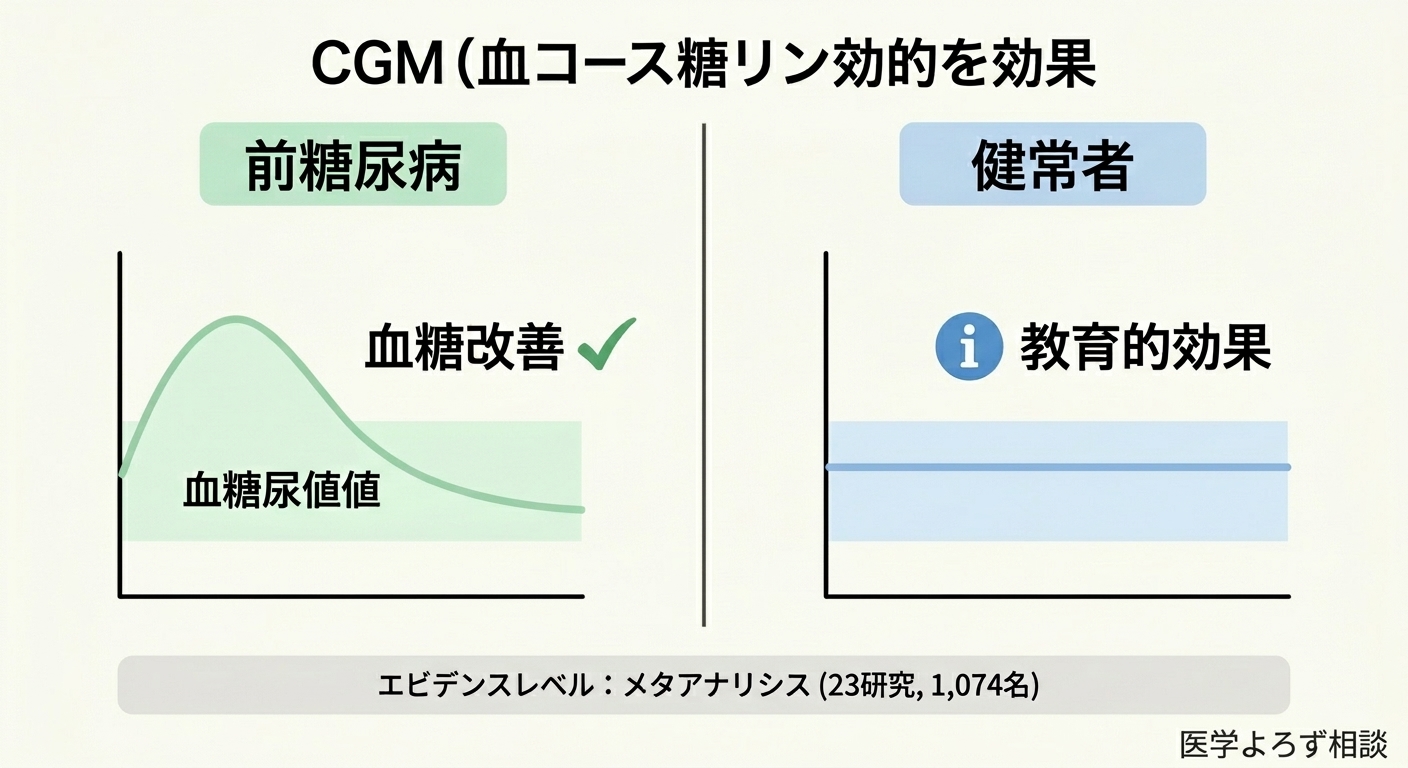
2026年に発表されたLiaoらのメタアナリシス[1]は、非糖尿病者を対象としたCGM研究23件(1,074名、11カ国)を統合解析した、現時点で最も包括的なエビデンスです。その結論は明確でした:
- 前糖尿病(HbA1c 5.7〜6.4%)の人: CGM使用により平均血糖値が有意に改善
- 健常者(HbA1c 5.6%以下): 有意な血糖改善は認められず、主に「教育的価値」にとどまる
つまり、「すでに血糖調節に問題を抱えつつある人」にはCGMが実質的な行動変容をもたらすが、「完全に健康な人」が装着しても、数値上の改善は限定的だということです。
CGMは「行動変容ツール」として機能するか
Richardsonらの2024年のメタアナリシス[3]は、CGMを「行動変容ツール」として評価したRCTのみを対象とした点で重要です。CGMフィードバックを受けた群では、炭水化物からのエネルギー摂取割合が有意に低下しました。ただし、総エネルギー摂取量や体重への有意な効果は確認されていません。
つまりCGMは「何を食べると血糖が上がるか」を可視化することで食事の質を変える力を持ちますが、「食べる量を減らす」「体重を落とす」という効果は、現時点ではエビデンスが不十分です。
心血管予防への可能性
Capponらの系統的レビュー[2]は、食後血糖スパイクと血糖変動性(glycemic variability)が独立した心血管リスク因子であることを踏まえ、CGMが心血管予防に貢献しうる可能性を示唆しています。しかし、長期的な心血管イベント(心筋梗塞や脳卒中)の減少を直接証明した大規模RCTは存在しません。これは今後の最重要課題です。
非侵襲CGMの展望
Dimovaらの2025年のレビュー[4]は、現在開発中の非侵襲的CGM(針を刺さずに血糖を測定する技術)に焦点を当てています。近赤外分光法やマイクロ波センサーなど複数のアプローチが進行中ですが、精度面では既存の侵襲的CGM(FreeStyleリブレ等)に大きく劣り、臨床使用には至っていません。将来的にスマートウォッチに搭載される可能性がありますが、現時点では「期待先行」の状態です。
睡眠トラッキング——「総睡眠時間はまずまず、睡眠段階は要注意」
消費者向けデバイスはPSGの代わりになるか
睡眠の「ゴールドスタンダード」は、脳波・眼球運動・筋電図を同時記録するポリソムノグラフィ(PSG)です。Apple Watch、Fitbit、Oura Ring、WHOOPなどの消費者向けデバイスは、加速度計と光電容積脈波(PPG)センサーで睡眠を推定しますが、その精度はPSGと比較してどの程度なのでしょうか。
多施設検証研究の結論
Leeらの2023年の多施設前向き検証研究[5]は、消費者向け睡眠トラッカー11機種(ウェアラブル5、ニアラブル3、エアラブル3)を75名の被験者でPSGと同時比較した、この分野で最も包括的な研究です。
結果は機種間で大きなばらつきがありました:
| 指標 | 最良の成績 | 最低の成績 |
|---|---|---|
| マクロF1スコア(睡眠段階の総合精度) | 0.69 | 0.26 |
| 総睡眠時間の誤差 | 許容範囲内(多くの機種) | 一部機種で大幅な乖離 |
Google Pixel WatchとApple Watch 8が比較的高い精度を示しましたが、いずれの機種も睡眠段階(浅い睡眠・深い睡眠・REM睡眠)の判定には課題があり、特に覚醒時間の検出が不正確でした。

機種ごとの特性
Aritake-Okadaらの2025年の検証研究[6]では、6機種(Fitbit Charge 5、Fitbit Sense、Withings Scanwatch、Garmin Vivosmart 4、WHOOP 4.0、Apple Watch Series 8)を62名で比較しました。ここから見えてくるのは:
- PPGセンサー搭載機種(心拍変動を利用)は、加速度計のみの機種より睡眠段階判定に優位
- 覚醒時間が短い夜は過大評価、長い夜は過小評価する傾向が全機種に共通
- 総睡眠時間の推定はすべての機種で研究用アクチグラフィと同等の精度
Mendezらの系統的レビュー[7]は、Fitbit Charge 4・Garmin Vivosmart 4・WHOOPの3機種に絞った評価で、WHOOPが総睡眠時間と浅い睡眠においてPSGとの乖離が最小でしたが、深い睡眠とREM睡眠の判定はいずれの機種でも改善が必要と結論しています。
臨床現場への示唆
まとめると、消費者向け睡眠トラッカーの「信頼度マップ」は以下のようになります:
| データの種類 | 信頼度 | 臨床での活用可能性 |
|---|---|---|
| 総睡眠時間 | ★★★★☆ | トレンドの把握に有用 |
| 就寝・起床時刻 | ★★★★★ | 概日リズムの評価に有用 |
| 深い睡眠の時間 | ★★☆☆☆ | 参考値としてのみ |
| REM睡眠の時間 | ★★☆☆☆ | 参考値としてのみ |
| 睡眠時無呼吸の検出 | ★★☆☆☆ | スクリーニング目的なら可能性あり |
重要なポイント: 睡眠トラッカーの数値そのものに一喜一憂するのではなく、「自分のベースラインからの変化」を見ることが臨床的に意味があります。
スマートウォッチ心電図——「心房細動スクリーニング」の大きな一歩
なぜ心房細動の早期発見が重要なのか
心房細動(AF)は最も一般的な不整脈であり、脳卒中リスクを約5倍に高めます[8]。問題は、AFは無症候性のことが多く、脳卒中で初めて診断されるケースが少なくないことです。定期健診の短時間心電図では発作性AFを捕捉できないため、24時間以上の連続モニタリングが理想ですが、従来のホルター心電図は患者負担が大きく、大規模なスクリーニングには不向きでした。
ここに、スマートウォッチが革命を起こしつつあります。
Apple Heart Study——42万人の衝撃
2019年にNEJMに発表されたPerezらのApple Heart Study[8]は、419,297名という前例のない規模で、Apple Watchの不規則脈通知アルゴリズムを検証しました:
- 0.52%(2,161名)が不規則な脈拍の通知を受領
- 通知後にECGパッチを装着した参加者のうち、34%にAFが確認
- 通知の84%がAFと一致
この研究は「サイトレス(来院不要)」デザインの先駆けであり、消費者デバイスによる大規模スクリーニングの可能性を世界で初めて実証しました。
メタアナリシスが示す診断精度
Apple Heart Studyから6年が経ち、データは大幅に蓄積されました。
Apple Watch特化のメタアナリシス(Kimら、2025年)[9]:
- AUC 0.968(SD 0.01)——非常に高い診断能
- アルゴリズム自動判定:感度86%、特異度94%
- 専門家による手動判読:感度96%、特異度95%
- 自動判定と手動判読の差(感度86% vs 96%)は、医師による確認の重要性を示唆
ブランド横断的メタアナリシス(De Vosら、2025年)[10]:
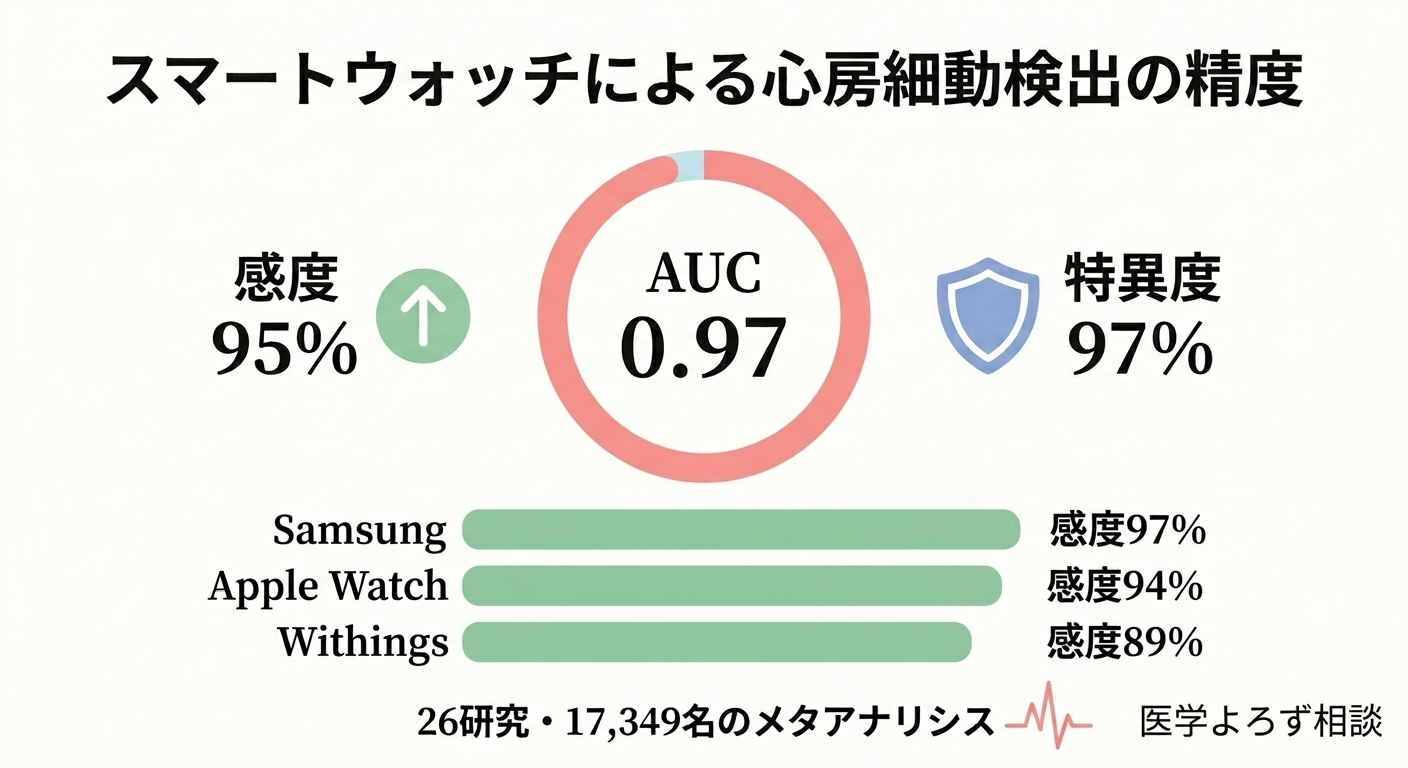
- 26研究、17,349名を統合
- 統合感度95%(95%CI 92-97%)、統合特異度97%(95%CI 94-98%)、AUC 0.97
- Samsung:感度97%、Apple Watch:感度94%、Withings:感度89%
- ただし異質性が高い(I²=95-99%)
ECGベースとPPGベースの違い
Iqhrammullaらの2025年のメタアナリシス[11]は、検出方式の違いに注目しました:
- ECGベース(Apple Watch等):特異度が高い。30秒間指を当てて記録するため、能動的な操作が必要
- PPGベース(光学式心拍センサー):常時モニタリングが可能だが、特異度でECGベースに劣る
臨床的には、PPGで常時スクリーニング → 異常検知時にECGで確認という2段階アプローチが最も実用的と考えられています。
日本の規制状況
日本不整脈心電学会と日本循環器学会は、2025年に「携帯型/装着型心電計の適切使用に関するコンセンサスステートメント」[14]を公表しました。これは日本でウェアラブル心電図を臨床活用する際の唯一の公式ガイダンスです。Apple Watchは2021年1月から日本で心電図機能が利用可能(医療機器認定済み)ですが、あくまで「不整脈の手がかりを得るツール」であり、確定診断には必ず12誘導心電図と専門医の判断が必要であることが強調されています。
ウェアラブルの新たなフロンティア——感染症と高齢者医療
感染症の発症前検出
Mishraらの2020年のNature Biomedical Engineering掲載研究[12]は、スマートウォッチデータからCOVID-19を症状出現前に検出できることを示した画期的な研究です。約5,300名のコホートからCOVID-19感染者32名を特定し:
- 81%(26/32名)で心拍数・歩数・睡眠時間に変化を検出
- 63%の症例を症状出現前にリアルタイムで検出可能
- 最大で発症9日前に異常を検知した例も
この研究は「ウェアラブルによる感染症サーベイランス」という新しいパラダイムを切り拓きました。今後、インフルエンザや他の感染症への応用が期待されますが、COVID-19に特化した小規模研究であり、一般化にはさらなる検証が必要です。
高齢者医療——フレイル・転倒・認知機能
原・山本の2025年の総説[15]は、日本の超高齢社会におけるウェアラブル活用を概観しています。心拍数・血圧・歩数・移動速度・姿勢・睡眠深度・ストレス状態をデジタルバイオマーカーとして活用し、フレイル・サルコペニア・認知機能低下・転倒・睡眠障害の早期検出に有用であることが報告されています。
日本の臨床現場での課題は、高齢者のデバイス装着コンプライアンスとデジタルリテラシーの問題です。家族や介護者が関与するサポート体制の構築が、普及の鍵を握っています。
科学の現在地:わかっていること、いないこと
確立された知見
- スマートウォッチECGは心房細動の検出において高い診断精度を持つ(感度95%、特異度97%)[10]
- CGMは前糖尿病者の血糖改善と食事行動の変容に有効[1][3]
- 睡眠トラッカーの総睡眠時間推定は臨床的に許容できる精度[5][6]
- ウェアラブルデータから感染症の発症前検出が原理的に可能[12]
未解明・限界
- CGMが「健常者」の長期的な健康アウトカムを改善するかは未証明。心血管イベントの減少を直接示した大規模RCTはゼロ[2]
- 睡眠段階(深い睡眠・REM)の判定精度は不十分。デバイスが示す「深い睡眠47分」を文字通りに受け取るべきではない[5][7]
- スマートウォッチAF検出の「偽陽性」問題。健康な若年者が不要な不安を抱えるリスクがある。通知を受けた際の適切なフォローアップ体制の整備が不可欠[8]
- 非侵襲的CGMの精度は既存センサーに大きく劣り、臨床使用には至っていない[4]
- ウェアラブルデータの相互運用性——デバイス間・メーカー間でデータ形式が統一されておらず、医療システムとの統合が困難[13]
- エビデンスの大半が欧米データであり、日本人を対象とした大規模研究は限定的
実践チェックリスト:ウェアラブルを賢く使うために
CGMを検討している方へ
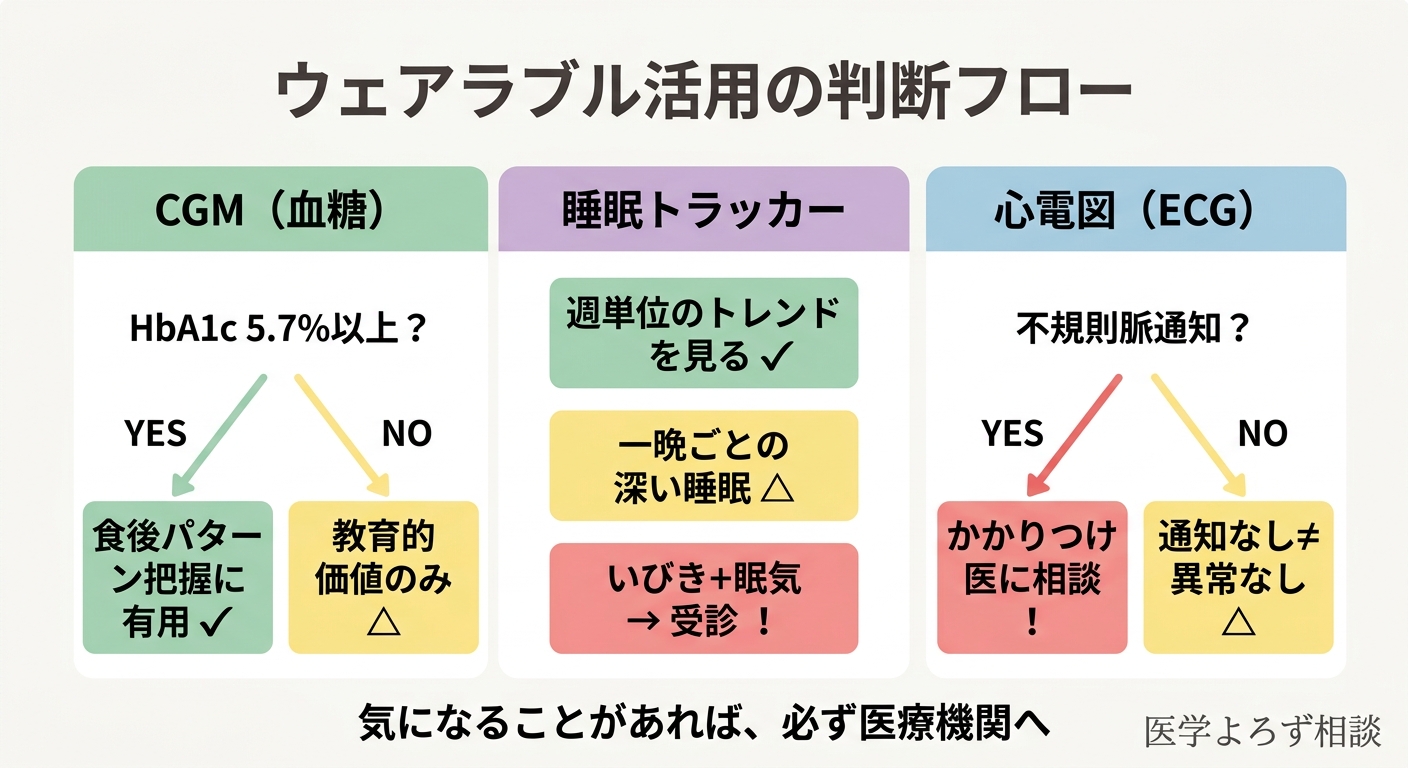
- ✅ HbA1c 5.7%以上(前糖尿病)の指摘がある → CGMで食後血糖パターンの把握は有用
- ⚠️ HbA1c正常で特にリスクなし → 教育的価値はあるが、費用対効果を考慮
- ❌ 「CGMの数値に振り回されてストレスを感じる」 → 健康不安の増強になりうる。中止を検討
睡眠トラッカーを使っている方へ
- ✅ 週単位のトレンド(平均睡眠時間の推移、就寝時刻の安定性)を見る → 最も有用
- ⚠️ 一晩ごとの「深い睡眠の時間」に一喜一憂する → 精度が不十分。参考値として
- ✅ 「いびきが多い」「日中の眠気がひどい」 → 睡眠時無呼吸症候群の可能性。医療機関を受診
スマートウォッチの心電図・不規則脈通知を使っている方へ
- ✅ 「不規則な脈拍」の通知を受けた → 焦らず、かかりつけ医に心電図を相談
- ✅ 動悸・めまい・息切れがある + 通知 → 速やかに循環器内科を受診
- ❌ 通知がないことを「心臓は大丈夫」の根拠にしない → 発作性AFは常時検出できない
おわりに:「データを味方にする」ために必要なこと
臨床医として日々患者さんと接する中で、ウェアラブルデバイスの普及がもたらす変化を実感しています。外来で「Apple Watchが不規則な脈拍を検知しました」と見せてくれる患者さんは増え、実際にそこから心房細動が見つかり抗凝固療法を開始できたケースもあります。
一方で、「睡眠スコアが低くて不安になった」「血糖値のグラフが気になって食事を楽しめない」という相談も少なくありません。テクノロジーは使い方次第で、健康への気づきにも、健康不安の種にもなります。
大切なのは、ウェアラブルデバイスを「診断ツール」ではなく「気づきのきっかけ」として位置づけることです。異常を感じたら医療機関を受診し、専門家と一緒にデータを解釈する——この「人間とテクノロジーの協働」こそが、予防医療の未来の姿だと確信しています。
本日のまとめ
- ウェアラブルの現在地: CGM・睡眠・心電図の3領域で科学的エビデンスが蓄積しているが、領域ごとに成熟度は大きく異なる
- 最もエビデンスが強い領域: スマートウォッチによる心房細動検出(感度95%、特異度97%)
- 判断に迷ったら: 数値そのものではなく「トレンドの変化」に注目し、気になることがあれば必ずかかりつけ医に相談
