はじめに:「全員同じ薬」の時代は終わりつつある
風邪をひいたら抗生物質、血圧が高ければ降圧薬、がんと言われたら抗がん剤——つい最近まで、医療は「100 人の患者に 100 人とも同じ薬を出す」のが当たり前でした。しかし同じ薬を飲んでも、よく効く人もいれば、まったく効かない人も、重篤な副作用に苦しむ人もいます。その違いの鍵を握っているのが、一人ひとりの「ゲノム(遺伝情報)」です。
2003 年にヒトゲノムの全塩基配列が解読されてから約 20 年。ゲノム解析のコストは当時の 300 万ドルから 1,000 ドル未満へと劇的に下がり、遺伝子検査は研究室の技術から臨床現場のツールへと変貌を遂げました。日本でも 2019 年にがん遺伝子パネル検査が保険適用となり、「患者のゲノム情報に基づいて治療を選ぶ」精密医療(プレシジョン・メディシン)は、もはや未来の話ではありません。
本記事では、がんゲノム医療から薬理ゲノミクス、さらにがん以外の領域への広がりまで、精密医療の最前線をエビデンスとともに解説します。
精密医療とは何か——One-Size-Fits-All からの転換
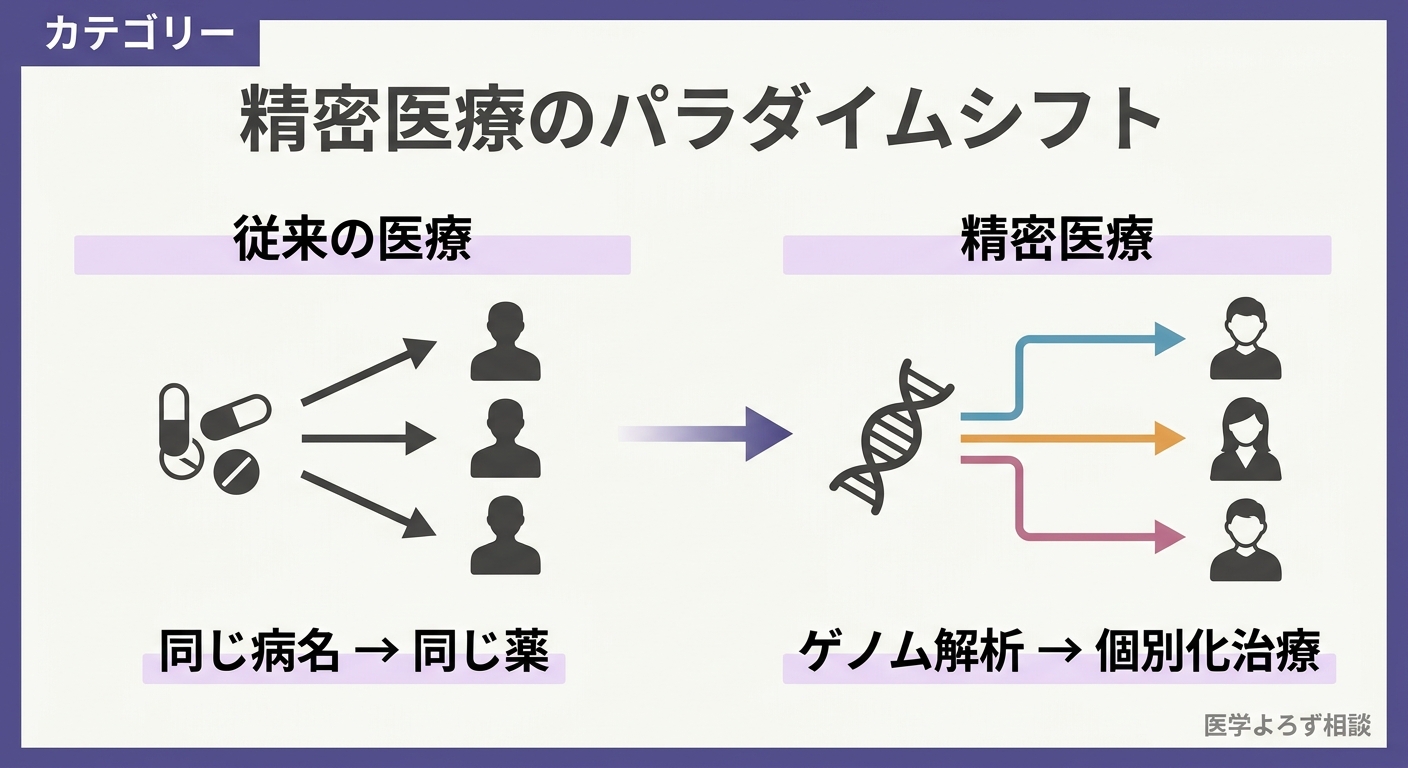
精密医療とは、患者一人ひとりの遺伝情報、環境因子、生活習慣を考慮して、最適な治療法を選択するアプローチです。従来の医療が「疾患名」で治療法を決めていたのに対し、精密医療は「その患者の体の中で何が起きているか」を分子レベルで理解し、治療を個別化します。
その中核を担うのが遺伝子検査です。がん細胞にどんな遺伝子変異があるかを調べれば、その変異を標的とする分子標的薬が使えるかもしれない。薬を代謝する酵素の遺伝子型を調べれば、副作用を避けながら適切な用量を決められるかもしれない。精密医療の進化とは、腫瘍の種類中心の治療から、ゲノム変異中心の治療へのパラダイムシフトそのものです [1]。
Tsimberidou らの包括的レビューは、この進化を明確に描いています。がん領域では「組織型不問(tissue-agnostic)」の治療——つまり、がんの発生部位に関係なく、特定の遺伝子変異を持つがんすべてに使える薬——が次々と承認され、ゲノム変異にマッチした治療は、マッチしない治療と比較して優れたアウトカムを示しています [1]。
がんゲノム医療の現在地
遺伝子パネル検査——日本の 54,000 人解析が示すもの
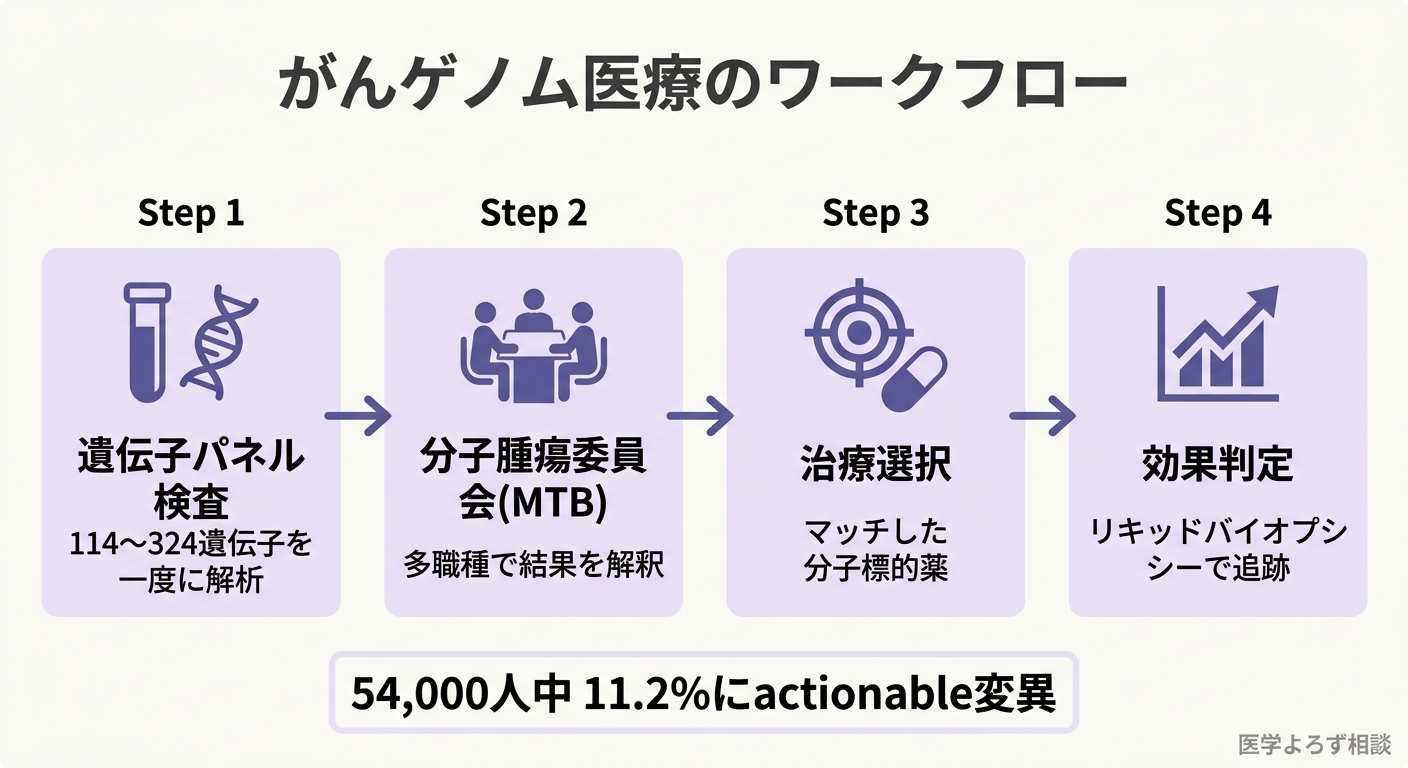
がんゲノム医療の入口となるのが、遺伝子パネル検査です。これは、がん細胞から数百の遺伝子を一度に解析し、治療標的となる変異を探す検査です。日本では 2019 年 6 月から保険適用となり、現在 NCC オンコパネル、FoundationOne CDx など 5 つの検査が保険収載されています。費用は約 56 万円で、3 割負担の場合は約 16.8 万円です。
2026 年 1 月、国立がん研究センターが画期的なデータを発表しました [14]。2019 年 6 月から 2024 年 6 月までの約 54,000 名の固形がん患者を対象とした解析で、11.2% に国内承認薬の標的遺伝子異常が検出され、5.4% に海外承認薬の標的遺伝子異常が見つかりました。つまり、検査を受けた患者の約 6 人に 1 人に、治療に直結しうる遺伝子変異が見つかったのです。
この数字は一見すると少なく感じるかもしれません。しかし、従来であれば「標準治療が効かなくなった後は打つ手がない」と言われていた患者さんにとって、新たな治療選択肢が開ける可能性は計り知れません。
分子腫瘍委員会(MTB)——検査結果を治療につなげる仕組み
遺伝子パネル検査で変異が見つかっても、それをどう治療に活かすかは単純ではありません。ここで重要な役割を果たすのが、分子腫瘍委員会(Molecular Tumor Board: MTB)です。MTB は、腫瘍内科医、病理医、遺伝カウンセラー、バイオインフォマティシャン(生命情報科学者)など多職種が参加し、個々の患者の遺伝子検査結果を解釈して治療方針を推奨する会議体です。
Larson らのシステマティックレビュー(14 研究、3,328 患者)によれば、MTB 推奨治療の奏効率は研究により 0-67% と幅がありますが、唯一の比較試験では MTB ガイド療法群で無増悪生存期間が有意に改善していました [2]。Luchini らのレビューも、MTB の構成要素や運用方法を体系的に整理し、actionability(臨床的に行動可能な変異かどうか)の分類法やターンアラウンドタイムの標準化が今後の課題であると指摘しています [3]。
つまり、遺伝子パネル検査は「検査して終わり」ではなく、MTB による多職種での解釈→治療選択→効果判定 というプロセス全体が機能して初めて、患者さんの利益につながるのです。
リキッドバイオプシー——血液で「がんの残り」を追う
精密医療のもう一つの革新が、リキッドバイオプシー(液体生検)です。従来の生検(バイオプシー)では腫瘍組織を直接採取する必要がありましたが、リキッドバイオプシーは血液中を循環する腫瘍由来 DNA(ctDNA)を解析することで、低侵襲にがんの情報を得られます。
Shen らのシステマティックレビュー・メタアナリシス(34 の診断研究、21 の予後研究)は、早期非小細胞肺がんにおけるリキッドバイオプシーの臨床的有用性を実証しています [12]。診断精度は AUC 0.84-0.87 と良好で、特に注目すべきは微小残存病変(MRD: Minimal Residual Disease)の検出能力です。手術後に MRD が陽性だった患者は、再発リスクが 4.95 倍(HR 4.95)、全生存期間の悪化が 3.93 倍(HR 3.93)と、きわめて強い予後予測因子であることが示されました。
さらに重要なのは、MRD が画像検査で再発が確認される平均 179 日前に検出可能だったという点です。つまり、画像では見えない段階で「がんが残っている」ことを血液検査で察知し、早期に追加治療を開始できる可能性があるのです。MRD 陽性患者で補助療法の有意なベネフィットも報告されており、リキッドバイオプシーは「がんの早期発見」だけでなく「再発の早期発見」の武器として期待されています。
薬理ゲノミクス——遺伝子で「薬との相性」がわかる
CPIC ガイドラインの成果
精密医療のもう一つの柱が、薬理ゲノミクス(ファーマコゲノミクス)です。これは、薬の効き方や副作用の出やすさを遺伝子型から予測し、個々の患者に最適な薬・用量を選択するアプローチです。
この分野の世界標準となっているのが CPIC(Clinical Pharmacogenetics Implementation Consortium)ガイドラインです。Caudle らの最新レポートによれば、CPIC は現在 34 遺伝子・164 薬剤をカバーし、PubMed 掲載の薬理ゲノミクス実装研究の 85% が CPIC を引用しています [5]。128 の医療機関と 40 の商業検査所が CPIC ガイドラインを使用しており、実装の障壁は「エビデンスの不足」から「臨床医教育・保険償還・電子カルテ統合」へとシフトしています。
Sadee らの包括的レビューも、薬物代謝酵素・トランスポーター・受容体のゲノム変異が薬効・副作用に与える影響を体系的に整理し、FDA 承認の個別化治療薬が急増していることを報告しています [4]。

成功例 1:DPYD とフルオロピリミジン系抗がん剤
5-FU やカペシタビンといったフルオロピリミジン系抗がん剤は、大腸がんや胃がんなど消化器がんの標準治療に広く使われています。しかし、DPYD(ジヒドロピリミジン脱水素酵素)遺伝子に変異を持つ患者では、薬の分解が遅れ、重篤な副作用——重度の下痢、骨髄抑制、まれに死亡——が生じるリスクが高くなります。
CPIC ガイドラインは、DPYD 変異保有者に対して遺伝子型に基づく用量調整または代替薬の選択を強く推奨しています [6]。事前に遺伝子検査を行うことで、命に関わる副作用を未然に防げる可能性がある、薬理ゲノミクスの代表的成功例です。
成功例 2:CYP2C19 とクロピドグレル
心筋梗塞や脳梗塞の予防に使われる抗血小板薬クロピドグレルは、体内で CYP2C19 という酵素によって活性化されます。CYP2C19 の中間代謝型・低代謝型の遺伝子型を持つ人では活性化が不十分で、血小板抑制が弱くなり、心血管イベントのリスクが上昇します。
Lee らによる 2022 年更新の CPIC ガイドラインは、これらの遺伝子型を持つ患者には代替の抗血小板薬(プラスグレルやチカグレロル)への変更を強く推奨しています [7]。日本人を含むアジア人では CYP2C19 低代謝型の頻度が欧米人より高い(約 15-20%)ため、この知見は日本の臨床現場にとって特に重要です。
成功例 3:CYP2D6 と抗うつ薬
うつ病の治療に広く使われる SSRI(選択的セロトニン再取り込み阻害薬)や SNRI の代謝にも、遺伝的な個人差が大きく影響します。Bousman らの 2023 年 CPIC ガイドラインは、CYP2D6・CYP2C19・CYP2B6 の遺伝子型に基づく用量調整・薬剤選択を推奨しています [8]。
例えば、CYP2D6 の超高速代謝型では薬が速く分解されて効果不十分になり、低代謝型では薬が体内に蓄積して副作用が出やすくなります。抗うつ薬は日常診療で最も処方頻度の高い薬剤クラスの一つであり、遺伝子型情報を活用することで「なかなか効く薬が見つからない」という患者さんの苦しみを軽減できる可能性があります。
日本の薬理ゲノミクスの現状
日本では薬理ゲノミクス検査の保険適用はまだ限定的です。一部の抗がん剤(イリノテカンの UGT1A1 検査など)では保険で検査が行われていますが、循環器領域や精神科領域での遺伝子型検査は一般臨床に浸透しているとは言えません。CPIC が指摘するように、臨床医への教育と電子カルテへの統合が今後の課題です [5]。一方で、Sadee らが指摘する民族間差異の問題は重要です。欧米のデータをそのまま日本人に適用できない場合があり、日本人集団でのバリデーションが求められます [4]。
がん以外に広がる精密医療
糖尿病——精密糖尿病医療の夜明け
精密医療はがんだけのものではありません。Tobias らが Nature Medicine に発表した第 2 回国際コンセンサスレポートは、糖尿病における精密医療の展望を包括的に整理しています [11]。
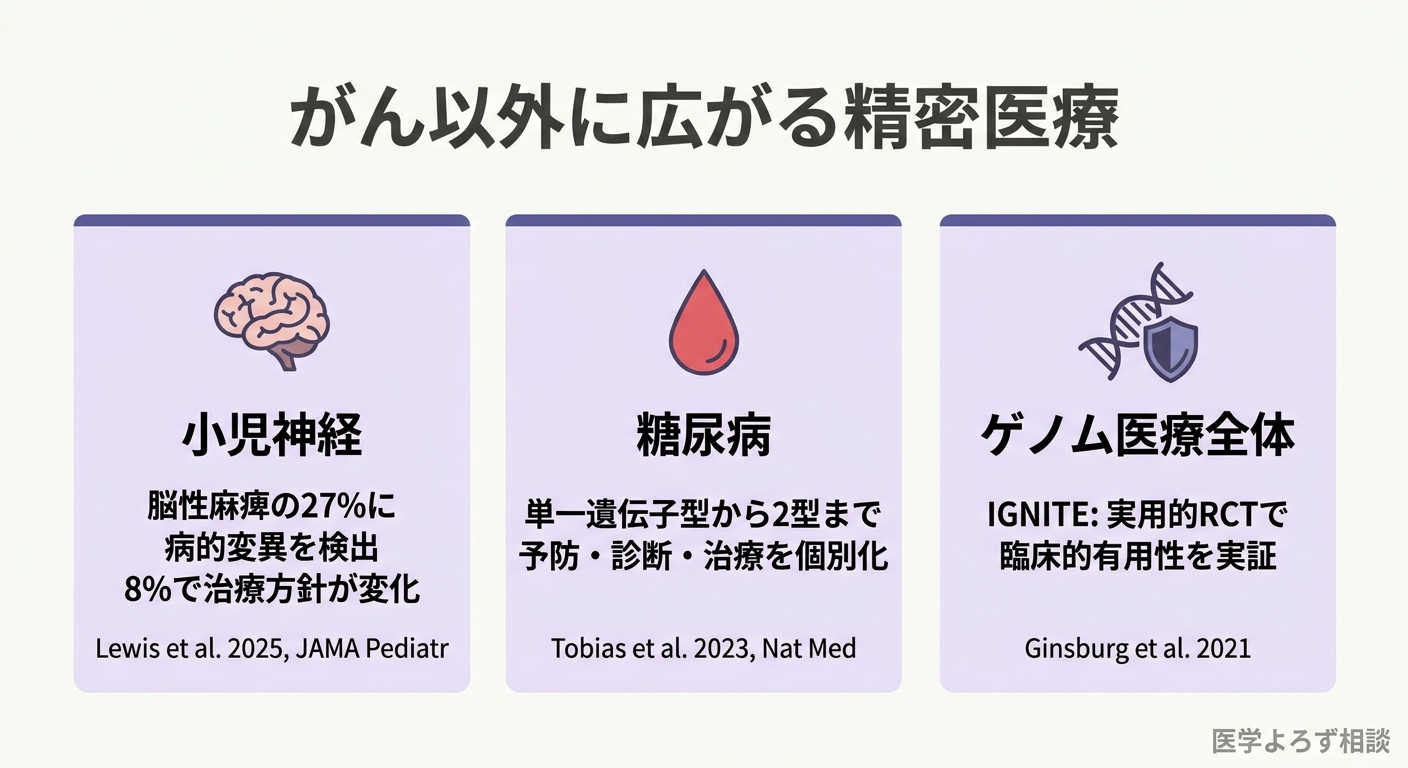
単一遺伝子性糖尿病(MODY など)では、遺伝子診断によって治療法が劇的に変わるケースがすでにあります。例えば、GCK 遺伝子変異による MODY2 は薬物治療が不要であり、HNF1A 変異による MODY3 はスルホニル尿素薬が著効します。2 型糖尿病でも、遺伝的リスクスコアやサブタイプ分類に基づく治療の個別化が模索されていますが、共通基準の欠如や費用対効果評価、健康公平性・アクセシビリティの問題が課題として残っています。
小児神経——脳性麻痺の 27% に遺伝子変異
Lewis らが JAMA Pediatrics に発表したシステマティックレビュー・メタアナリシスは、がん以外の精密医療の可能性を鮮やかに示す研究です [10]。脳性麻痺患者 1,841 名のエクソーム解析(タンパク質をコードする遺伝子全体の解析)の結果、27% に病的または病的疑いの変異が検出され、8% に治療変更を促す actionable な所見が見つかりました。
58 の遺伝子で治療選択肢があり、未治療時は 97% が中等度から高い重症度でした。つまり、従来「原因不明」とされてきた脳性麻痺の相当数に遺伝的な原因があり、それに基づく治療介入が可能だということです。小児神経領域への精密医療の拡大を示す、質の高いエビデンスと言えます。
科学の現在地:わかっていること、わかっていないこと
確立された知見
- がんゲノム医療は臨床実装段階に入った: 日本では約 54,000 人の解析で 11.2% に国内承認薬の標的変異を検出 [14]。MTB を通じた治療選択の有効性も示されている [2][3]
- リキッドバイオプシーは再発予測に有用: MRD 陽性は再発リスク 4.95 倍、画像より平均 179 日早く検出可能 [12]
- 薬理ゲノミクスは「安全な投薬」に貢献できる: CPIC ガイドラインが 34 遺伝子・164 薬剤をカバーし、DPYD、CYP2C19、CYP2D6 など複数の遺伝子で強い推奨が確立 [5][6][7][8]
- がん以外の疾患でも精密医療は有効: 脳性麻痺の 27% に遺伝的原因、8% に actionable な所見 [10]
まだわかっていないこと
- 長期的な予後改善の実証: 遺伝子検査に基づく治療変更が最終的に生存期間を延ばすかどうかの大規模前向き試験は限られている
- 費用対効果の検証: 高額な遺伝子パネル検査の医療経済学的な妥当性は十分に検証されていない
- 民族間差異への対応: 欧米中心のデータベースに基づく判定を、日本人集団にそのまま適用できるかは検証が必要 [4]
- 非がん領域での臨床実装: 糖尿病 [11] や小児神経 [10] での知見は蓄積されつつあるが、実臨床への実装はこれから
- ゲノムデータの活用と倫理: ゲノム情報の取り扱い、遺伝差別防止、インフォームド・コンセントの標準化が必要 [13]
実践チェックリスト
がん患者・ご家族の方へ
- 標準治療が効きにくくなった場合、がん遺伝子パネル検査について主治医に相談してみてください。保険適用で受けられます(自己負担 3 割で約 16.8 万円)
- 検査は「がんゲノム医療中核拠点病院」または「がんゲノム医療拠点病院」で実施されます。全国にネットワークがあります
- 検査結果は MTB(分子腫瘍委員会)で多職種チームが解釈します。結果の説明時には、遺伝カウンセラーが同席することもあります
- 約 11% の確率で国内承認薬の標的変異が見つかりますが、見つからないこともあります。その場合でも、臨床試験への参加などの選択肢が示されることがあります
薬の効きが気になる方へ
- 薬を飲んでも効きにくい、あるいは副作用が強く出るという経験があれば、薬理ゲノミクス検査の可能性について医師に相談してみてください
- 日本では保険適用の範囲は限定的ですが、一部の抗がん剤(UGT1A1 検査など)では実施されています
- 特にクロピドグレルを処方されている方は、CYP2C19 の遺伝子型がアジア人で変異頻度が高いことを知っておくと有益です [7]
すべての方へ
- 遺伝子検査を受ける際は、遺伝カウンセリングを受けることが推奨されます。日本医学会のガイドラインは、適切なインフォームド・コンセントと遺伝情報の保護を重視しています [13]
- 遺伝子情報は本人だけでなく血縁者にも関わる情報です。検査前に「知りたくない権利」も含めた十分な説明を受けてください
- DTC(Direct-to-Consumer、消費者直販型)遺伝子検査と医療機関での遺伝子検査は質・目的が異なります。健康に関わる判断は医療機関の検査結果に基づいて行ってください
おわりに:一人ひとりの体に合わせた医療へ
外来で「この薬はあなたに合うと思います」と処方箋を書くとき、実は私たちは経験と平均的なデータに頼っている部分が少なくありません。「飲んでみて効かなければ変えましょう」——正直なところ、それが現実です。
しかし、精密医療は少しずつ、この「試行錯誤」を「科学的な予測」に変えつつあります。遺伝子パネル検査で新たな治療の扉が開く患者さんが 10 人に 1 人いる。血液検査で画像より半年早くがんの再発を察知できる。遺伝子型を調べることで、命に関わる副作用を未然に防げる。これらはもう、夢物語ではありません。
もちろん、すべての疾患で精密医療が実用段階にあるわけではなく、費用対効果や民族間差異、倫理的課題など、乗り越えるべきハードルは残っています。それでも、「一人ひとりの体に合わせた医療」という方向性は、医学の歴史の中でも最も希望に満ちた潮流の一つだと私は考えています。
ご自身やご家族の治療で「遺伝子検査」という選択肢が浮かんだとき、本記事がその一歩を踏み出すための参考になれば幸いです。
本日のまとめ
- がんゲノム医療は実装段階: 日本で約 54,000 人解析、11.2% に国内承認薬の標的変異。保険適用あり(自己負担約 16.8 万円)
- 薬理ゲノミクスで安全な投薬: DPYD、CYP2C19、CYP2D6 など遺伝子型に基づく薬剤選択・用量調整で副作用を回避できる
- がん以外にも拡大中: 脳性麻痺の 27% に遺伝的原因、糖尿病でも精密医療の国際コンセンサスが形成されつつある
関連記事:
