はじめに:眠っている間に、あなたの体は「若返って」いる
「よく寝た朝は顔色がいい」——これは単なる気のせいではありません。
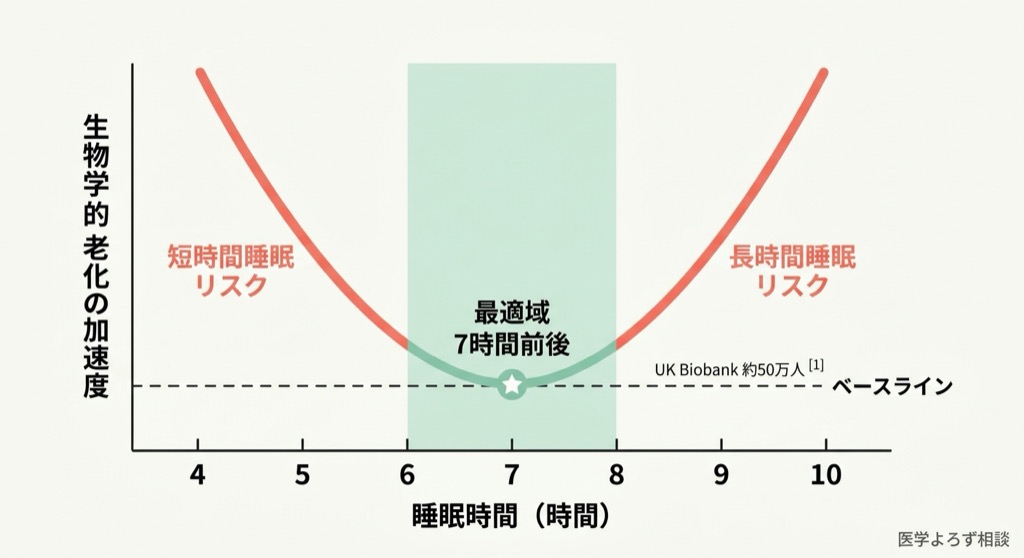
2024年、英国の約50万人を対象とした大規模研究が、衝撃的な事実を明らかにしました。睡眠時間と「生物学的老化」の関係はU字型を描く——つまり、短すぎる睡眠も長すぎる睡眠も、細胞レベルで老化を加速させるのです [1]。
さらに2025年、Cell誌に掲載された画期的な研究は、睡眠中に脳の「下水道システム」が作動し、アルツハイマー病の原因となるタンパク質を洗い流すメカニズムを、分子レベルで初めて解明しました [8]。しかも、一般的な睡眠薬がこのクリーニング機能を阻害する可能性も示されたのです。
「アンチエイジング」と聞くと、高価なサプリメントや最先端の美容医療を思い浮かべるかもしれません。しかし科学が指し示すのは、もっとシンプルな答えです。
毎晩の睡眠こそが、私たちに与えられた最も強力な「若返りの時間」である。
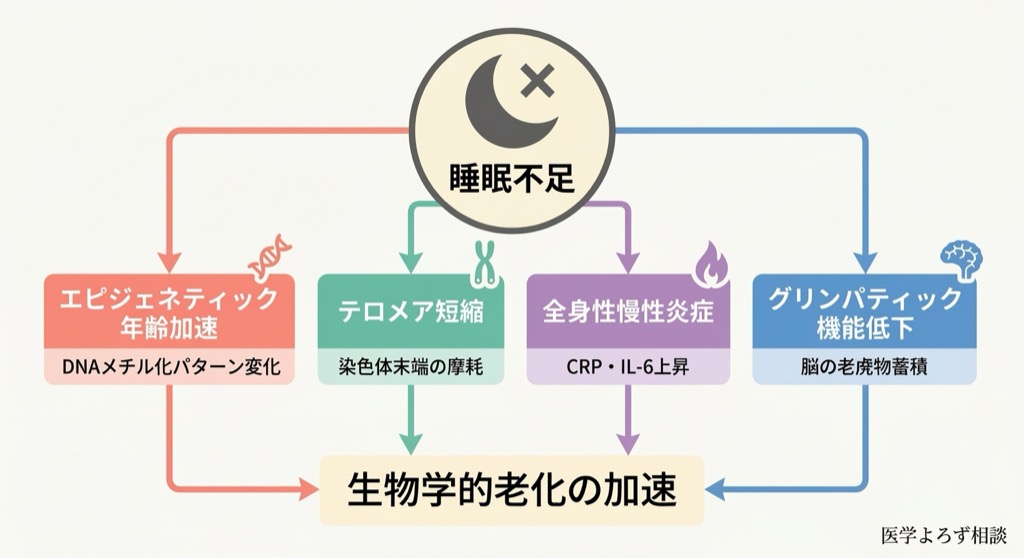
この記事では、睡眠と老化の関係を、エピジェネティクス(遺伝子の使われ方)、テロメア(染色体の末端構造)、グリンパティック系(脳の老廃物除去)、そして炎症という4つの最新科学の窓から解き明かしていきます。
睡眠の「設計図」——なぜ深い眠りが鍵なのか
私たちの睡眠は、均一な「意識のオフ」ではありません。一晩の間に、脳は精巧なプログラムに従って複数のステージを周期的に繰り返しています。
ノンレム睡眠とレム睡眠
睡眠は大きくノンレム睡眠(脳が休息するフェーズ)とレム睡眠(脳が活発に活動するフェーズ)に分けられます。ノンレム睡眠はさらにステージ1(浅い)からステージ3(深い)に分類され、ステージ3が徐波睡眠(じょはすいみん)——いわゆる「深い睡眠」です。
一晩の睡眠では、約90分の周期でノンレム睡眠とレム睡眠が交互に訪れます。重要なのは、徐波睡眠は入眠後の最初の数時間に集中するという点です。つまり、「最初の3時間」が深い睡眠のゴールデンタイムなのです。
加齢とともに失われる「深い睡眠」
悩ましいことに、この徐波睡眠は加齢とともに顕著に減少します。20代では睡眠全体の約15〜20%を占める徐波睡眠が、50代では10%前後に、70代では5%以下にまで減ってしまうことがあります。
では、この「深い睡眠の喪失」は、単に眠りが浅くなるだけの問題なのでしょうか? 答えは「否」です。2023年、JAMA Neurology誌に掲載されたFramingham Heart Studyの解析結果は、その影響の大きさを定量的に示しました。60歳以降の徐波睡眠の1%の減少あたり、認知症発症リスクが27%上昇するのです [15]。
この数字の意味は重大です。深い睡眠を守ることは、脳の老化を防ぐことと直結しているのです。
脳の「夜間清掃システム」——グリンパティック系の発見
2012年の革命
2012年、ロチェスター大学のMaiken Nedergaard教授らのグループは、脳にリンパ管に相当する老廃物除去システムが存在することを発見し、グリンパティック系(glial-lymphatic system)と名づけました [9][10]。
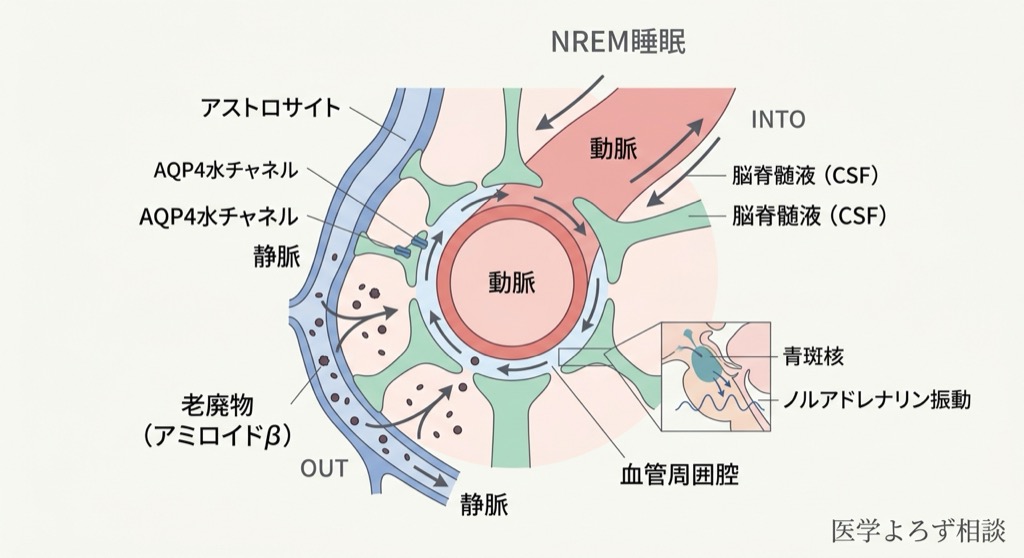
体の他の臓器では、リンパ管が老廃物を回収しています。しかし脳にはリンパ管がない——これは長年の謎でした。Nedergaard教授らが見つけたのは、アストロサイト(脳のグリア細胞の一種)が血管の周囲にトンネル状の経路を形成し、脳脊髄液を脳の奥深くまで流し込んで老廃物を洗い出す仕組みでした。
そして驚くべきことに、この脳の下水道システムは、主に睡眠中に作動するのです。覚醒時と比べて、睡眠中のアミロイドβ(アルツハイマー病の原因タンパク質)のクリアランスは約2倍に増加することが確認されています [10]。
2025年の新発見:なぜ睡眠中に「洗い流し」が起きるのか
2025年、同じNedergaardグループがCell誌に発表した研究は、グリンパティック系の駆動メカニズムをついに解明しました [8]。
鍵を握っていたのはノルアドレナリンでした。NREM睡眠(ノンレム睡眠)中、脳幹の青斑核からノルアドレナリンが周期的に放出されます。このノルアドレナリンの振動が脳血管の緩やかな収縮・拡張運動(血管運動)を引き起こし、その「ポンプ作用」によって脳脊髄液が脳内に押し込まれ、老廃物が洗い流されるのです。
この研究で臨床的に重要な発見がもう一つありました。一般的な睡眠薬であるゾルピデム(マイスリーの成分)を投与すると、ノルアドレナリン振動が抑制され、グリンパティッククリアランスが低下したのです。つまり、薬で眠っても、脳のクリーニングは十分に行われない可能性があるということです。
加齢でグリンパティック系が衰える理由
加齢に伴いグリンパティック系の効率は著しく低下します [11]。その原因として、以下のメカニズムが指摘されています。
- アクアポリン4(AQP4)の偏在消失: 若い脳ではアストロサイトの血管側にAQP4水チャネルが集中し、効率的な水の流入を可能にしています。加齢とともにこの極性配置が崩れ、水の流れが滞ります
- 脳血管の拍動低下: 動脈硬化により血管壁の弾力性が失われ、脳脊髄液を押し込む「ポンプ圧」が弱まります
- 徐波睡眠の減少: 前述のとおり、グリンパティック系を駆動する深い睡眠そのものが減少します
こうして「深い睡眠の減少→グリンパティック機能低下→タンパク質蓄積→さらなる睡眠障害」という悪循環が形成されます。Nedergaard教授はこれを「認知症への最終共通経路」と表現しています [9]。
細胞の老化時計を進める「睡眠の質」
脳だけではありません。睡眠の乱れは、全身の細胞レベルで老化を加速させることが、近年の研究で次々と明らかになっています。
エピジェネティック年齢——DNAメチル化が語る「本当の年齢」
私たちの細胞には「エピジェネティッククロック」と呼ばれる分子時計があります。DNAのメチル化パターン(遺伝子の使われ方を制御する化学修飾)を解析することで、暦年齢とは異なる「生物学的年齢」を推定できるのです。
2022年のAging Cell誌の研究は、睡眠の質の低下がエピジェネティック年齢の加速と有意に関連することを示しました [2]。眠りの質が悪い人は、実年齢より「生物学的に老けている」可能性があるのです。
2025年には、中国の中高年コホートを対象とした研究で、不規則な睡眠パターンと短時間睡眠がDNAメチル化年齢を加速させることが確認されました [3]。これはアジア人集団での貴重なエビデンスであり、日本人にも外的妥当性が高いと考えられます。
テロメアの短縮——染色体の「命の回数券」
テロメアは染色体の末端を保護するキャップ構造であり、細胞分裂のたびに少しずつ短くなります。テロメアの長さは生物学的老化のバイオマーカーとして広く研究されています。
2025年、Sleep Medicine Reviews誌に掲載された40万人超を対象としたメタ分析は、睡眠の質の低下とテロメア短縮の間に有意な関連があることを報告しました [5]。この規模のメタ分析で確認されたことは、「睡眠とテロメア老化」の関連がもはや偶然ではないことを強く示唆しています。
因果関係の証拠——メンデルランダム化解析
「睡眠の質が悪い人は老化が早い」という関連は、因果関係を意味するのでしょうか。2025年のJournal of Affective Disorders誌に掲載されたメンデルランダム化解析は、この問いに一歩踏み込みました [7]。遺伝的に睡眠障害のリスクが高い人は、エピジェネティック老化マーカーおよびフレイルティ(虚弱)マーカーにおいても加速が見られたのです。
メンデルランダム化は、遺伝的変異を「自然の実験」として利用し、交絡因子の影響を最小化する手法です。この結果は、睡眠の乱れが老化を「引き起こす」方向の因果関係を支持する重要な知見です。
「静かな炎症」——寝不足が体内に火をつける
慢性炎症(inflammaging)と睡眠
老化研究の世界では、加齢に伴う低レベルの慢性炎症を「インフラメイジング(inflammaging)」と呼びます。この「静かな火事」は、動脈硬化、糖尿病、がん、認知症といった加齢性疾患の共通基盤とされています。
では、睡眠と炎症はどのように関係するのでしょうか。
2016年、UCLAのMichael Irwin教授らが発表したランドマーク的メタ分析(72研究、5万人超)は、その関係を決定的に示しました [12]。睡眠障害はCRP(C反応性タンパク質、全身炎症のマーカー)の上昇(効果量 0.12)およびIL-6(インターロイキン6、炎症性サイトカイン)の上昇(効果量 0.20)と有意に関連していたのです。
興味深いのは、短時間睡眠だけでなく、長時間睡眠もCRPおよびIL-6の上昇と関連していたことです。ここでも「U字型」の関係が浮かび上がります。
何日寝不足が続くと炎症が起きるのか?
2025年の更新版メタ分析は、この疑問に具体的な数値で答えました [13]。35研究・887名の実験的断眠データを解析した結果、3夜以上の部分的断眠(1日約4.5時間睡眠)で、IL-6が有意に上昇(効果量 d=0.42)し、CRPも上昇(効果量 d=0.76)することが確認されました。
一方で、一晩だけの完全断眠では、これらの炎症マーカーに有意な変化は見られなかったのです。
この結果は臨床的に重要な示唆を含んでいます。一晩の徹夜よりも、数日間にわたる慢性的な睡眠不足のほうが、炎症という点ではより危険だということです。
睡眠→炎症→脳老化の連鎖
2025年のEBioMedicine誌の研究は、この炎症経路がどこに行き着くかを示しました [16]。fMRI(機能的磁気共鳴画像法)によるbrain age prediction(脳年齢予測)を用いた解析で、睡眠の質の低下が脳年齢の加速(brain age gap)と関連し、その媒介因子として全身性炎症が同定されたのです。
つまり、寝不足→全身の炎症→脳の老化加速という因果経路が、画像データで可視化されたのです。
深い眠りと「成長ホルモン」——夜の修復工場
徐波睡眠中の成長ホルモンパルス
成長ホルモン(GH)は、子どもの成長だけでなく、成人においても筋肉量の維持、脂肪代謝、骨密度の保持、認知機能に重要な役割を果たしています。
GHの分泌は一日中均一ではありません。1日のGH分泌の約70〜80%は、徐波睡眠中に集中して起こります [17]。脳下垂体からのGH分泌は、深い睡眠に入ってから約30〜60分後にピークを迎えます。
加齢によるGH分泌低下
GH分泌量は思春期にピークを迎え、その後は10年ごとに約14%ずつ低下していきます [17]。40代では若年時の約半分に、70代では3分の1以下にまで減少します。
この加齢に伴うGH分泌の低下は、サルコペニア(筋肉減少)、内臓脂肪の増加、骨密度低下、認知機能低下——いわゆる「老化のサイン」と密接に関連しています。
ここで見逃せないのが、徐波睡眠の減少とGH分泌低下が並行して進むという事実です。深い睡眠が減れば、GH分泌の「窓」も狭まる。この連鎖は、睡眠の質の低下が老化の複数の側面を同時に加速させるメカニズムの一つと考えられています。
なお、GH補充療法(GH注射)によるアンチエイジング効果については、現時点では長期安全性が確立されておらず、がんリスクへの懸念も指摘されています [17]。自然な深い睡眠を確保することこそが、GH分泌を維持する最も安全な方法です。
「何時間」よりも「質」と「一貫性」——日本のデータから
厚生労働省「睡眠ガイド2023」
2024年2月、厚生労働省は「健康づくりのための睡眠ガイド2023」を公表しました [20]。2014年版「睡眠指針」の改訂版であり、エビデンスに基づく推奨を含んでいます。成人の適正睡眠時間として6〜8時間が示されていますが、より重要なのは「休養感(ぐっすり眠れた感覚)」であると強調されています。
最適な睡眠時間は「7時間前後」
前述のUK Biobank研究 [1] は、睡眠時間と生物学的老化のU字型関連を示しました。最も生物学的老化が遅かったのは7時間前後の睡眠群です。5時間以下の短時間睡眠だけでなく、9時間以上の長時間睡眠も老化の加速と関連していました。
ただし、最適な睡眠時間には個人差があります。重要なのは「時間」だけではありません。
「毎日同じ時間に寝る」ことの科学的根拠
2023年のNHANES(米国国民健康栄養調査)データの解析は、日ごとの睡眠パラメータの変動が大きいほど、生物学的老化が加速することを示しました [4]。つまり、平日5時間・週末10時間という「寝だめパターン」は、細胞レベルでは老化を加速させている可能性があるのです。
2020年の系統的レビュー(41研究、9万人超)でも、遅い就寝時刻と大きな睡眠変動が健康上の有害アウトカムと関連することが確認されています [19]。
このエビデンスが示すのは、シンプルなメッセージです。「何時間寝るか」と同じくらい、「毎日同じ時間に寝て、同じ時間に起きる」ことが重要なのです。
科学の現在地:わかっていること、いないこと
確立された知見
- 睡眠の質の低下は、エピジェネティック年齢加速およびテロメア短縮と有意に関連する(メタ分析レベルで確認) [2][5]
- グリンパティック系は主に睡眠中に作動し、加齢とともに効率が低下する [9][10][11]
- 数日間の慢性的な睡眠不足(4.5時間×3夜以上)は全身性炎症マーカーを上昇させる [12][13]
- 徐波睡眠の減少は認知症リスクの独立した予測因子である [15]
- 睡眠時間と生物学的老化にはU字型の関連があり、7時間前後が最適域である [1]
未解明点・現在の限界
- グリンパティック系の研究の多くはマウスモデルに基づいており、ヒトでの直接的な測定方法はまだ確立されていない [8][10]
- 「睡眠の質を改善すれば生物学的老化を逆転できるか」を直接示した介入RCTはまだない
- 睡眠薬(ゾルピデム等)のグリンパティック系への影響は動物実験レベルであり、ヒトでの確認が必要 [8]
- エピジェネティック年齢加速が実際の健康アウトカム(寿命、疾患発症)にどの程度直結するかは研究途上
- 個人の最適睡眠時間を決定する遺伝的・環境的要因の解明は不十分
「若返り睡眠」のための実践チェックリスト
エビデンスから導かれる具体的なアクションを整理します。
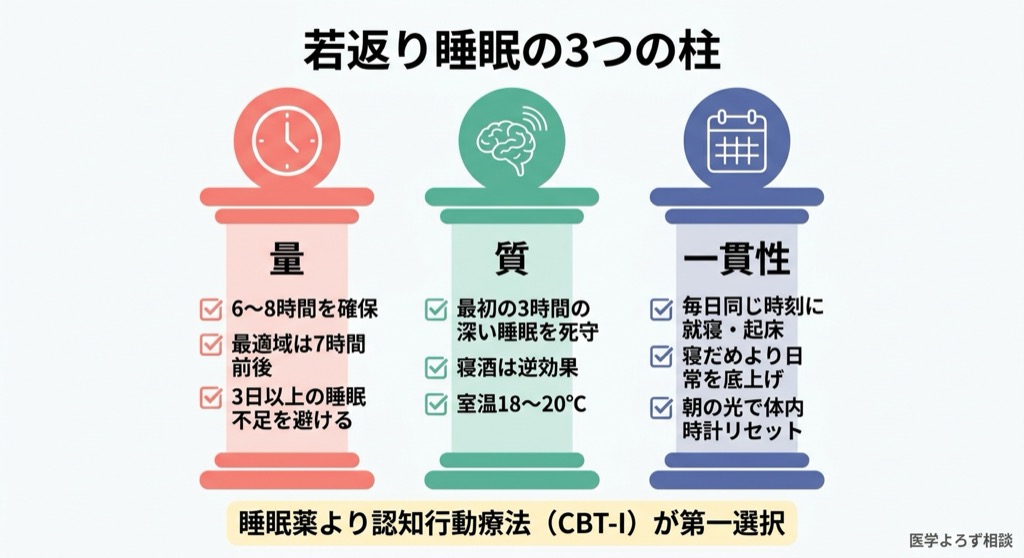
睡眠の「量」を確保する
- 成人は6〜8時間を目安にする(厚労省推奨 [20])
- 生物学的に最も老化が遅い睡眠時間は7時間前後 [1]
- 5時間以下の睡眠が3日以上続くと炎症マーカーが上昇しはじめる [13]
睡眠の「質」を高める
- 入眠後3時間の深い睡眠を死守する: 成長ホルモン分泌のゴールデンタイム [17]
- 就寝前のアルコールは深い睡眠を減少させる——「寝酒」は逆効果
- 寝室の温度は18〜20℃が徐波睡眠を増やすとされる
睡眠の「一貫性」を守る
- 就寝時刻と起床時刻を平日・休日問わず一定にする [4][19]
- 寝だめよりも日常の睡眠時間を底上げする
- 体内時計のリセットには朝の光暴露が最も効果的
睡眠薬に頼りすぎない
- ベンゾジアゼピン系・Z薬(ゾルピデム等)は深い睡眠を抑制する可能性がある [8]
- 不眠症の第一選択治療は認知行動療法(CBT-I)であり、薬物療法ではない
- 睡眠薬の使用は医師と相談の上で最小限に
おわりに:最も身近で、最も過小評価されている「抗老化戦略」
外来で「アンチエイジングのためにNMNサプリを飲んでいます」「テロメアを伸ばすにはどうしたら?」と質問されることがあります。しかし正直にお伝えすると、NMNサプリのヒトでの長期有効性はまだ確立されておらず、テロメラーゼを安全に活性化する方法も見つかっていません。
一方で、毎晩の深い睡眠がエピジェネティック年齢を若く保ち、テロメアの短縮を遅らせ、脳の老廃物を洗い流し、炎症を抑え、成長ホルモンの分泌を維持するというエビデンスは、複数の大規模研究で繰り返し確認されています。
睡眠は、無料で、毎日実践でき、そして科学的根拠が最も蓄積されたアンチエイジング戦略です。
今夜、スマートフォンを置いて、少しだけ早くベッドに入ってみてください。その習慣が10年後の「生物学的年齢」を変えるかもしれない——そう考えるだけの科学的根拠は、すでに十分にそろっています。
本日のまとめ
- 睡眠と老化の関係: 睡眠の質・量・一貫性は、エピジェネティック年齢、テロメア長、脳のクリアランス機能、全身性炎症を通じて生物学的老化に直接影響する
- 最適な睡眠の条件: 7時間前後の睡眠を、毎日同じ時間に取り、最初の3時間の深い睡眠を確保すること
- 判断に迷ったら: 慢性的な不眠や日中の強い眠気がある場合は、まずかかりつけ医に相談を。不眠症の第一選択治療は睡眠薬ではなく認知行動療法(CBT-I)です
関連記事:
