はじめに:あなたの染色体は、今日も少しずつ短くなっている
2004年、カリフォルニア大学サンフランシスコ校(UCSF)の研究チームが、科学史に残る発見を報告しました。
慢性的なストレスを抱える母親たちの血液を調べたところ、最もストレスが高い女性の染色体末端は、低ストレスの女性と比べて約10年分も短いことがわかったのです [1]。
この「染色体末端」こそが、テロメアと呼ばれる構造です。
テロメアは「命の回数券」「老化の砂時計」——メディアではそんな表現で紹介されます。SNSを開けば「テロメアを伸ばすサプリ」「テロメア年齢測定キット」の広告が目に飛び込んできます。
しかし、テロメアの科学はそれほど単純ではありません。
2025年のメンデルランダム化研究(遺伝子を使って因果関係を推定する手法)では、テロメア長と寿命には因果関係がない可能性すら報告されています [2]。「テロメアが長い=長生き」という方程式は、想像以上に複雑なのです。
この記事では、2026年4月時点で発表されている16件の主要論文——メタ分析、RCT(無作為化比較試験)、メンデルランダム化研究を中心に、テロメアの「本当の姿」を解き明かします。
運動はテロメアを守る? ストレスは本当にテロメアを縮める? テロメア測定を受ける意味はある? そして遺伝子治療でテロメアを伸ばす時代は来るのか?
科学的エビデンスをもとに、一つずつ紐解いていきましょう。
テロメアとは何か——染色体の「靴紐キャップ」
末端を守る6文字の繰り返し
私たちの細胞の核には、46本の染色体が収められています。染色体はDNAがタンパク質に巻きついた構造ですが、その両端に位置するのがテロメア(telomere)です。
テロメアは「TTAGGG」という6塩基の配列が数千回繰り返された構造で、出生時にはおよそ10,000〜15,000塩基対の長さがあります。靴紐の先端についているプラスチック製のキャップ(アグレット)を想像してください。このキャップがなければ、靴紐はほどけてしまう。テロメアはまさに、染色体がほどけたり、互いにくっついたりするのを防ぐ「保護キャップ」です。
テロメアの表面は、シェルタリン(shelterin)と呼ばれる6種類のタンパク質複合体で覆われています。シェルタリンは、テロメアが「損傷したDNA」と誤認されるのを防ぎ、不要なDNA修復反応が起きないようにしています [3]。
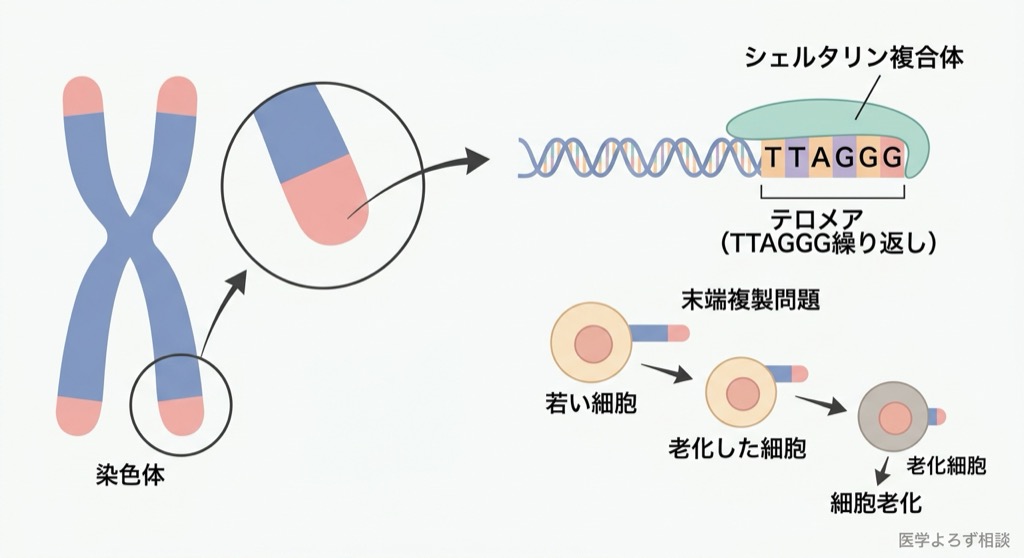
末端複製問題——細胞分裂のたびに失われるもの
ここで問題があります。細胞が分裂するとき、DNAは複製されますが、線状染色体の末端は完全には複製できないのです。これは1970年代にJames WatsonとAlexei Olovnikovが独立に指摘した「末端複製問題(end-replication problem)」と呼ばれる分子生物学の根本的な制約です。
その結果、細胞分裂のたびにテロメアは約30〜200塩基対ずつ短くなっていきます。テロメアがある限界まで短くなると、シェルタリンがDNAを覆いきれなくなり、DNA損傷応答が発動します。細胞は「細胞老化(senescence)」と呼ばれる状態に入り、分裂を停止するか、アポトーシス(プログラム細胞死)を起こします。
これがテロメアの「回数券」的な側面です。テロメアが短くなるにつれ、分裂能力が失われていく。
テロメラーゼ——「回数券を補充する酵素」
しかし、すべての細胞がテロメアの短縮に無力なわけではありません。
テロメラーゼ(telomerase)は、テロメアのTTAGGG配列を伸長させる酵素です。TERT(テロメラーゼ逆転写酵素)とTERC(テロメラーゼRNA構成要素)の2つのサブユニットからなり、テロメアの末端にDNA配列を付加することで、短縮を相殺します。
テロメラーゼは、幹細胞や免疫細胞、生殖細胞では活発に働いています。しかし、体細胞の大部分ではテロメラーゼ活性は極めて低い——これが、加齢とともにテロメアが短縮する主な理由です。
Elizabeth Blackburn、Carol Greider、Jack Szostakの3名は、テロメラーゼの発見と染色体保護メカニズムの解明により、2009年にノーベル生理学・医学賞を受賞しました。
ストレスがテロメアを「10年分」縮める——Epel & Blackburnの衝撃
介護ストレスの母親たちが教えてくれたこと
2004年、Elissa EpelとElizabeth Blackburn(のちのノーベル賞受賞者)のチームは、心理的ストレスとテロメア短縮の関係を初めて示す論文をPNASに発表しました [1]。
研究対象は58名の健康な閉経前女性。慢性疾患を持つ子どもを介護する母親39名と、健常児の母親19名です。
結果は衝撃的でした。
- 最も知覚ストレスが高い女性は、低ストレスの女性と比べてテロメアが約10年分短い
- 高ストレス群では、酸化ストレスが有意に上昇
- テロメラーゼ活性は有意に低下
「10年分の老化」——この数字が世界中のメディアを駆け巡り、テロメア研究は精神神経免疫学の中心テーマとなりました。
メカニズム——なぜストレスがテロメアを縮めるのか
2022年、同じUCSFのLinとEpelは、ストレスからテロメア短縮に至る分子メカニズムを体系的にまとめた包括的レビューを発表しました [3]。
その経路は、驚くほど複雑で、かつ巧妙に連鎖しています。
第1の経路:グルココルチコイド(コルチゾール)
慢性的なストレスは、視床下部-下垂体-副腎(HPA)軸を持続的に活性化し、コルチゾールの過剰分泌を引き起こします。高コルチゾール環境は、テロメラーゼの発現を直接抑制し、テロメアの修復能力を低下させます。
第2の経路:活性酸素種(ROS)
ストレスに伴うコルチゾール上昇は、ミトコンドリアの機能不全を引き起こし、活性酸素種(ROS)の産生を増加させます。ROSはテロメアのグアニン豊富な配列(TTAGGGのG)を優先的に酸化し、テロメアDNAに直接的な損傷を与えます。
テロメアDNAは、ゲノムの他の部位と比べてROS感受性が高いことが知られています。これは、テロメアのGGG配列が酸化されやすいためです。
第3の経路:慢性炎症
ストレスによるNF-κBの活性化は、IL-6やTNF-αなどの炎症性サイトカインの産生を促進します。慢性炎症はテロメラーゼ活性を抑制するとともに、免疫細胞の過剰な分裂を促し、テロメア短縮を加速させます。
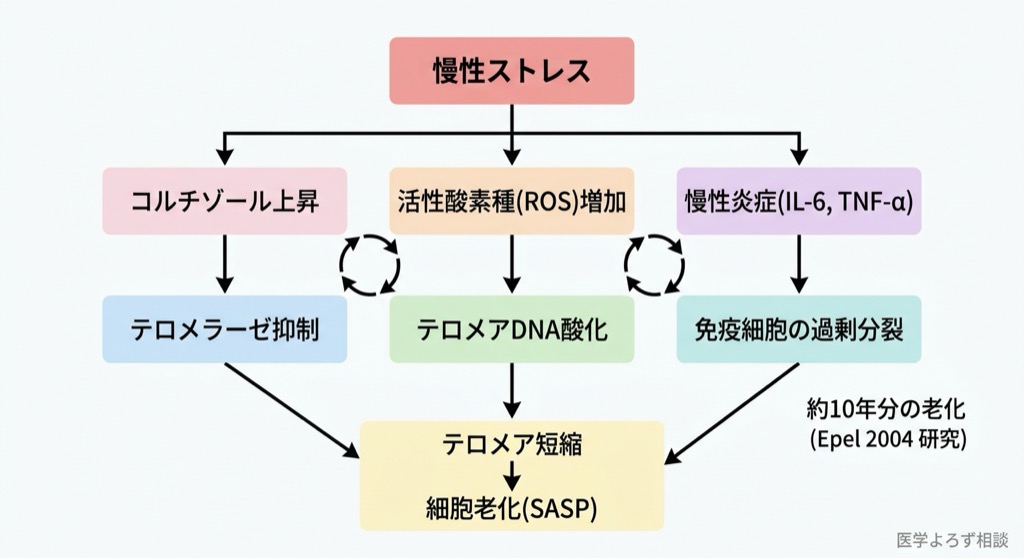
重要なのは、これら3つの経路が正のフィードバックループを形成していることです。コルチゾールがROSを増やし、ROSがミトコンドリアを傷つけ、ミトコンドリアの機能不全がさらにROSを増やす。炎症がテロメアを縮め、短縮したテロメアが細胞老化を引き起こし、老化細胞がさらに炎症性物質を放出する——いわゆるSASP(老化細胞関連分泌表現型)です。
ミトコンドリア-テロメア軸という新概念
2026年に発表されたTippairoteらの視点論文は、この連鎖をさらに一歩進めた「バイオエネルギー負債モデル」を提唱しています [4]。
このモデルでは、テロメア短縮の真の上流制約はエネルギーの不足であると考えます。ストレスによるエネルギー需要の増大と、ミトコンドリアのエネルギー供給能力の低下——この不均衡が、テロメラーゼ活性の低下を引き起こし、結果としてテロメアが短縮する。
つまり、テロメラーゼ活性は「早期の、エネルギー感受性のあるストレスマーカー」であり、テロメア短縮そのものは「遅延した構造的帰結」だというのです。
この視点は、前回の記事で取り上げたNAD+(ミトコンドリア機能に不可欠な補酵素)との接点を示唆します。NAD+の低下がミトコンドリア機能を損ない、それがテロメア維持能力の低下につながる——老化の複数のホールマークが、エネルギー代謝という共通の基盤で結びついているのです。
女性はより影響を受けやすい?
2024年のSouza-Talaricoらによるシステマティックレビュー(15研究、9,446名)は、興味深い性差を明らかにしました [5]。
心理的ストレスとテロメア短縮の関連は、女性で特に強いことが示されたのです。重大なライフストレッサー(介護、死別、離婚など)を経験している女性では、ストレス反応の生物学的指標(コルチゾール、IL-6、血圧)もテロメア長と有意に関連していました。
さらに、O'Donovanらの研究では、悲観的な性格傾向そのものがテロメア短縮(β=−0.68, p=0.001)およびIL-6上昇(β=0.50, p=0.02)と独立して関連することが示されています [6]。興味深いことに、楽観主義はテロメア長と有意な関連を示しませんでした。
「ポジティブ思考がテロメアを守る」のではなく、「慢性的な悲観がテロメアを傷つける」——この非対称性は、ストレス管理の重要性を改めて浮き彫りにします。
運動はテロメアの味方——ただし「やりすぎ」は敵になる
メタ分析が示す明確なエビデンス
運動がテロメアを保護するというエビデンスは、近年のメタ分析で急速に蓄積されています。
2025年、SunらはRCT(無作為化比較試験)のみを対象としたメタ分析を発表しました [7]。結果は明快です。
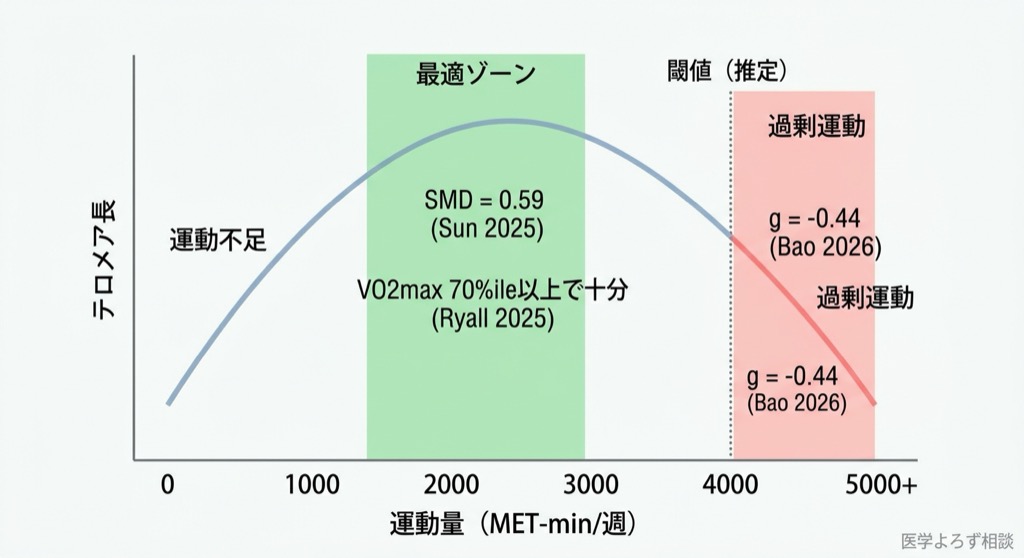
- テロメア長の維持:SMD = 0.59(95%CI 0.14–1.06, p=0.01)
- テロメラーゼ活性の増強:SMD = 0.35(95%CI 0.20–0.51, p<0.00001)
- 有酸素運動がテロメラーゼ活性に最も一貫した効果
- 有意な効果には16週以上の介入が必要
つまり、RCTという最も信頼性の高い研究デザインで、「運動はテロメアを守り、テロメラーゼを活性化する」ことが確認されたのです。
同じ2025年、Sánchez-Gonzálezらは12件のシステマティックレビューを統合したアンブレラレビューを発表しました [8]。22件の一次研究から算出された全体効果量は0.28(95%CI 0.118–0.439)。30週未満の介入でより大きな効果が見られ、HIIT(高強度インターバルトレーニング)が中等度の効果を示しました。
Ryall & Denham(2025年)のメタ分析は、VO2max(最大酸素摂取量)とテロメア長の関係に焦点を当てています [9]。VO2maxが年齢・性別調整後の70パーセンタイル以上の人は、それ以下の人よりテロメアが有意に長い(SMD=0.36)。しかし、70〜90パーセンタイルと90パーセンタイル以上の間には差がありませんでした。
この結果は実践的に重要なメッセージを含んでいます——過度な持久力トレーニングは不要であり、中等度の有酸素能力を維持するだけでテロメア保護には十分だということです。
複合運動(筋トレ+有酸素)が最も効果的
Buttetら(2022年)のメタ分析は、20研究・2,995名を対象に、生活習慣介入のテロメアへの効果を検証しました [10]。
注目すべきは、運動の種類による効果の違いです。
- 運動±食事介入群:テロメア長が有意に増加(ES=0.17)
- 対照群:テロメア長が短縮(ES=−0.32)
- 筋力トレーニングと有酸素運動の複合が、単独よりも効果的
有酸素運動だけでも効果はありますが、筋トレを組み合わせることでさらにテロメア保護効果が高まる——これは、一般的な運動ガイドライン(週150分の中等度有酸素運動+週2回の筋力トレーニング)を支持するエビデンスです。
過度な運動はテロメアを「傷つける」
しかし、2026年に発表されたBaoらのメタ分析は、重要な警告を発しています [11]。
31研究を分析した結果、疲弊的・激烈な運動はテロメア長を有意に短縮させる(g=−0.44, 95%CI −0.83 to −0.03)ことが示されたのです。
さらに、酸化ストレスマーカー(8-OHdG)の上昇、炎症性サイトカイン(IL-6)の増加、VO2maxの低下も確認されました。
メタ回帰分析では、約4,000 MET-min/週を超えるとIL-6反応が急激に増加する閾値が示唆されています。4,000 MET-min/週とは、たとえば時速8kmのランニングを週に約7時間行う計算になります。
つまり、運動とテロメアの関係は直線的ではなく、逆U字型(または適量で最大効果、過剰で害)の関係にあるのです。
この「ゴルディロックスゾーン」——多すぎず少なすぎない最適な運動量——の存在は、マラソンランナーやウルトラトレイルの愛好者にとって重要な示唆を含んでいます。ただし、4,000 MET-min/週という閾値はメタ回帰による推定値であり、個人差が大きい点には注意が必要です。
Ornish研究が示した「生活習慣処方箋」
3ヶ月でテロメラーゼが上がった
Dean Ornishといえば、植物性食事と生活習慣改善で心臓病の進行を逆転させた先駆的研究で知られる医師です。そのOrnishが、Blackburnのチームと組んで行った研究が、テロメア分野に大きなインパクトを与えました。
2008年、Lancet Oncologyに発表されたパイロット研究 [12] では、低リスク前立腺がん男性30名が、以下の包括的生活習慣改善プログラムに3ヶ月間取り組みました。
| 介入内容 | 詳細 |
|---|---|
| 食事 | 植物性中心、低脂肪(脂肪10%以下) |
| 運動 | 中等度の有酸素運動、週6日・30分 |
| ストレス管理 | ヨガ、瞑想、呼吸法、毎日60分 |
| 社会的支援 | 週1回のグループセッション |
結果、わずか3ヶ月で末梢血単核球のテロメラーゼ活性が有意に増加しました(p=0.031)。しかもテロメラーゼの増加は、LDLコレステロールの減少(r=−0.36)と心理的苦痛の減少(r=−0.35)と関連していました。
5年後——テロメアは本当に伸びていた
さらに注目すべきは、2013年の5年追跡データです [13]。
介入群10名と対照群25名を比較した結果:
- 介入群:テロメア長が+0.06 T/S units増加
- 対照群:テロメア長が−0.03 T/S units減少
- 群間差:p=0.03
さらに、生活習慣の遵守度が高いほどテロメアの増加幅が大きいという用量反応関係が確認されました(β=0.07/パーセンタイルポイント, p=0.005)。
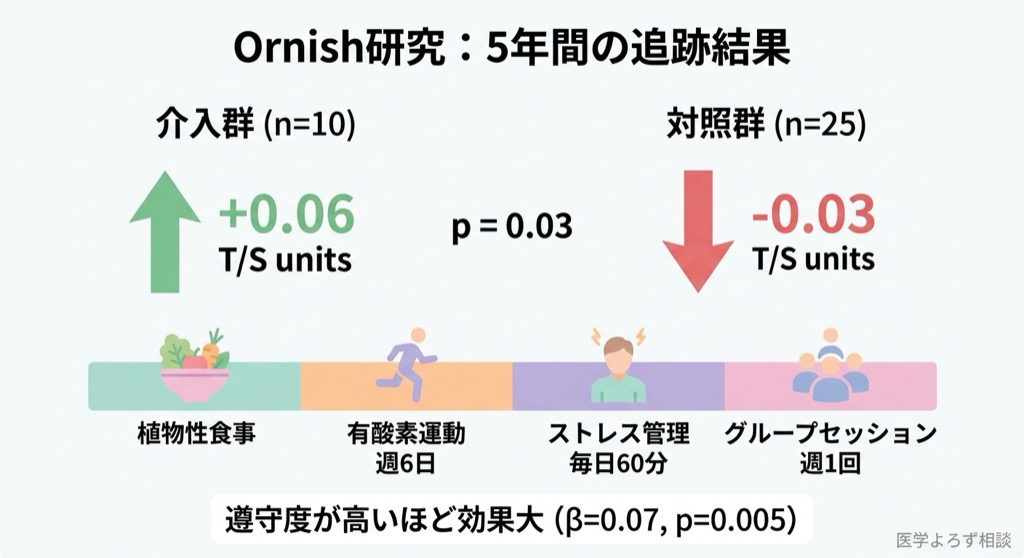
この研究は、少人数(n=35)かつ非ランダム化という限界がありますが、「生活習慣改善でテロメアが5年間にわたり維持・増加する」ことを示した唯一の長期追跡研究として、現在も頻繁に引用されています。
用量反応関係が示された点は特に重要です。「すべてを完璧にしなくても、やった分だけ効果がある」——これは、忙しい日常の中で生活改善に取り組む人々にとって、心強いメッセージです。
食品由来の抗酸化物質でもテロメアは守れる
2025年のWattanathornらによるRCTは、アントシアニン(ブルーベリーや紫米に含まれる抗酸化物質)を豊富に含む色素米の効果を検証しました [14]。
45〜65歳の90名を3群(プラセボ/低用量/高用量)に分け、12週間摂取させた結果:
- 低用量群:テロメア長・テロメラーゼ活性・炎症マーカーが改善
- 高用量群:認知機能・シワ・動脈硬化指数・酸化ストレスが改善
興味深いことに、テロメアへの効果は低用量で、他の効果は高用量で見られるという非直線的な用量反応を示しました。この研究は単施設のパイロット的RCTですが、食品由来の抗酸化物質によるテロメア保護の可能性を示すエビデンスとして注目されます。
なお、ビタミンDとテロメア長の関連を調べた大規模メタ分析(21研究、185,191名)では、血清ビタミンD値とテロメア長に正の関連が確認されています(β=0.04)[15]。効果量は小さいものの、特に女性とビタミンD欠乏者で関連が強く、ビタミンD欠乏の是正がテロメア保護に寄与する可能性が示唆されています。
テロメア測定は受けるべきか——「バイオマーカー」としての限界
メンデルランダム化が突きつけた不都合な真実
近年、テロメア測定を商業的に提供するクリニックが増えています。「テロメア年齢」を測定し、生物学的な若さを数値化するというコンセプトは魅力的に映ります。
しかし、2025年に発表されたSchoolingらのメンデルランダム化(MR)研究は、この期待に冷水を浴びせる結果を示しました [2]。
UK Biobank約50万人のデータを用いたこの研究では、遺伝的に決定されるテロメア長と寿命の因果関係を検証しました。MRは、遺伝子変異を「自然のランダム化」として利用することで、観察研究では排除できない交絡因子の影響を除外できる手法です。
結果は明確でした。
- テロメア長は男性の寿命と因果的に関連していない(0.17年/SD, 95%CI −0.54 to 0.88)
- 女性でも同様に有意な関連なし(0.04年/SD, 95%CI −0.88 to 0.96)
- エピジェネティック時計(GrimAge, PhenoAge, HannumAge)も寿命との因果関連なし

つまり、「テロメアが長い人は長生きする」という因果関係は、最も厳密な因果推論の手法では支持されなかったのです。
テロメア測定に意味はないのか?
ただし、この結果は「テロメアには何の意味もない」という意味ではありません。
MR研究にはいくつかの限界があります。遺伝的に決定されるテロメア長は、生涯を通じたテロメアの短縮速度とは異なります。生まれつきテロメアが長い人でも、その後の生活習慣やストレスによって急速に短縮する可能性があり、MRではこの動的な変化を捉えきれません。
現時点でのコンセンサスは以下のようにまとめられます。
テロメア測定で「わかること」
- 一時点での生物学的老化のおおまかな目安
- 同年齢集団の中での相対的な位置
- 生活習慣改善の効果を追跡するモチベーションツール
テロメア測定で「わからないこと」
- あなたが何歳まで生きるか
- 特定の疾患にかかるかどうか
- テロメアを「伸ばす」ための個別的な処方
テロメア測定を受けること自体に害はありませんが、現時点では臨床的な治療方針を左右するほどの有用性は確立されていません。「健康のバロメーター」としては一定の参考価値がありますが、測定結果に一喜一憂する必要はないでしょう。
テロメア治療の最前線——遺伝子治療は「夢」から「現実」へ
Blasco研究——マウスの寿命を24%延ばした遺伝子治療
2012年、スペイン国立がん研究センター(CNIO)のMaria Blascoのチームは、テロメラーゼ遺伝子治療の概念実証研究をEMBO Molecular Medicineに発表しました [16]。
この研究では、AAV(アデノ随伴ウイルス)ベクターを使って、成体マウス(1歳)と老齢マウス(2歳)にマウスTERT遺伝子を導入しました。
結果は驚異的でした。
| アウトカム | 1歳群 | 2歳群 |
|---|---|---|
| 寿命の中央値延長 | +24% | +13% |
| インスリン感受性 | 改善 | 改善 |
| 骨密度 | 改善 | 改善 |
| 神経筋協調 | 改善 | 改善 |
| がん発生率 | 増加なし | 増加なし |
最も重要なポイントは、テロメラーゼの過剰発現にもかかわらず、がんの発生率が増加しなかったことです。テロメラーゼはがん細胞で高発現していることが知られており、テロメラーゼの活性化は「がんを促進するのではないか」という懸念がありました。しかし、成体以降に発現させた場合、この懸念は当てはまらないことが示されたのです。
ヒトでの初の臨床成果
マウスからヒトへの橋渡しも、着実に進んでいます。
2025年、米国のElixirgen Therapeutics社は、テロメア生物学疾患(TBD:先天的にテロメアが極端に短い希少疾患群)の患者に対する遺伝子治療EXG-34217の初期臨床結果をNEJM Evidenceに報告しました。最初の2名の患者で、テロメアの持続的な伸長が確認され、24ヶ月および5ヶ月の観察期間中に安全性の問題は認められませんでした。
ただし、これは「老化を逆転させる」治療ではなく、テロメアが先天的に短い希少疾患への治療であることを強調しておきます。健常者のアンチエイジング目的でのテロメラーゼ遺伝子治療は、まだ臨床試験段階にすら到達していません。
「テロメラーゼ活性化サプリ」の現実
市販されている「テロメラーゼ活性化」を謳うサプリメントの多くは、アストラガルス(黄耆)由来のシクロアストラゲノールを主成分としています。in vitro(試験管内)ではテロメラーゼ活性の増加が報告されていますが、ヒトでのRCTは限られており、テロメア長を有意に延長したという確固たるエビデンスは確立されていません。
現時点では、サプリメントよりも、次のセクションで紹介する「エビデンスに基づく生活習慣改善」のほうが、はるかに科学的根拠が強固です。
科学の現在地:わかっていること、いないこと
確立された知見(エビデンスレベルが高い)
- テロメアは加齢とともに短縮し、細胞老化・疾患リスクと関連する
- 慢性的な心理的ストレスは、テロメア短縮を加速させる [1][3][5]
- 中等度の有酸素運動はテロメア長を維持し、テロメラーゼ活性を増強する [7][8][9]
- 筋力トレーニングと有酸素運動の複合がより効果的 [10]
- 包括的な生活習慣改善(食事・運動・ストレス管理)はテロメアを保護する [12][13]
有望だがさらなる検証が必要
- 過度な運動(約4,000 MET-min/週超)がテロメアを縮める可能性 [11]
- ビタミンD充足とテロメア長の正の関連 [15]
- アントシアニンなど食品由来抗酸化物質のテロメア保護効果 [14]
- ミトコンドリア-テロメア軸の「バイオエネルギー負債」モデル [4]
未解明・議論中
- テロメア長と寿命の因果関係(MR研究では否定的 [2])
- テロメア測定の臨床的有用性
- テロメラーゼ遺伝子治療の長期安全性(ヒト)
- テロメア短縮速度の最適な測定・評価法
実践チェックリスト:テロメアを守るためにできること
エビデンスに基づく「テロメア保護戦略」を、実践しやすい形でまとめました。
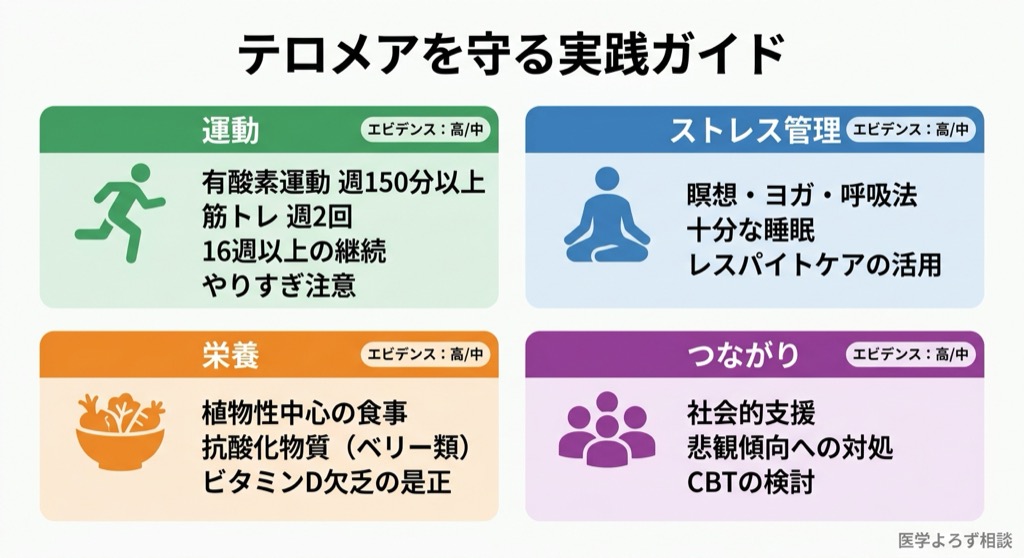
運動(エビデンスレベル:高)
- 有酸素運動:週150分の中等度(早歩き、軽いジョギング)またはそれ以上 [7][8]
- 筋力トレーニング:週2回以上。有酸素との複合がより効果的 [10]
- 16週以上の継続が効果発現に必要 [7]
- やりすぎ注意:極端な長距離走やオーバートレーニングは逆効果の可能性 [11]
- 目安:VO2maxを年齢・性別の70パーセンタイル以上に維持。それ以上の向上はテロメア保護には不要 [9]
ストレス管理(エビデンスレベル:中〜高)
- 瞑想・ヨガ・呼吸法:Ornish研究では毎日60分のストレス管理を実施 [12][13]
- 慢性的な悲観傾向への対処:必要に応じて認知行動療法(CBT)の検討 [6]
- 介護者・高ストレス環境にある方:レスパイトケア(一時的な休息)を積極的に活用 [1][5]
- 十分な睡眠:テロメア保護に直接のRCTはないが、概日リズムの維持がミトコンドリア機能に寄与 [4]
栄養(エビデンスレベル:中)
- 植物性食品を中心とした食事:Ornish研究では低脂肪植物性食事を採用 [12][13]
- 抗酸化物質が豊富な食品:ベリー類、紫色の食品(アントシアニン)[14]
- ビタミンD:欠乏の是正(特に女性)[15]。血液検査で25(OH)D値を確認し、不足があれば補充
- 地中海食:直接のテロメアRCTは少ないが、抗炎症作用を通じた保護効果が期待される
受診の目安
- テロメア測定は現時点では「任意」——保険適用はなく、自費検査(3〜5万円程度)
- 測定結果に基づく治療方針の変更は現時点では推奨されない
- テロメア測定を受けるより、上記の生活習慣改善に注力するほうが、エビデンスに基づく選択
おわりに:「テロメアを守る」とは「丁寧に生きる」こと
テロメアの科学は、過去20年で目覚ましい進歩を遂げました。
Epel & Blackburnが「ストレスがテロメアを縮める」ことを示してから、運動がテロメアを守ること、生活習慣の包括的改善がテロメアを伸ばすことまで——エビデンスは着実に積み上げられています。
しかし同時に、テロメアの科学は「テロメアを長くすれば万事解決」という単純な答えを否定してもいます。メンデルランダム化研究が示すように、テロメア長と寿命の因果関係すら、まだ確定していないのです。
私が臨床医として感じるのは、テロメアを守る行為——適度に動き、よく食べ、ストレスを和らげ、人とのつながりを大切にする——は、結局のところ「健康的に生きる」ことそのものだということです。テロメアは、その「丁寧な生き方」が細胞レベルで報われていることを教えてくれる、ひとつの窓なのかもしれません。
特別なサプリメントも、高額な測定キットも、今すぐ必要ではありません。今日から始められること——週末の散歩、深呼吸の習慣、色とりどりの食卓——がテロメアを守る最も確実な方法です。
遺伝子治療の時代はゆっくりと、しかし確実に近づいています。しかしそれが一般の人々に届くまでの間、科学が教えてくれる「今できる最善」を、一つずつ実践していきましょう。
本日のまとめ
- テロメアの本質: 染色体末端の保護キャップ。加齢とストレスで短縮し細胞老化を促すが、「テロメアが長い=長生き」という単純な因果関係は確定していない
- 守るための科学: 中等度の運動(週150分+筋トレ週2回)、ストレス管理、植物性中心の食事が、複数のメタ分析で支持される最もエビデンスの強い戦略
- 判断に迷ったら: 高額な測定やサプリに投資するより、今日から「動く・食べる・休む」を少しだけ改善する。テロメアは「丁寧な日常」に応えてくれる
関連記事:
