はじめに——「検診を受けなさい」の一言では済まない理由
日本のがん検診受診率は、胃がん約48%、大腸がん約47%、肺がん約53%、乳がん約47%、子宮頸がん約43%です [1]。欧米諸国が70~80%の受診率を達成していることを考えると、日本は「検診後進国」と言わざるを得ません。
しかし、「だから検診を受けましょう」と勧めるだけでは、この記事を書く意味がありません。
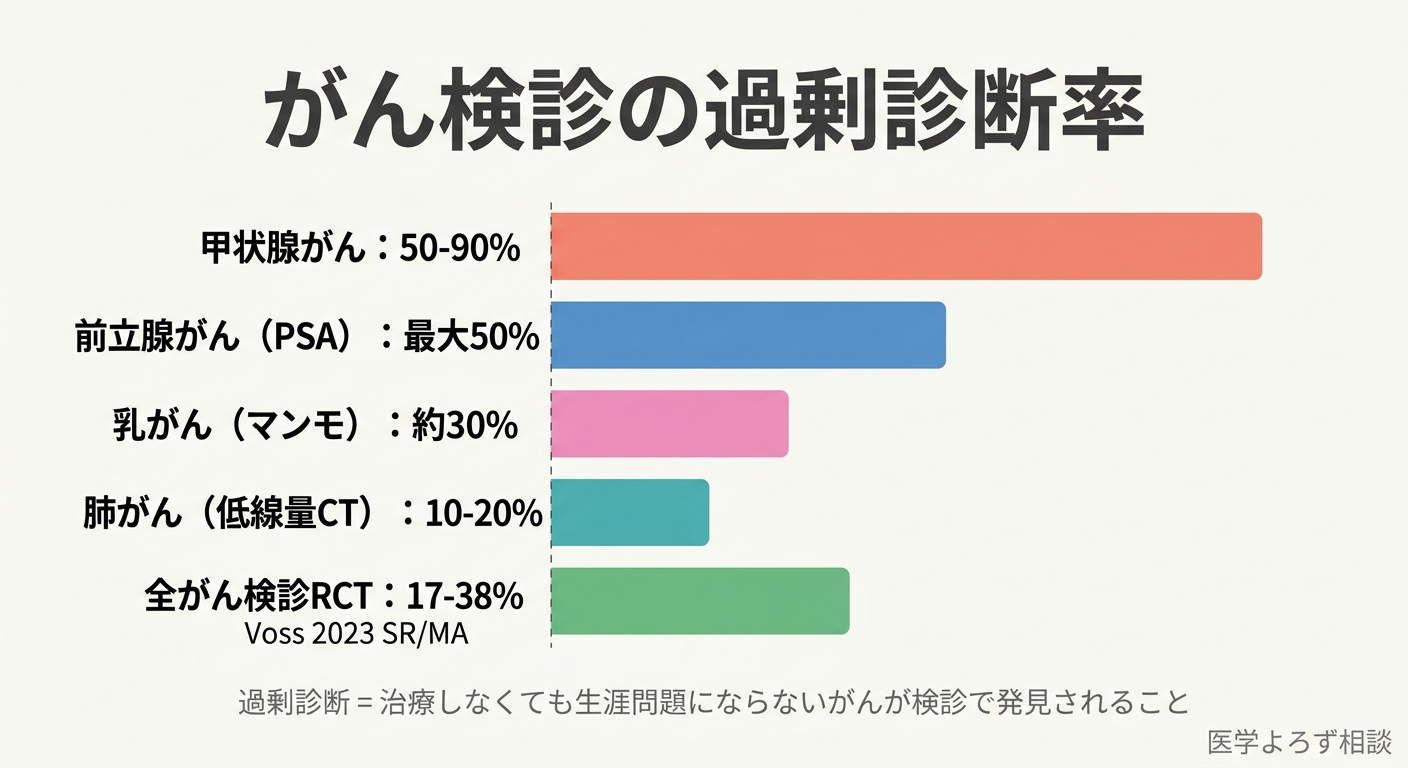
なぜなら、がん検診には「利益」と「害」の両面があるからです。検診によって救われる命がある一方で、治療しなくても問題にならなかった「がん」が見つかり、不要な手術や治療を受けてしまうリスクもあります。これを過剰診断(治療しなくても生涯問題を引き起こさないがんが検診で発見されること)と呼びます。
2023年のシステマティックレビュー(SR: 複数の研究結果を統合した最も信頼性の高い研究デザイン)では、がん検診のランダム化比較試験(RCT: 対象者を無作為に2群に分けて効果を比較する試験デザイン)19件を再分析した結果、過剰診断率は17%~38%に達することが明らかになりました [2]。しかもこの数値は、バイアスリスクの高い試験を除外した「控えめな推定」であり、実際の過剰診断はさらに多い可能性があります。
この記事では、日本の5大がん検診のエビデンスを正直に整理し、「検診を受けるべきか」をあなた自身が判断できる情報を提供します。さらに、多がん早期発見検査(MCED: Multi-Cancer Early Detection)や液体生検といった新技術の「期待」と「慎重さ」についても、最新の科学的知見に基づいて解説します。
5大がん検診の概要——日本のガイドラインが推奨する方法
日本の対策型がん検診は、国立がん研究センターのガイドラインに基づいて5つのがん種を対象としています [1][8]。

胃がん検診
対象は50歳以上、2年に1回。検査方法は胃部X線検査(バリウム検査)または胃内視鏡検査(推奨グレードB)です。日本は世界でも胃がん罹患率が高い国であり、ヘリコバクター・ピロリ菌感染が主要なリスク因子です。
大腸がん検診
対象は40歳以上、年1回。検査方法は免疫法による便潜血検査(推奨グレードA)です。コクラン・レビュー(32万人以上)で大腸がん死亡率が16%減少することが確認されており、5大検診の中で最も費用対効果に優れた検診とされています [4]。全大腸内視鏡検査は対策型検診としては推奨されていません(グレードC)。
肺がん検診——2025年、18年ぶりの大改訂
2025年に日本肺癌学会が18年ぶりにガイドラインを改訂しました [8]。最大の変更点は、低線量コンピュータ断層撮影(低線量CT: 通常のCTより放射線量を大幅に減らした撮影法)検査が重喫煙者に対して推奨グレードAに格上げされたことです。
| 検査方法 | 対象 | 推奨グレード | 間隔 |
|---|---|---|---|
| 胸部X線検査 | 40-79歳(全員) | A | 年1回 |
| 低線量CT検査 | 50-74歳の重喫煙者(喫煙指数600以上) | A | 年1回 |
| 喀痰細胞診 | — | D(非推奨) | — |
乳がん検診
対象は40歳以上の女性、2年に1回。検査方法はマンモグラフィ(推奨グレードB)です。欧州委員会乳がんイニシアティブ(ECIBC)の系統的レビューでは、50~69歳では2年間隔が利益と害の最適なバランスであることが示されています [3]。年1回のスクリーニングは偽陽性が大幅に増加する一方、追加の利益はわずかでした。
子宮頸がん検診
対象は20歳以上の女性、2年に1回。従来の細胞診に加え、30歳以上ではヒトパピローマウイルス(HPV: 子宮頸がんの原因ウイルス)検査単独法(5年に1回)も選択肢となっています。HPV検査の中等度異形成以上の検出感度は約90%で、細胞診の約75%を上回ります。
がん検診の「利益」を定量する——死亡率減少効果のエビデンス
がん検診の最も重要な評価指標は「死亡率の減少」です。「がんが見つかった」「生存率が上がった」ではありません。なぜなら、検診によって診断が早まると、見かけ上の生存期間は延びますが、実際の死亡時期は変わらないことがあるからです(リードタイムバイアス)。
低線量CT肺がん検診——最も強力なエビデンス
肺がんの低線量CT検診は、現在のがん検診の中で最も強力な死亡率減少効果のエビデンスを持っています。
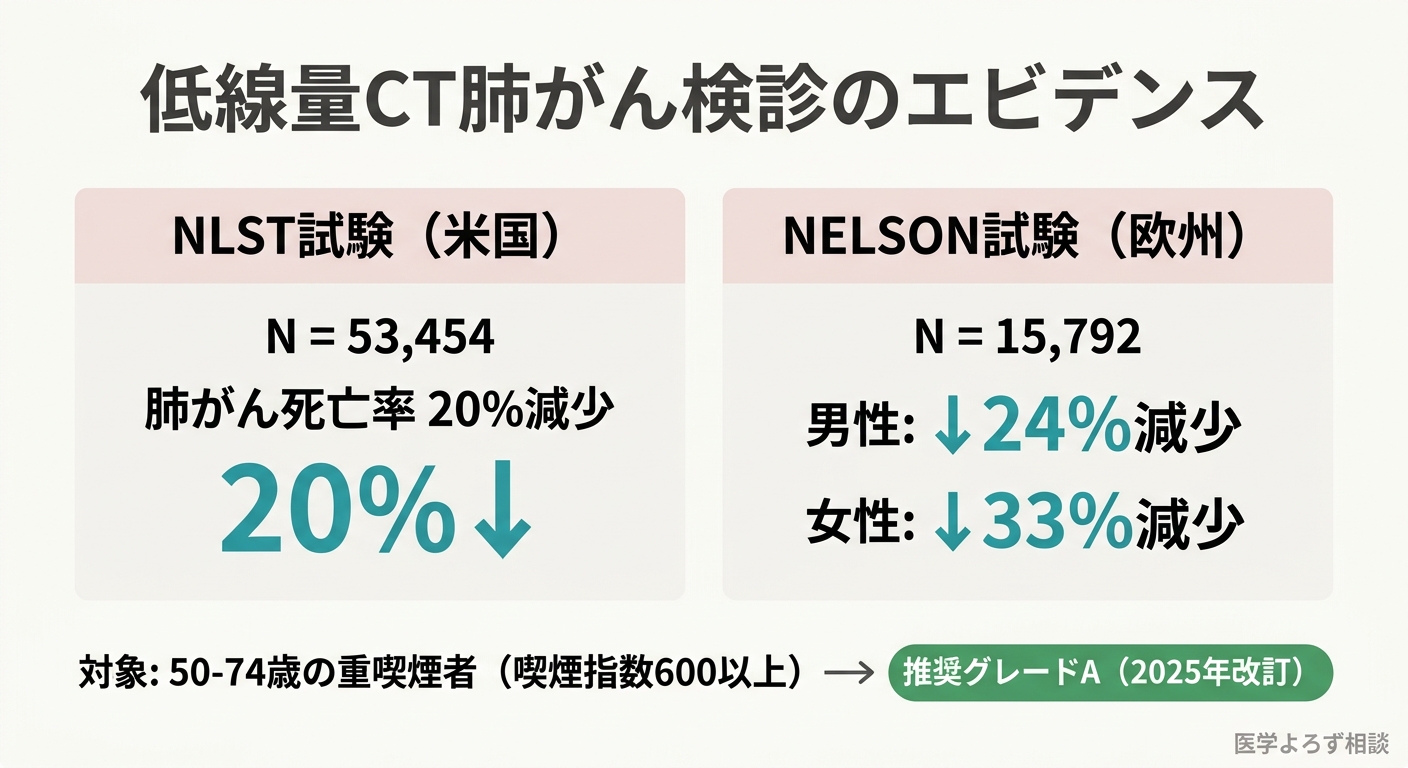
米国NLST試験(N=53,454)では、低線量CT群の肺がん死亡率が胸部X線群に比べて20%減少しました [5]。欧州NELSON試験(N=15,792)では、男性で24%、女性で33%の死亡率減少が確認されています [6]。
さらに、2026年に報告されたStockholm PLUSパイロット研究では、スウェーデンの重喫煙女性990名を対象に組織的な低線量CT検診を実施した結果、肺がん15例が検出され、そのうち87%がIA期(最も早い段階)で発見されました [9]。陽性的中率(PPV: 陽性結果のうち実際にがんだった割合)は24%で、組織的検診の実行可能性が実証されています。
ただし注意すべき点もあります。NLST試験では、陽性結果の約95%が偽陽性(がんではないのに陽性判定)でした。不必要な追加検査や生検が実施されるリスクがあることを、受診前に理解しておく必要があります。
マンモグラフィ乳がん検診——年齢と間隔が鍵
ECIBCの系統的レビュー(1 RCT + 13観察研究 + 11モデリング研究)は、マンモグラフィ検診の最適な間隔は年齢によって異なることを示しています [3]。
- 50~69歳: 2年間隔が最適。年1回にしても追加の利益はわずかで、偽陽性が大幅に増加する
- 45~49歳: 年1回にするメリットはさらに小さく、害の増加が大きい。利益と害のバランスは50~69歳より不利
- 70~74歳: より長い間隔でも利益は維持され、害が減る可能性がある
便潜血検査による大腸がん検診
コクラン・レビュー(32万人以上のデータ)により、免疫法便潜血検査による大腸がん死亡率の16%減少が確認されています [4]。スクリーニング必要数(NNS: 1人の死亡を防ぐために検診が必要な人数)は約900人です。自己負担500~1,000円で受けられる費用対効果の高い検診です。
がん検診の「害」を正直に語る——過剰診断・偽陽性・心理的影響
過剰診断——検診の最大のジレンマ
過剰診断とは、「治療しなくても生涯問題を引き起こさないがんが、検診によって発見・診断されること」です。これは検診の避けられない副作用であり、患者にとっては「がん」と告知され、不要な治療(手術・放射線・化学療法)を受けることを意味します。
Voss(2023年)らのシステマティックレビューでは、19のRCTを再分析し、バイアスリスクの高い試験を除外した結果、過剰診断率は17%~38%に達することが示されました [2]。重要なのは、多くの試験が過剰診断の推定を目的として設計されていなかったため、この数値でさえ過小評価の可能性があることです。
また、Senevirathna(2023年)らのスコーピングレビューでは、過剰診断の定量化方法が46研究で分析されましたが、方法によって結果が大きく乖離しており、標準化された方法が存在しないことが指摘されています [10]。つまり、「過剰診断が何%か」という問いに対する確定的な答えはまだなく、どの数字を見るかで印象が大きく変わるのが現状です。
偽陽性——「がんかもしれない」と言われる恐怖
偽陽性とは、がんでないのに検査で「陽性」と判定されることです。精密検査が必要になり、身体的・心理的な負担が生じます。検診で「要精検」と判定されても、約80~95%はがんではないことを覚えておいてください。ただし、精密検査を受けるまでの不安は、経験した人にしかわからないほど大きなものです。
PSA前立腺がん検診の論争——「推奨しない」の科学的根拠
前立腺がん検診は、がん検診における最も激しい議論の一つです。

Ilic(2013年)らのコクランシステマティックレビューは、5つのRCT(N=341,342)を統合分析しました [7]。その結果は明確です。
PSA検診は前立腺がん死亡率を有意に低下させませんでした(リスク比(RR: 介入群と対照群のリスクの比)1.00、95%信頼区間(CI: 真の値が存在する確率95%の範囲)0.86-1.17)。
ただし、5つのRCTのうちERSPC試験のみが、55~69歳の男性における前立腺がん死亡率の21%の有意な減少(RR 0.84, 95%CI 0.73-0.95)を報告しています。一方、米国PLCO試験は有意な利益を示しませんでした(RR 1.15, 95%CI 0.86-1.54)。
問題は、PSA検診による過剰診断が最大50%に達することです。前立腺がんと診断された場合、手術や放射線治療に伴う尿失禁や勃起障害といった副作用のリスクがあります。「がんが見つかったのに治療しない」という選択は、心理的に極めて困難です。
日本では、前立腺がんPSA検診は対策型検診として非推奨(グレードC)とされています。任意型検診(人間ドック等)として受ける場合は、利益と害を十分に理解した上での個別判断が求められます。
MCED検査(多がん早期発見)の最前線——期待と慎重さ
液体生検とcfDNA——血液1本で50種類以上のがんを検出?
多がん早期発見検査(MCED)は、血液中の細胞遊離DNA(cfDNA: がん細胞から血液中に放出されるDNA断片)のメチル化パターンを解析することで、50種類以上のがんの信号を1回の血液検査で検出しようとする技術です。その代表がGRAIL社のGalleri検査です。
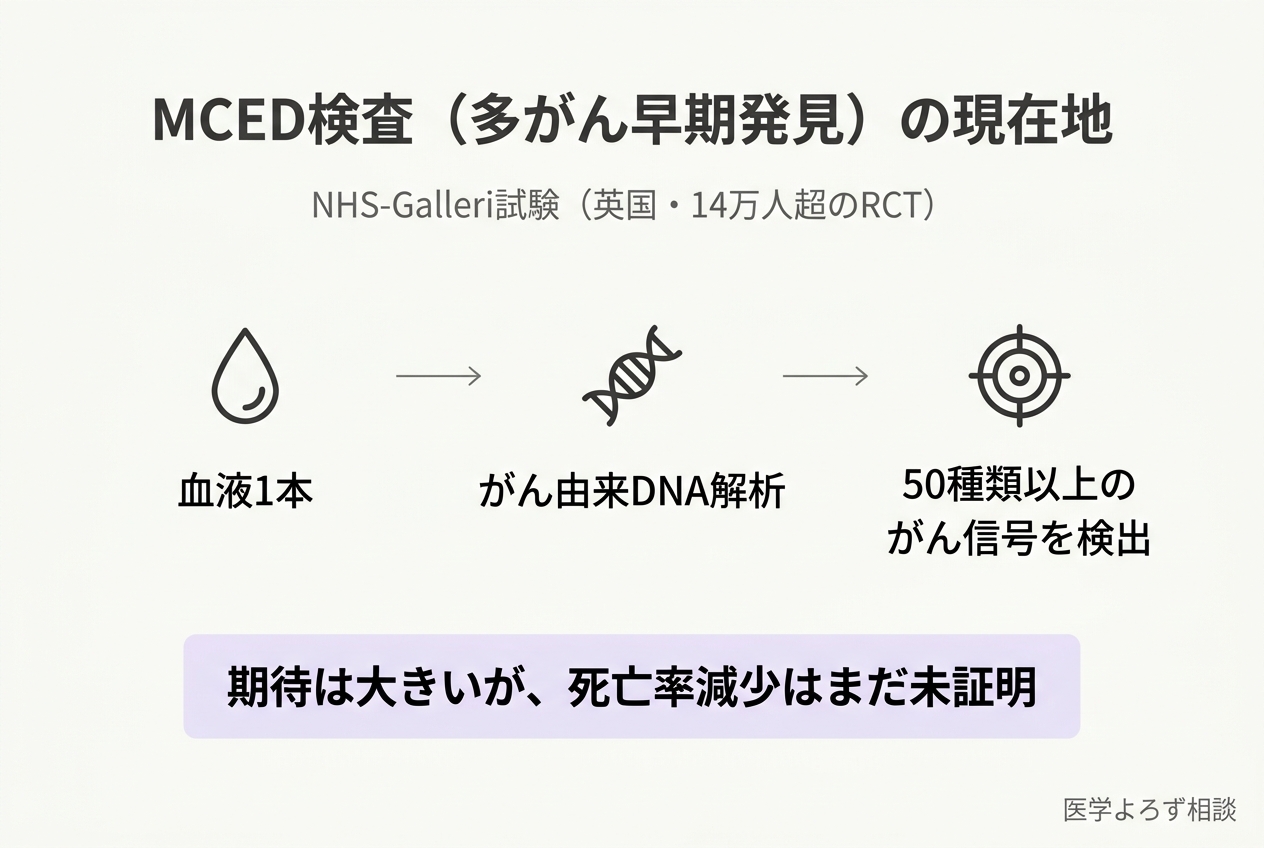
NHS-Galleri試験——14万人超の大規模RCT
英国で進行中のNHS-Galleri試験は、14万人以上を対象とした大規模RCTです。Marlow(2026年)らの質的研究では、がん信号が検出された41名にインタビューを実施し、診断プロセスの体験が極めて多様であることが明らかになりました [11]。がん信号の検出部位によって必要な検査や医療スタッフとの接触回数が大きく異なり、患者ナビゲーション(患者を適切な診療に導く支援体制)の必要性が強調されています。
Marlow(2023年)らは、NHS-Galleri試験内に心理的影響評価プロトコルを組み込んでいます [12]。がん信号が検出された約700名を3時点で追跡し、不安・スクリーニングの心理的帰結・結果の理解度を評価するものです。MCED検査が広く導入された場合に予想される心理的影響を、事前に科学的に評価しようとする先見的な取り組みです。
現時点でのMCED検査の限界
MCED検査について、正直に伝えるべき事実があります。
- ステージI(最早期)の感度は約20~30%にとどまる。「早期発見」を謳いながら、最も早い段階のがんの大部分を見逃す
- 陽性的中率(PPV)は61.6%。陽性と判定されても約4割はがんではない
- 死亡率減少効果は未証明。がんを「見つける」ことと「死亡率を下げる」ことは同義ではない。この点が証明されるまで、対策型検診への導入は時期尚早
新技術への期待と慎重さ——公衆の嗜好とAI画像診断
新しいがん検診に人々は何を求めているか
Har(2025年)らのシステマティックレビューは、新興がんスクリーニング技術に対する公衆の嗜好を調べた23の離散選択実験(DCE: 仮想的な選択肢を提示して人々の好みを定量化する研究手法)を統合分析しました [13]。液体生検5件、ゲノム検査8件を含む分析から、以下のことが明らかになっています。
- 感度が最も重要な属性として挙げられた。人々は「見逃さない検査」を最も重視する
- 一方でデータプライバシーへの懸念も強く、ゲノム検査では遺伝情報が保険や雇用に影響する可能性への不安が表明されている
- 検査の利便性・低コスト・低侵襲性も重要な決定因子である
前立腺がん検診の次世代——リキッドバイオプシーへの展開
Sequeira(2024年)らのシステマティックレビュー(24研究)は、液体生検ベースのバイオマーカーが前立腺がんのリスク層別化に有望であることを示しています [14]。尿ベースのバイオマーカーが全体の54.2%を占め、PSAに代わるより精度の高いスクリーニングツールの開発が進んでいます。ただし、リスクグループの分類基準が研究間で統一されておらず、臨床実装にはバイオマーカーの標準化と検証が不可欠です。
AI画像診断の併用
人工知能(AI)を用いた画像診断支援は、マンモグラフィや低線量CT検診の読影精度を向上させる可能性があります。放射線科医の読影にAIを「ダブルチェック」として併用するアプローチは、偽陽性を減らしつつ感度を維持する方向で研究が進んでいます。ただし、大規模RCTでの検証はまだこれからの段階です。
日本の読者へ——年齢別の推奨一覧と受診判断チェックリスト
対策型検診(自治体のがん検診)の推奨一覧
| がん種 | 対象年齢 | 間隔 | 検査方法 | 推奨 | 自己負担目安 |
|---|---|---|---|---|---|
| 胃がん | 50歳以上 | 2年に1回 | X線 or 内視鏡 | B | 1,500-3,000円 |
| 大腸がん | 40歳以上 | 年1回 | 便潜血検査 | A | 500-1,000円 |
| 肺がん(X線) | 40-79歳 | 年1回 | 胸部X線 | A | 500-1,000円 |
| 肺がん(CT) | 50-74歳の重喫煙者 | 年1回 | 低線量CT | A | 自治体による |
| 乳がん | 40歳以上女性 | 2年に1回 | マンモグラフィ | B | 1,000-2,000円 |
| 子宮頸がん | 20歳以上女性 | 2年に1回 | 細胞診 / HPV | A/B | 500-1,000円 |
受診判断チェックリスト
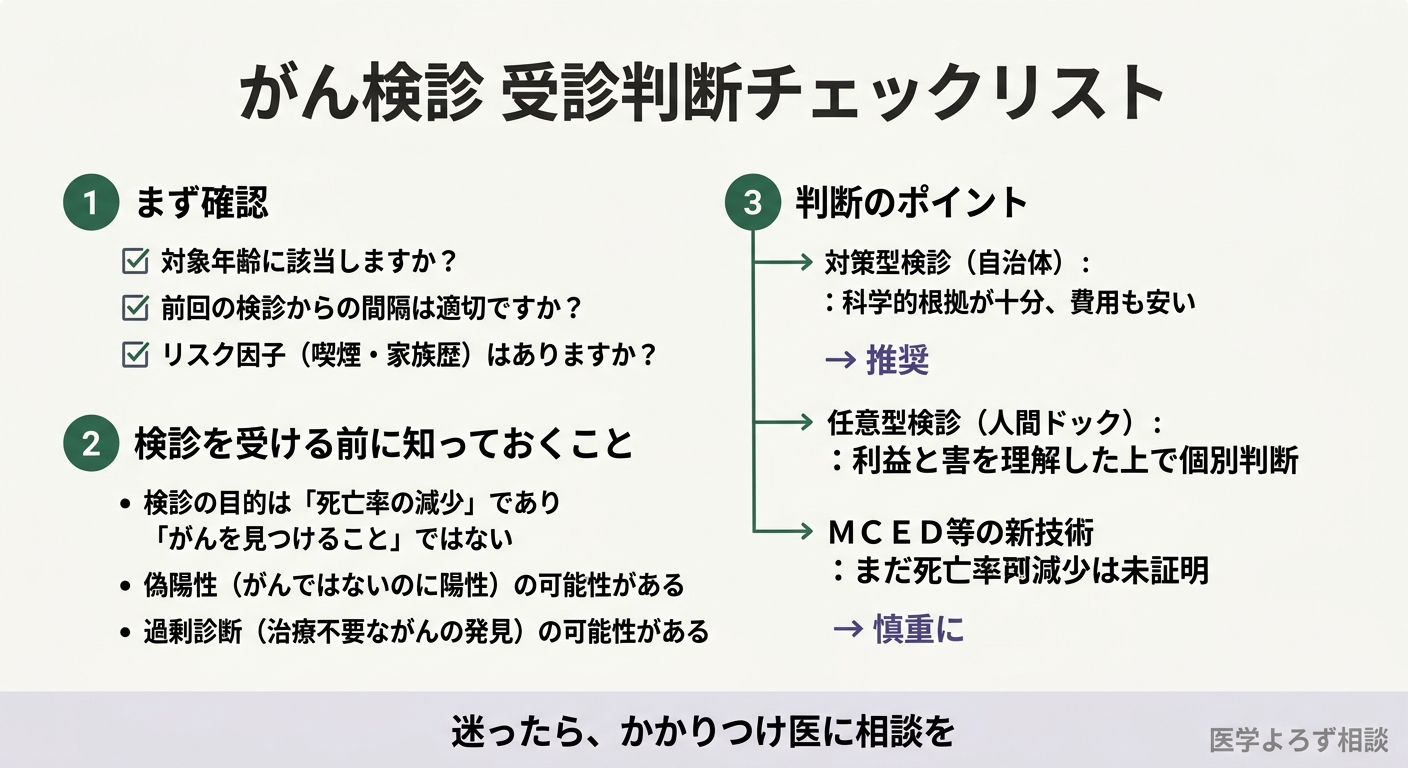
「精密検査が必要」と言われたら
検診で「要精検」と判定されても、約80~95%は「がんではない」ことを覚えておいてください。しかし、精密検査は必ず受けてください。検診の利益は、精密検査を受けて初めて完結します。
医師の見解
がん検診は「受けるべきか、受けないべきか」という二者択一の問題ではありません。
対策型検診(自治体のがん検診)については、対象年齢に該当するなら受診を推奨します。 科学的根拠に基づいて死亡率減少効果が確認された検査のみが推奨されており、費用も低廉です。特に大腸がん検診(便潜血検査)は年1回、わずか500~1,000円で受けられる最も費用対効果の高い検診です。
一方、MCED検査などの新技術については、現時点では慎重な姿勢が必要です。 「血液1本で50種類のがんを検出」という謳い文句は魅力的ですが、ステージIの感度は20~30%にとどまり、何よりも死亡率減少効果がまだ証明されていません。「がんを見つけること」と「がんによる死亡を減らすこと」は同義ではない——この原則を忘れないでください。
PSA前立腺がん検診については、55~69歳の男性で個別に相談する価値があります。ただし、過剰診断が最大50%に達するという事実と、治療に伴う副作用のリスクを十分に理解した上での判断が求められます。
最後に一つ。検診で「要精検」と言われた場合、必ず精密検査を受けてください。約80~95%はがんではありませんが、残りの5~20%にとっては、その精密検査が命を救う可能性があります。
関連記事: