はじめに:「エクソソーム治療」という言葉に惹かれたあなたへ
「エクソソームで若返り」「幹細胞エクソソームで薄毛改善」——SNSや美容クリニックの広告で、こうした言葉を目にする機会が急増しています。
2023年時点で、日本国内でエクソソーム治療を提供する医療機関は669施設に達しました[1]。アンチエイジング、育毛、美肌、関節痛——さまざまな効果が謳われ、1回あたり数万円から数十万円の費用がかかる自由診療として急速に普及しています。
しかし、その実態はどうでしょうか。
2026年4月現在、FDA(米国食品医薬品局)が承認したエクソソーム治療製品は世界にゼロです[11]。日本でも薬事承認された製品は存在しません。厚生労働省は2024年7月に全国の都道府県に対してエクソソーム製品の販売監視強化を通達し[14]、日本再生医療学会は安全性ガイダンスを公表しました[12]。
この記事では、エクソソーム治療について「何がわかっていて、何がわかっていないのか」を、最新のシステマティックレビューと公的機関の情報に基づいて整理します。期待に応える内容もあれば、厳しい現実もあります。しかし、あなたの健康に関わる決断だからこそ、科学的な事実を知ったうえで判断していただきたいのです。
エクソソームとは何か——細胞が放つ「メッセージカプセル」
細胞間コミュニケーションの主役
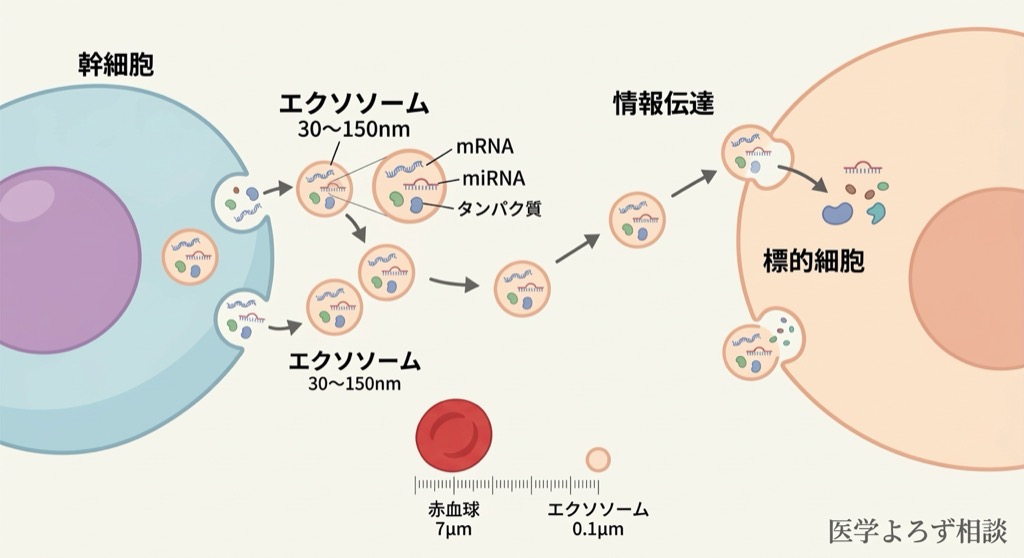
エクソソーム(exosome)とは、ほぼすべての細胞が分泌する直径30〜150ナノメートル(1ナノメートルは100万分の1ミリ)の微小な膜小胞です。細胞外小胞(Extracellular Vesicles: EVs)の一種であり、内部にタンパク質、脂質、mRNA、miRNAなどの生理活性物質を含んでいます。
かつてエクソソームは「細胞のゴミ」と考えられていましたが、1990年代以降の研究で、細胞間の情報伝達を担う「メッセージカプセル」としての役割が明らかになりました。エクソソームは血液や体液中を移動し、離れた場所にある細胞に情報を届けることで、免疫調節、組織修復、炎症制御などに関与しています。
なぜ治療に使おうとするのか
再生医療では従来、幹細胞そのものを体内に投与する方法(細胞治療)が主流でした。しかし、細胞治療には以下の課題があります:
- 腫瘍形成リスク: 移植した細胞ががん化する可能性
- 免疫拒絶反応: 他人の細胞を使う場合の拒絶
- 品質管理の困難さ: 生きた細胞の保存・輸送が難しい
エクソソームは細胞ではなく「分泌物」であるため、理論上これらのリスクが低減される可能性があります。これが「セルフリー(細胞を使わない)再生医療」として注目される理由です。
臨床エビデンスの現在地——領域別に検証する
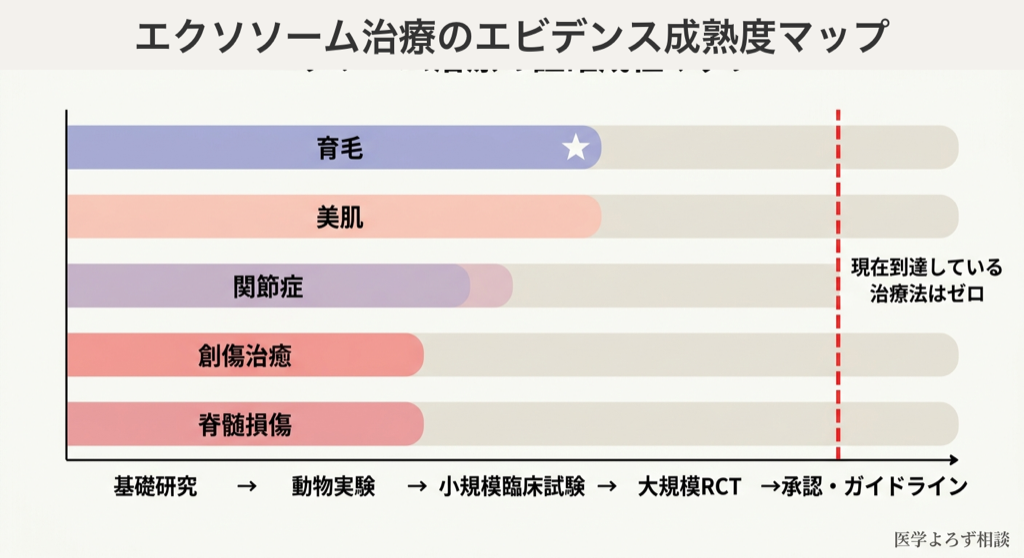
エクソソーム治療の臨床研究は急速に増加しています。世界で約240件の臨床試験が登録されていますが、その大半は早期段階(Phase I/II)です[2]。ここでは、消費者の関心が高い3つの領域について、最新のシステマティックレビューに基づいて現状を整理します。
育毛(脱毛症)——最も臨床データが蓄積された領域
育毛は、エクソソーム治療の中で最もヒト臨床データが蓄積されている領域です。
2025年に発表されたシステマティックレビューでは、11件の臨床研究(RCT 2件、後方視的研究3件、前向き単群研究3件、症例シリーズ1件、症例報告2件)が解析されました[3]。主な結果は以下の通りです:
- 毛髪密度: 9.5〜35本/cm²の増加
- 毛髪径: 最大13.01μmの増加
- 患者満足度: 概ね高評価(10点中8.5点のRCTあり)
- 重篤な有害事象: 報告なし(軽度の一過性発赤が20%に出現)
別のレビューでも9件の臨床研究(125名の脱毛症患者)で全研究が少なくとも1つの毛髪パラメーターの改善を報告しています[4]。
ただし、重大な限界があります:
- サンプルサイズが極めて小さい(最大でも85名)
- プラセボ対照のRCTは2件のみ
- 使用されるエクソソームの由来(脂肪、臍帯、骨髄など)、濃度、投与法がバラバラ
- 長期追跡データがない(最長でも96週間)
- 研究間の異質性が高く、メタアナリシスが実施できていない
皮膚の若返り(スキンリジュベネーション)
2026年2月に発表された最新のシステマティックレビューでは、19件のヒト研究が解析されました[9]。
エクソソームベースの治療は、肌の質感、弾力性、しわの改善に有効性を示唆する結果が得られています。しかし同時に、少なくとも10件の重篤な有害事象が報告されており、安全性への懸念も指摘されています。
大規模なRCTは存在せず、エビデンスの質は総じて低い段階にとどまっています。
変形性関節症(OA)
変形性膝関節症に対するエクソソーム治療は、前臨床研究では有望な結果が示されていますが、ヒトの大規模臨床試験データは極めて限定的です。
2025年の研究では、PRP(多血小板血漿)中のエクソソームサイズが膝OA治療の転帰に影響する可能性が示唆されました[10]。しかし、エクソソーム単独での治療効果を検証した質の高いRCTは、2026年4月時点で存在しません。
前臨床レベルでは、脂肪由来幹細胞エクソソームが軟骨再生を促進するという複数のシステマティックレビューがありますが、動物モデルの結果をそのままヒトに外挿することはできません。
安全性リスク——「細胞ではないから安全」は本当か
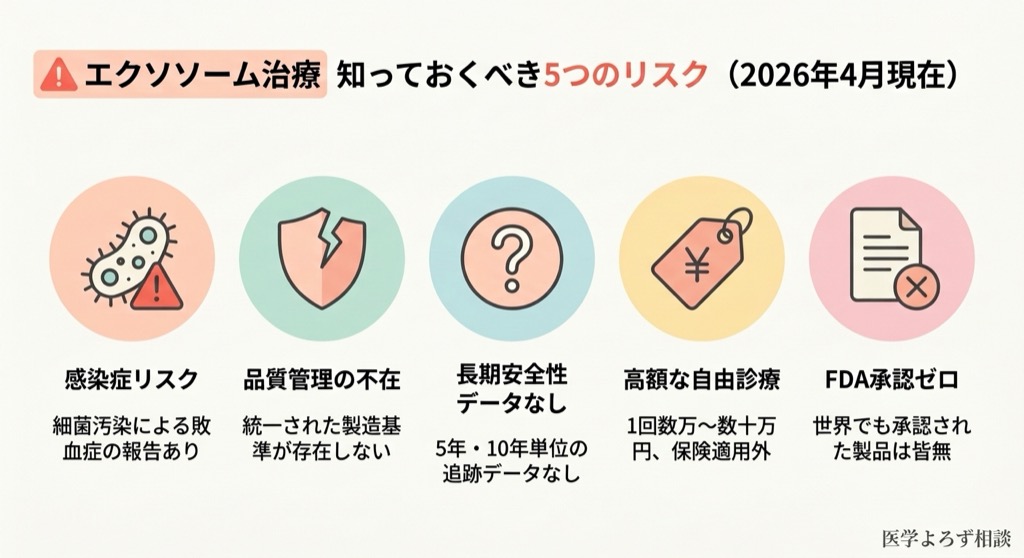
エクソソーム治療の推進者は、「細胞を使わないから安全」と主張します。しかし、実際のデータはその楽観を許しません。
FDAが警告する重篤な有害事象
FDAは2019年にエクソソーム製品に関する公式安全性通知を発出し、以下のリスクを警告しました[11]:
- 重篤な感染症(細菌汚染による敗血症など)
- アレルギー反応
- 腫瘍形成の可能性
2024〜2025年にかけて、FDAはEvolutionary Biologics社、Chara Biologics社、New Life Medical Services社に対して警告書を発出し、未承認のエクソソーム製品の販売中止を命じています。
日本での健康被害
日本では2023年に、自由診療の再生医療で死亡事例が報告されています。東京都中央区のクリニックで脂肪由来幹細胞の点滴投与を受けた50代の女性が治療中に急変し、死亡しました。また、エクソソーム投与後にがんの増悪がみられたにもかかわらず治療が続けられた事例も報じられています。
これらはエクソソーム「単独」の事例とは限りませんが、自由診療における再生医療全般の安全管理の問題を浮き彫りにしています。
品質管理の根本的な課題
現在のエクソソーム製品には、以下の品質管理上の問題があります:
| 課題 | 内容 |
|---|---|
| 由来の多様性 | 脂肪、臍帯血、骨髄、植物など由来が異なり、成分も効果も異なる |
| 製造標準の不在 | 統一された製造・精製基準がなく、製品間の品質差が大きい |
| 濃度・含有物のばらつき | エクソソームの数や内容物が製品ごとに異なる |
| 保存・輸送の困難さ | 温度管理の不備で内容物が失活する可能性 |
| 定義の曖昧さ | 実際には他の細胞外小胞や不純物を含む製品も多い |
規制の最前線——日米はどう動いているか
米国FDA:「ゼロトレランス」の姿勢
FDAの立場は明確です。エクソソーム製品はいかなる医療用途にも承認されていない[11]。
FDAはエクソソームを「生物学的製剤」として規制する方針であり、臨床使用には治験届(IND)の提出と臨床試験の実施が必要です。しかし現実には、「幹細胞クリニック」が独自の解釈で未承認エクソソーム製品を販売し続けており、FDAは2024年以降だけで複数の警告書を発出しています。
日本:急速な規制整備の動き
日本では、再生医療等安全性確保法(安確法)がエクソソームを直接的には規制していませんでした。しかし、急速な自由診療の拡大を受けて、規制整備が加速しています。
主な動き:
- 2023年11月: 日本再生医療学会(岡野栄之理事長)がエクソソームに関する提言を発表[13]。科学的エビデンスが不十分な段階での安易な臨床応用に注意喚起。
- 2024年4月: 日本再生医療学会が「細胞外小胞等の臨床応用に関するガイダンス」を公表[12]。再生医療と同等の安全性・品質基準を求める。
- 2024年7月: 厚生労働省が全国の都道府県に対してエクソソーム製品の販売監視強化を通達[14]。
- 2024年10月: 京都大学iPS細胞研究所・国立がん研究センターがStem Cell Reports誌で規制整備の必要性を指摘する論文を発表[1][15]。
日本再生医療学会のガイダンスは、エクソソーム治療を提供する医療機関に対して、以下を求めています:
- 再生医療と同レベルの安全性・品質管理
- 製造・保管・投与の適切な管理
- リスクとエビデンスレベルについて患者への正確な情報提供
科学の現在地:わかっていること、いないこと
確立された知見
- エクソソームは細胞間コミュニケーションに重要な役割を果たしている
- 前臨床研究(動物実験)で、エクソソームの治療効果を示す多数のデータが存在する
- 育毛領域では小規模ながらヒトでの有効性を示唆する臨床データがある[3][4]
- エクソソーム製品の品質は由来・製造法によって大きく異なる
- 2026年現在、いかなる国でも承認されたエクソソーム治療製品は存在しない[11]
未解明点・限界
- 長期安全性: 5年、10年単位での安全性データが存在しない
- 最適な投与法: 由来、濃度、投与経路、回数の最適化が未確立
- 作用メカニズムの全貌: エクソソーム内のどの成分がどの効果に寄与するか解明途上
- 品質標準: 製品の品質を保証する国際的な規格がない
- コスト対効果: 既存の標準治療と比較した費用対効果のデータがない
- 個人差への対応: 誰に、どのタイプのエクソソームが最も有効かの予測法がない
実践チェックリスト:エクソソーム治療を勧められたとき
もし医療機関でエクソソーム治療を勧められた場合、以下のポイントを確認してください。
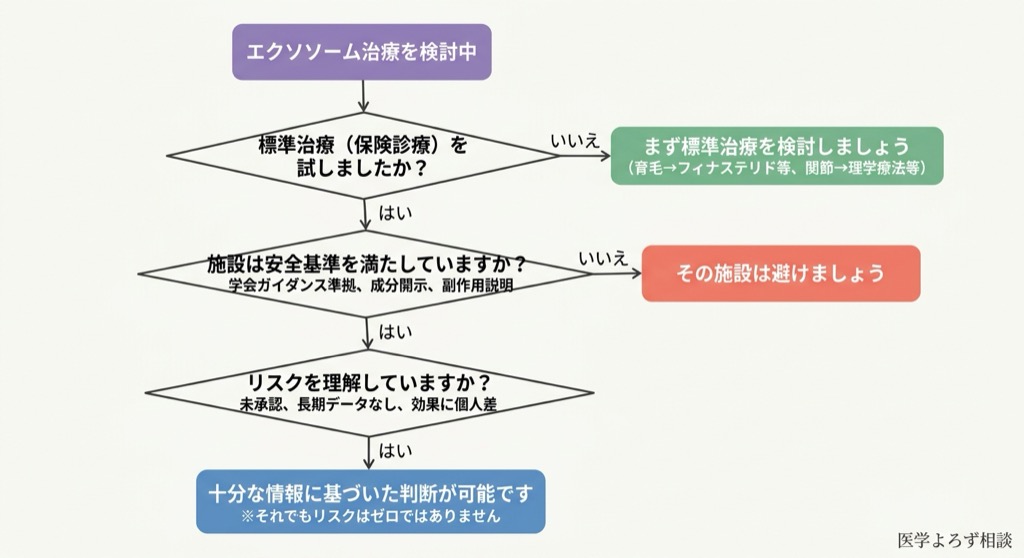
必ず確認すべき5つの質問:
-
「この治療はFDAまたは厚生労働省に承認されていますか?」 →2026年4月現在、承認製品は存在しません。「承認済み」と回答する施設は虚偽です。
-
「使用するエクソソームの由来、製造法、品質検査データを開示できますか?」 →日本再生医療学会のガイダンスでは、透明な情報開示を求めています。
-
「起こりうる副作用とその対処法を説明してください」 →感染症、アレルギー反応、がんの増悪リスクについて十分な説明があるべきです。
-
「この治療のエビデンスレベルはどの程度ですか?大規模RCTの結果はありますか?」 →現時点では小規模研究のみ。大規模RCTは存在しないことを理解しましょう。
-
「標準治療(保険診療)と比較した場合の利点は何ですか?」 →育毛ならフィナステリド/ミノキシジル、関節症なら理学療法やヒアルロン酸など、エビデンスが確立された標準治療が存在します。
避けるべき危険信号(レッドフラッグ):
- 「エクソソームで〇〇が治る」と断言する
- 副作用やリスクの説明がない、または「副作用はありません」と言う
- 「FDA承認」「学会認定」など虚偽の表現を使う
- 高額なパッケージ契約を急かす
- 成分や由来の詳細を開示しない
おわりに:科学的な希望と、冷静な判断のあいだで
エクソソーム研究は、再生医療の未来を切り拓く可能性を秘めています。細胞そのものを使わない「セルフリー治療」という概念は革新的であり、前臨床データは確かに有望です。
しかし、「有望な基礎研究」と「安全で有効な臨床治療」のあいだには、長い道のりがあります。薬が患者に届くまでには、Phase I(安全性)→ Phase II(有効性)→ Phase III(大規模検証)→ 承認審査という、通常10〜15年のプロセスが必要です。エクソソーム治療は、このプロセスの初期段階にあります。
問題は、科学的検証が完了する前に、商業的な提供が先行していることです。日本の669施設で提供されている治療のほとんどは、十分なエビデンスに基づいていません。「最先端」という言葉の響きに惑わされず、現時点でのエビデンスレベルを正しく理解することが、あなた自身と家族の健康を守る第一歩です。
今後、大規模RCTの結果が出揃い、品質基準が整備されれば、エクソソーム治療が標準的な医療として認められる日が来るかもしれません。その日まで、科学的な希望を持ちつつ、冷静な判断を続けていきましょう。
本日のまとめ
- エクソソーム治療の本質: 細胞間コミュニケーションを担う微小カプセルを利用した「セルフリー再生医療」の試み。前臨床では有望だが、ヒトでの大規模検証は未完了。
- 現時点でのエビデンス: 育毛領域で小規模な臨床データあり。美肌・関節症は前臨床〜小規模臨床段階。FDA承認製品はゼロ。
- 判断に迷ったら: まず保険適用の標準治療を検討し、それでもエクソソーム治療を希望する場合は、5つの質問で施設の信頼性を確認してください。
関連記事:
